


第一作者:方瀟
通訊作者:丁勇教授
通訊單位:蘭州大學
論文DOI:10.1039/D5EE00652J
全文速覽
人工光合成是一種有潛力的過氧化氫(H2O2)生產策略,但較差的電荷分離和轉移限制了光催化效率。本工作在三元堿金屬鹽(LiCl/NaCl/KCl)中合成了具有電子勢阱效應的鈉/鉀聚(七嗪亞胺)(NaK-PHI)光催化劑,以提高電荷的傳輸效率和光催化活性。NaK-PHI通過?O2?參與和1O2參與的氧還原(ORR)反應和四電子水氧化(WOR)反應途徑合成H2O2。引入的氰基(?C≡N)作為吸電子基團可以提高PHI的局部負電荷密度,并通過吸引空穴加速載流子的分離。引入Na+和K+會觸發電子勢阱效應,光生電子被捕獲在NaK-PHI上,從而抑制電子-空穴對的復合。得益于?C≡N和堿金屬離子形成的強內建電場,NaK-PHI在純水中的H2O2生成速率為672.5 μmol g-1h-1,優于大多數報道的氮化碳光催化劑。NaK-PHI在420 nm處的表觀量子產率為13.9%,太陽能到化學能的轉換效率為0.68%。這種利用內建電場驅動力來改善光生載流子遷移和傳輸的策略為高效的人工光合成H2O2提供了一種新方法。
研究背景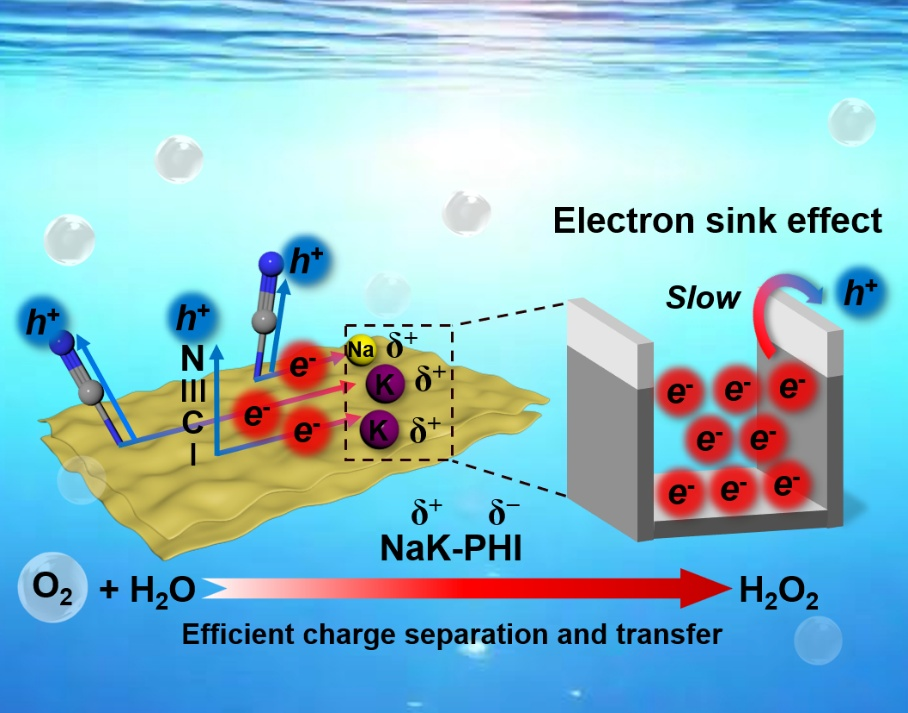
H2O2在化學工業中被用作原料,廣泛用于漂白、醫療消毒和水處理。鑒于其高能量密度和液體儲存運輸的能力,它也被認為是一種有前景的氫能載體。人工光合成H2O2是一種極具潛力的綠色途徑,近年來備受關注。氮化碳(CN)是一種制備簡單、原料豐富的有機半導體材料。其中,金屬聚(七嗪亞胺)(M-PHI)是一種新型的離子型CN,已被公認為是一種高活性的光催化劑。到目前為止,由一元和二元堿金屬鹽制備的PHI已被廣泛用于犧牲劑(如異丙醇、甘油、乙醇、甲醇等)條件下的光催化H2O2合成。三元熔鹽法制備的CN光催化機理和堿金屬在促進H2O2合成中的作用仍有待研究。
光催化合成H2O2主要通過載流子轉移途徑實現。載流子轉移途徑產生光生載流子和自由基中間體。特別是在純水系統中,光催化劑在沒有犧牲劑、助催化劑或調節溶液pH值的情況下分離和轉移電荷是非常具有挑戰性的。為了解決這一問題,一種有效的方法是在半導體中引入電子陷阱態,允許激發的電子局域化,從而抑制載流子的復合。我們使用堿金屬離子來捕獲光生電子,使用?C≡N基團來吸引光生空穴,在無犧牲劑下促進電荷分離,從而在純水中光催化合成H2O2。
本文亮點
1.開發了一種低熔點的三元熔鹽法制備NaK-PHI,?C≡N基團、Na+和K+同時引入到NaK-PHI中以控制電子-空穴分離。
2.證明了NaK-PHI的H2O2合成是通過?O2?參與和1O2參與的氧還原反應以及四電子水氧化反應途徑實現的。
3.建立了電子勢阱模型,以全面了解NaK-PHI中光生載流子的有效分離和轉移。利用穩態表面光電壓(SPV)和瞬態光電壓(TPV)測試證明了NaK-PHI的電子勢阱效應。
圖文解析
NaK-PHI是在三元共晶鹽(LiCl/NaCl/KCl)中合成的。作為吸電子基團,?C≡N基團增強了CN的局部負電荷密度,并捕獲光生空穴以分離載流子。在PHI中引入堿金屬離子充當電子陷阱態,增加了電荷分離的程度。在?C≡N基團和堿金屬離子誘導的強內建電場下,NaK-PHI通過不同的ORR反應和四電子WOR途徑實現了無需犧牲試劑的光催化合成H2O2。
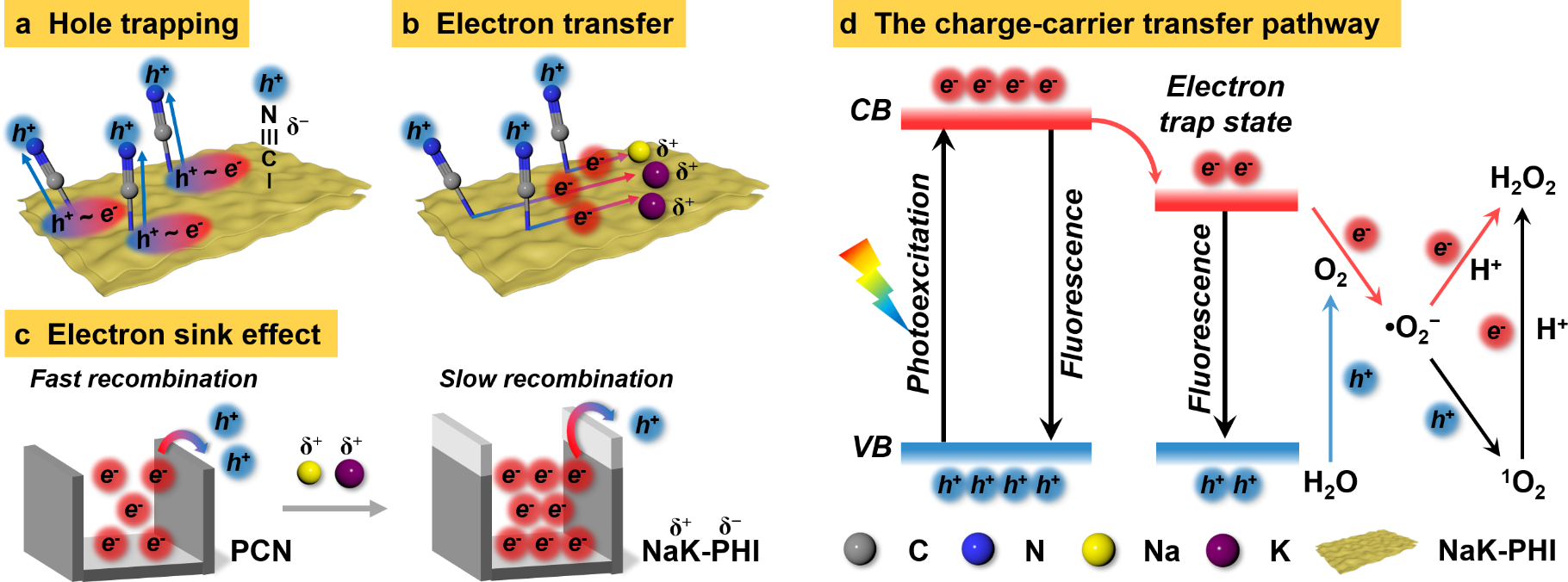
圖1.具有電子勢阱效應的NaK-PHI通過ORR和WOR途徑合成H2O2
NaK-PHI是通過低熔點(mp=354.4°C)的LiCl/NaCl/KCl熔鹽法制備的。FTIR、XPS和ICP測試證明了?C≡N基團和Na+和K+的引入。
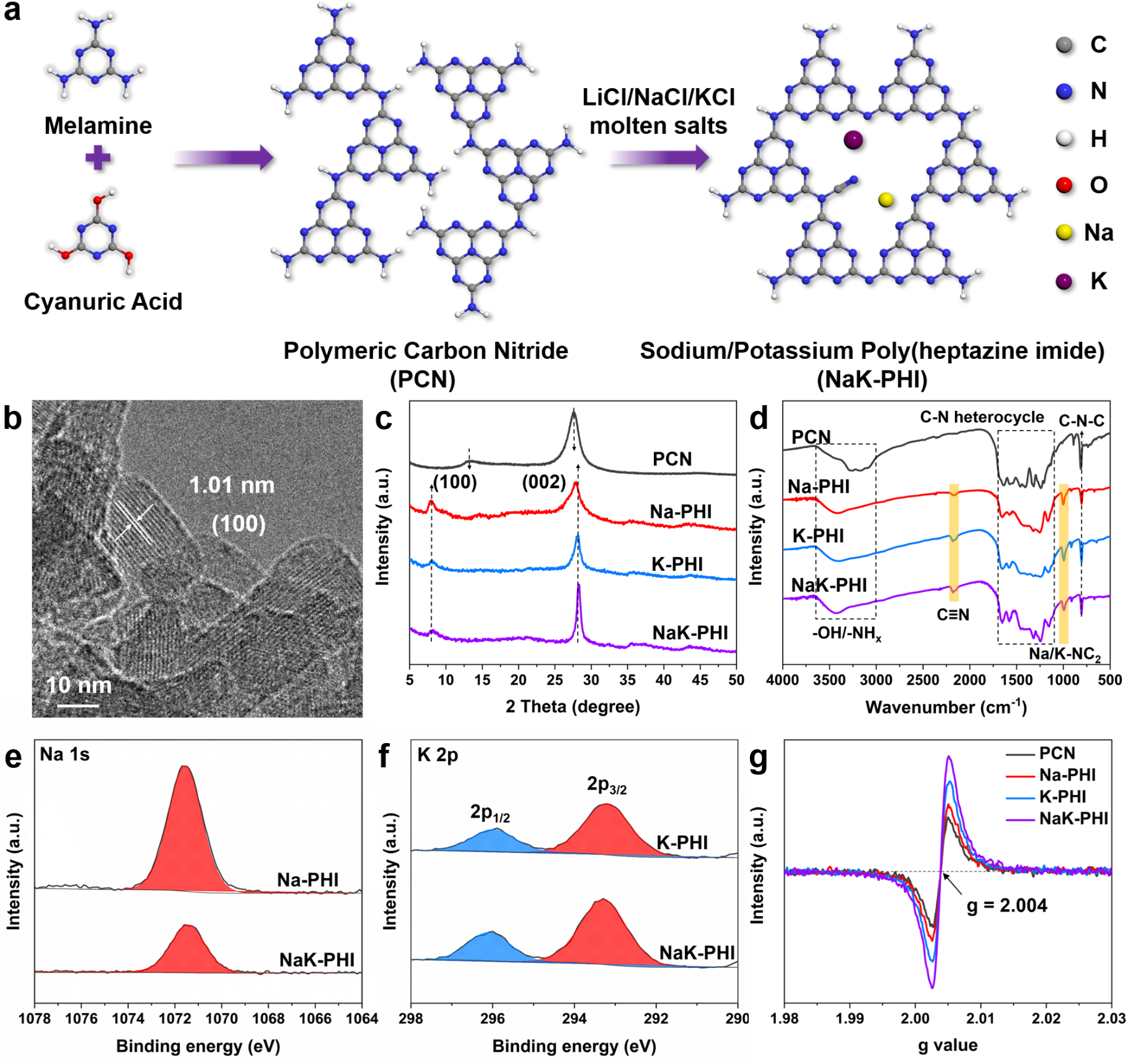
圖2. 目標催化劑的合成和表征
樣品的所有導帶值都高于O2還原電位,確保催化劑在熱力學上有利于H2O2的生成。NaK-PHI的價帶值足夠正,可以進行四電子WOR反應。與PCN相比,其他樣品的壽命較短,熒光強度較弱,表明PHI樣品的熒光快速淬滅。引入?C≡N基團和堿金屬離子大大抑制了光生電荷的復合。
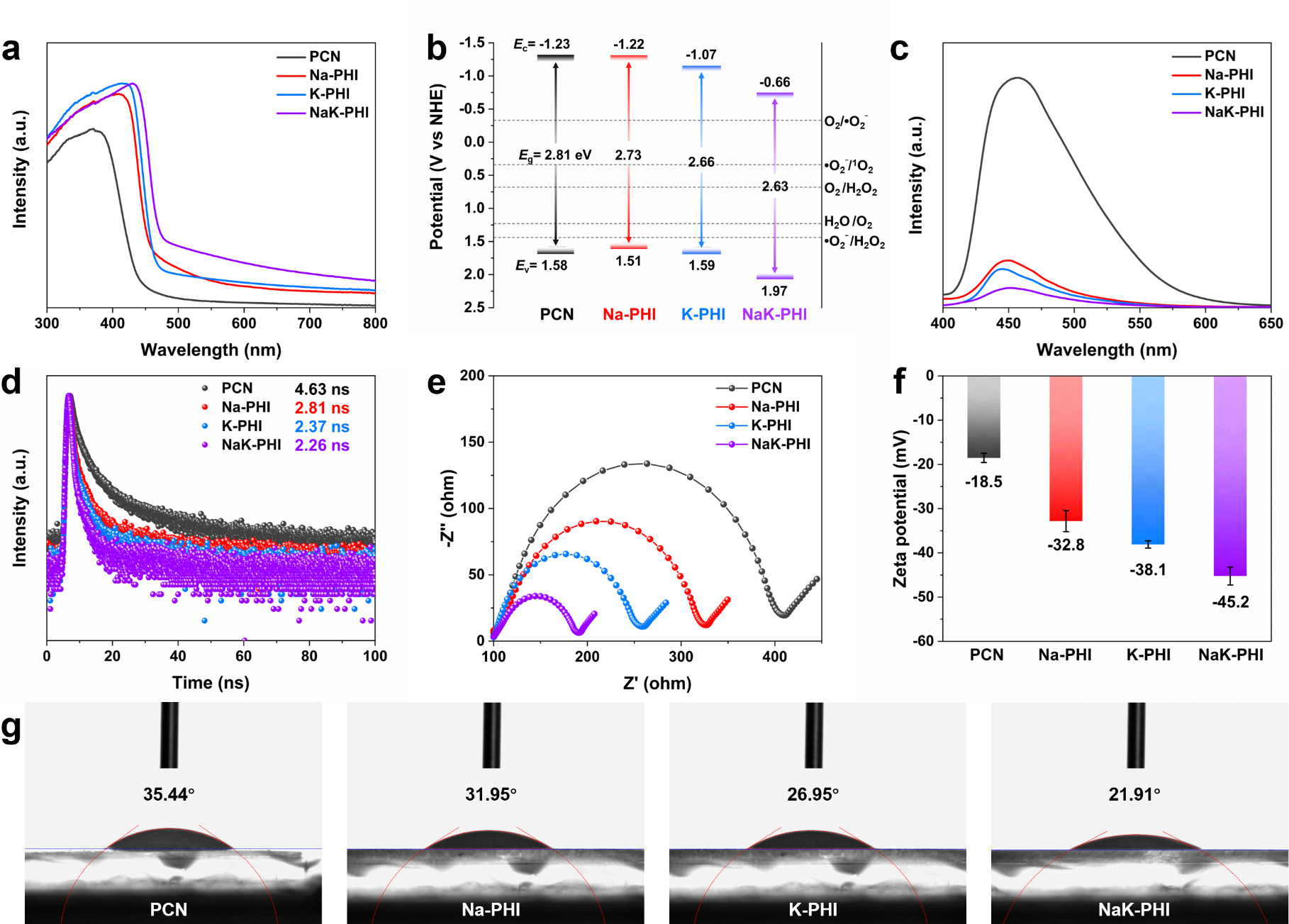
圖3. 目標催化劑的光電性質和電子結構
H2O2的產生通過三種途徑進行:1)兩步ORR(O2→?O2?→H2O2);2)有1O2參與的ORR(O2→?O2?→1O2→H2O2);3)四電子WOR(H2O→O2→H2O2)。值得注意的是,路徑2和3突出了光生空穴的有效利用。通過消耗光生空穴形成1O2和O2可以改善載流子分離并促進ORR。因此,ORR和WOR的協同作用有效地提高了光催化生成H2O2的效率。
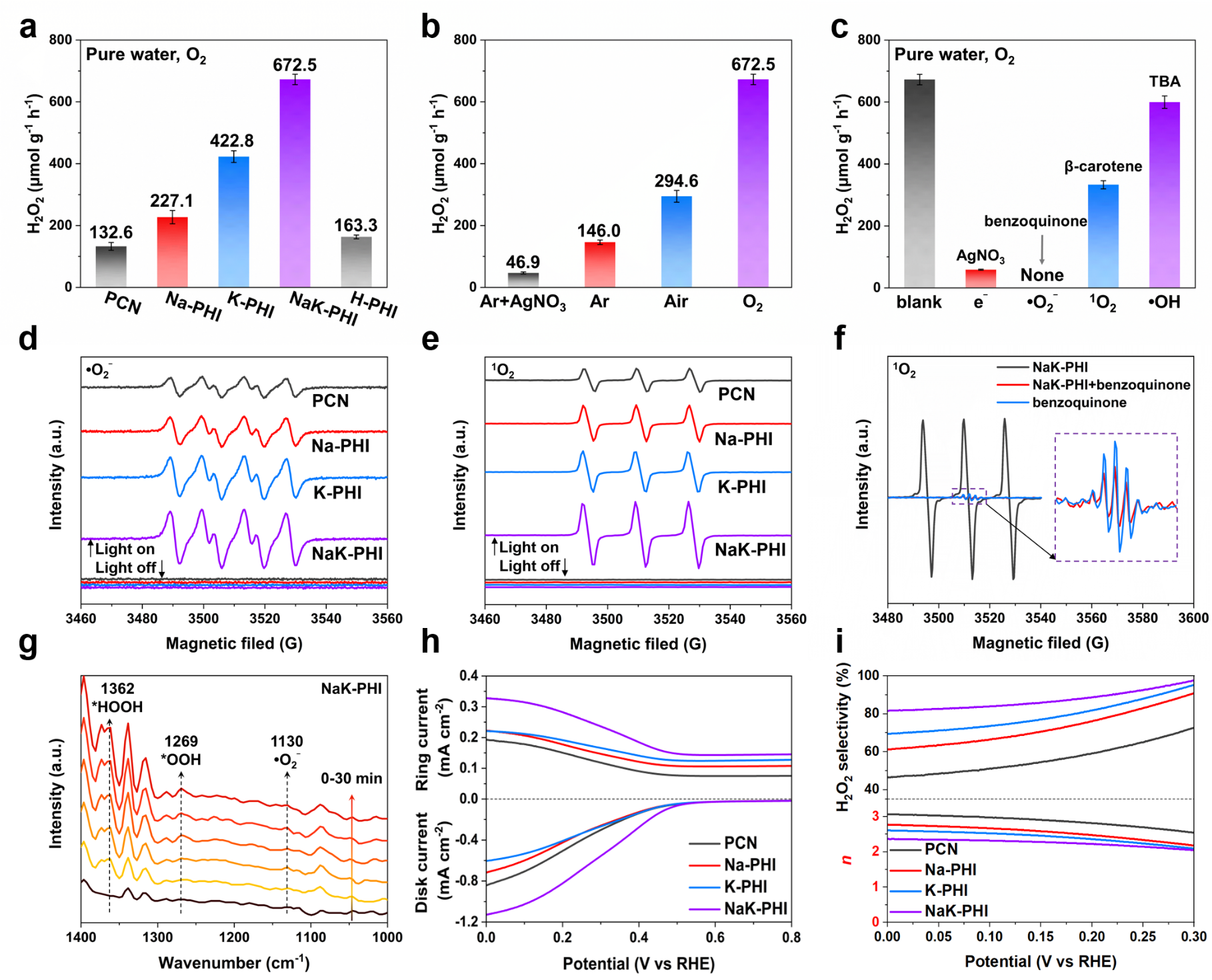
圖4. 催化劑合成H2O2性能和反應途徑
通過理論計算發現,?C≡N基團作為吸電子基團,在引入CN結構時會吸引周圍電子。引入?C≡N基團可以提高CN的局部負電荷密度,通過吸引光生空穴加速載流子的分離。具有四對孤對電子的O2分子(電子積累區)傾向于在缺電子位點(電子耗盡區)吸附。Na+和K+離子周圍的電子密度小于其他區域的電子密度,表明它們缺電子并具有路易斯酸性。因此,NaK-PHI中的Na+和K+比其他N原子位點更有可能與O2反應。O2與NaK-PHI的堿金屬離子位點之間表現出明顯的電荷密度堆積。吸附在NaK-PHI上的O2與Na+和K+位點有強烈相互作用,實現了有效的電子轉移。O2-TPD測試證明了NaK-PHI對O2的表面結合強度比PCN強。準原位XPS測試結果表明NaK-PHI上的Na+和K+離子容易捕獲光生電子,這有利于進一步的ORR。基于上述結果,進一步計算了PCN和NaK-PHI上ORR的自由能變化。PCN和NaK-PHI的反應位點分別是七嗪環的N原子和堿金屬離子。與PCN相比,Na和K活性位點的引入極大地促進了O2的吸附(從1.52 eV降低到-1.32 eV)。因此,通過降低O2吸附和活化的能壘,NaK-PHI表現出比PCN更高的ORR反應性。
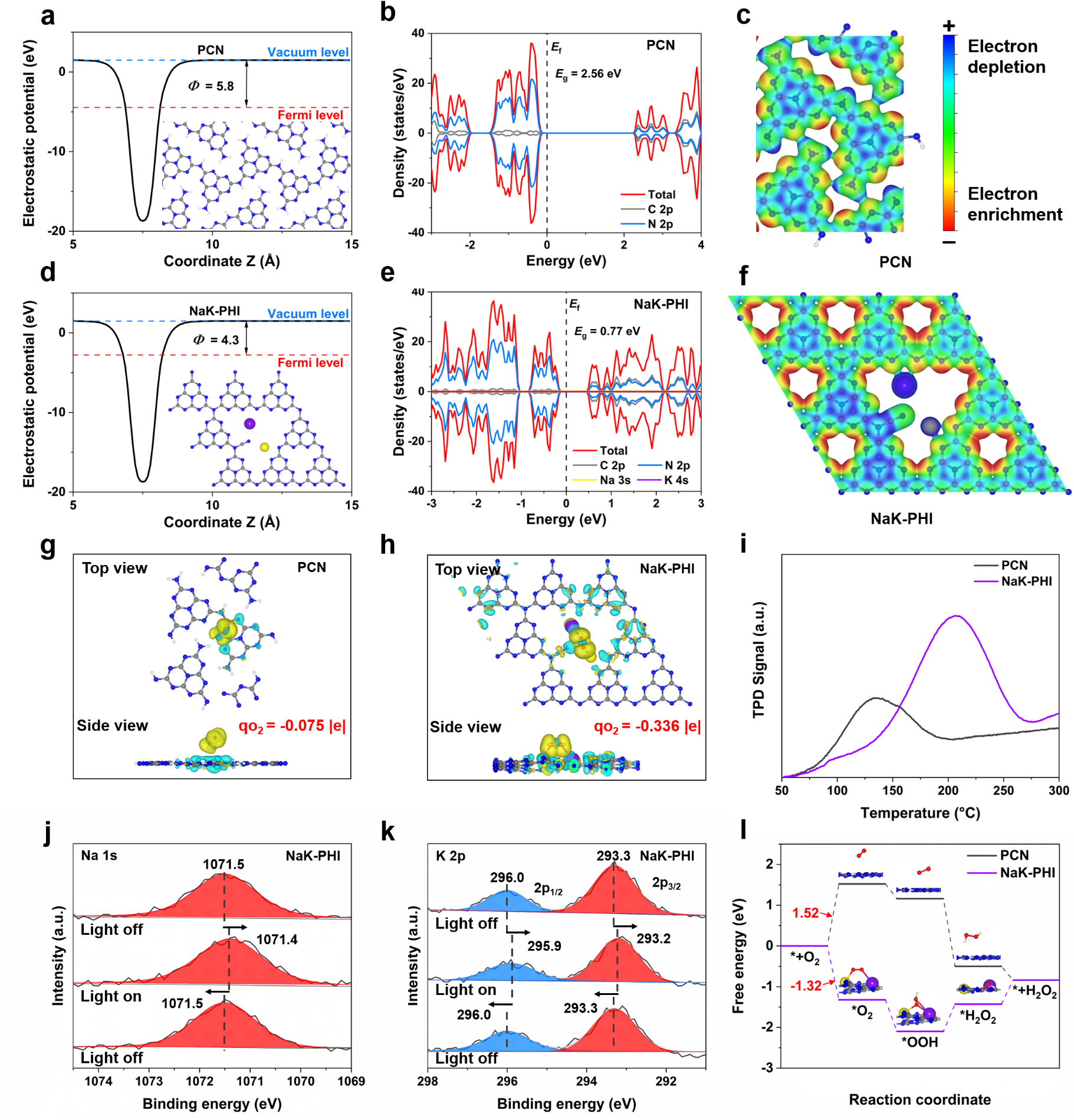
圖5. 堿金屬位點對合成H2O2的催化增強機制
我們建立了電子勢阱模型,以進一步了解M-PHI的光生電子儲存機制。當在PHI中引入Na+和K+時,PHI的電負性(δ?)增加,這增加了PHI的電子勢壘,并進一步延長了光生電子的壽命。NaK-PHI在350-430 nm處表現出最高的正SPV信號,表明分離電荷是最有效的。值得注意的是,Na-PHI、K-PHI和NaK-PHI在430-600 nm范圍內顯示負的SPV信號,表明PHI中積累了光生電子。TPV測試中NaK-PHI的SPV強度大于PCN,表明NaK-PHI的光生電荷分離效率更高。與PCN相比,NaK-PHI的TPV曲線衰減更慢、更平緩,表明電荷復合更慢。更重要的是,具有電子勢阱效應的NaK-PHI在TPV曲線上產生負信號區域。隨著時間的推移,“被捕獲”的光生電子緩慢穿過電子勢阱的能壘,與光生空穴復合,最終達到平衡。通過開爾文探針力顯微鏡(KPFM)和光電流測試可知NaK-PHI的內建電場強度比PCN高12.6倍,進一步闡明了催化劑中有效電荷分離和轉移的形成。

圖6. NaK-PHI的電子勢阱模型和其引起的內建電場
總結展望
用三元共晶鹽(LiCl/NaCl/KCl)合成了一種具有電子勢阱效應的光催化劑NaK-PHI。得益于電子勢阱效應,NaK-PHI中不均勻的電荷分布產生了強大的內建電場,促進了有效的電荷分離和轉移。電子勢阱效應模型有望在光催化和光電催化系統中有更多應用。
作者介紹
方瀟(第一作者),在讀博士生,師從丁勇教授。主要研究方向為氮化碳材料的設計合成及其在人工光合成過氧化氫的應用。以第一和共同第一作者身份發表Energy Environ. Sci., Nano Res., Sci. China Chem. Chem. Commun.等SCI論文5篇,主持中央高校優秀研究生創新項目和甘肅省研究生“創新之星”項目。

丁勇教授(通訊作者),博士生導師、飛天學者特聘教授、隴原人才B類計劃入選者,現任蘭州大學化學化工學院物理化學研究所所長。他于2004年12月在中國科學院蘭州化學物理研究所獲得博士學位后入職蘭州大學化學化工學院,2009年12月至2011年1月赴美國埃默里大學化學系開展訪問學者研究工作,并于2011年5月獲聘教授。SCI一區雜志Chinese Journal of Catalysis和Chinese Chemical Letters編委,清華大學出版社雜志Polyoxometalates編委。兼任中國科學院蘭州化學物理研究所“羰基合成與選擇氧化國家重點實驗室”客座研究員。其科研工作聚焦于能源與環境催化領域,在國內外各種學術會議上做了70多場主題和邀請報告。至今作為第一或者通訊作者已在Angew. Chem. Int. Ed, Energy Environ. Sci., Adv. Funct. Mater., ACS Energy Lett., ACS Catal., Appl. Catal.B.-Environ., Sci. China Chem.等SCI學術刊物上發表研究論文近180篇,獲得授權專利多項。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn