


研究背景
異雜Diels–Alder(HDA)反應是一種高效構建六元雜環結構的經典手段,廣泛應用于活性天然產物的合成。盡管HDA反應在化學合成中已有成熟應用,但自然界中僅有少數能夠催化HDA反應的酶,且僅限于單一雜原子的反應體系。
自然界中存在一類具有氧橋三環縮醛結構的天然產物,具有多種生物活性,但其生物合成機制仍不清楚。受到化學合成中以鄰醌亞甲基(o-QM)與羰基發生[4?+?2]環加成生成氧橋三環結構的啟發,研究者推測自然界中可能存在能催化雙氧雜DA反應(dual-oxa DA)的酶。以(?)-ABX為代表的這類化合物,通過化學合成產物為外消旋體且產率不高,探索其天然生物合成機制具有重要意義。
研究內容
研究人員此前已確定了(-)-ABX 的芳香骨架 PDA 相關的生物合成基因簇,但其核心結構氧橋三環縮醛的酶促形成機制仍未明確。通過實驗研究人員推測,前體 1 先被 Abx(?)E 立體專一性還原為 (8S)-2,然后通過 Abx(?)F 的催化高效且專一地轉化為 (-)-ABX,若無 Abx(?)F 則會緩慢自發生成 (+)-ABX 和 (?)-ABX 的混合物。本研究通過實驗和理論計算系統揭示了天然產物 (?)-ABX 中獨特的氧橋三環縮醛結構的形成機制。
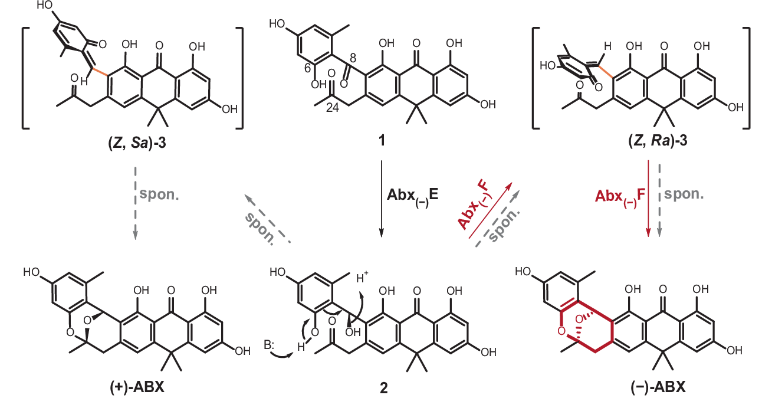
圖1(-)-ABX形成氧橋三環縮醛的關鍵步驟。
研究發現,氧橋三環縮醛結構并非通過傳統的脫水環化或SN1、SN2機制生成,因為這些路徑無法解釋最終產物的手性構型,也不符合同位素實驗的結果。本研究提出并驗證了一種全新機制:Abx(?)E 催化前體化合物1還原為中間體2;隨后,在 Abx(?)F 的催化下,2脫水生成具有軸手性的 o-QM中間體3,再通過高選擇性的dual-oxa DA反應形成 (?)-ABX 的三環結構。
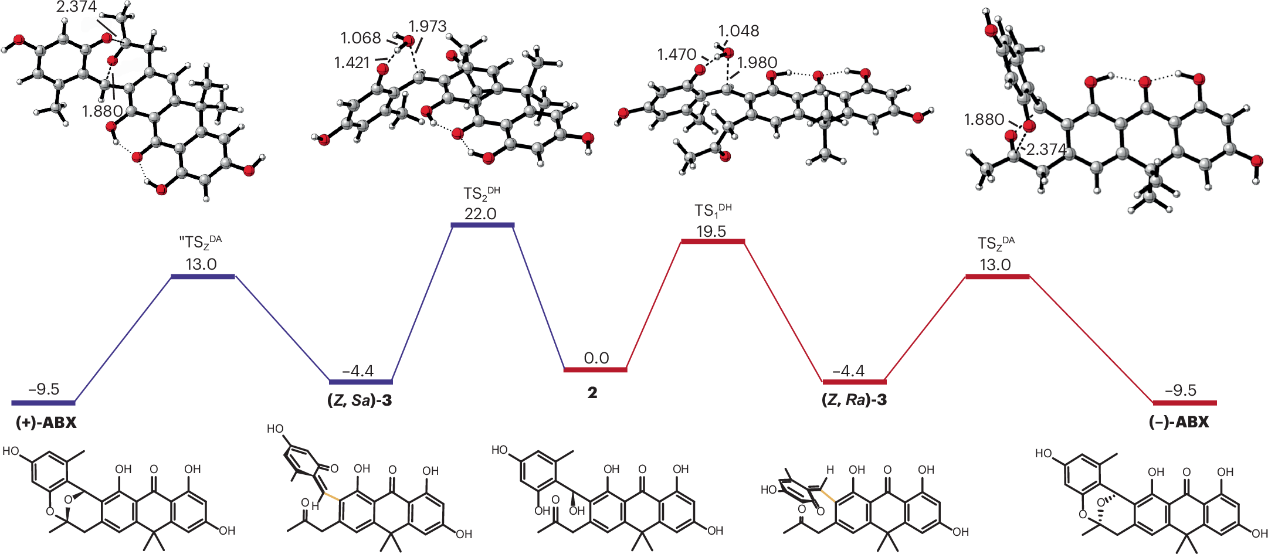
圖22到(?)-ABX的勢能面
為了驗證上述提出的機制,進行了DFT 計算。在非酶環境中,8-OH的消除可以通過鄰位酚(6-OH)基團的質子供給來促進。由于新形成的C7=C8雙鍵會產生軸手性,中間體3可能存在兩種過渡態,TS1DH和TS2DH(圖2和圖3a,b)。計算分析表明,脫水反應發生在化學過程的較晚階段,此時6-OH的質子轉移幾乎完成,因此鄰位位置會積累顯著的負電荷。這使得在TS1DH中蒽酰羥基呈反式取向相比于TS2DH中的順式取向更加有利,能量差約為2.5 kcal/mol(圖2和圖3a,b)。這意味著將主要生成(Ra)-3。進一步的8-OH脫水被計算為放能反應,能量釋放為4.4 kcal/mol,這主要歸因于一個分子分解為兩個分子所帶來的熵增益。對于oxa-DA反應,中間體3中的o-QM基團和24位羰基(C24=O)可能有四種合理的取向(圖3c),這取決于C7=C8雙鍵的E/Z構型以及C24取代基的exo/endo取向。然而,由于C9和C22之間的芳香鍵連接,實際上只有兩種取向能夠成為可行的過渡態,即TSEDA和TSZDA(圖3 d, e)。這兩種過渡態分別會生成(R-C8, S-C24)、(S-C8, R-C24)和(R-C8, R-C24)、(S-C8, S-C24)的DA加成產物。雖然這兩種過渡態在幾何上均可行,但TSEDA在能量上無法達到,其能量比TSZDA高出38.0 kcal/mol(圖3e)。因此,只有TSZDA的加成產物可以生成,即(?)-ABX (R-C8, R-C24)和(+)-ABX (S-C8, S-C24),這一結果與實驗結果一致。
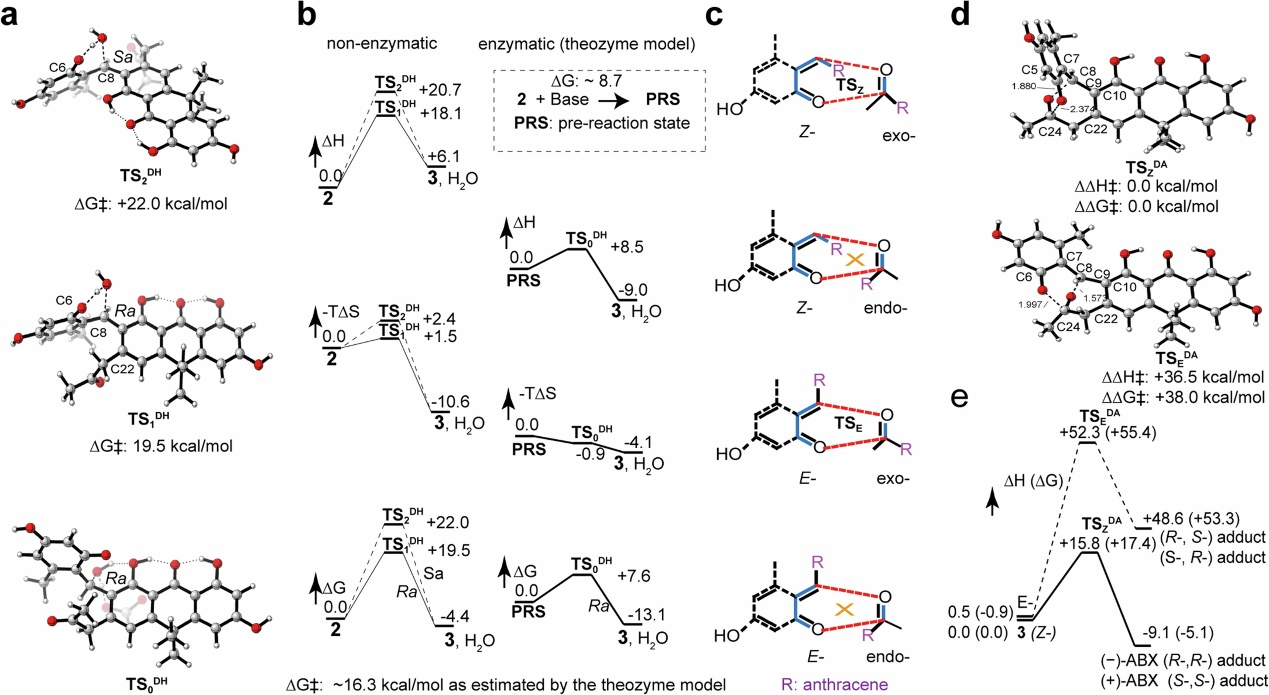
圖3QM計算支持并解釋了Abx(-)F的立體特異性dual-oxa DA環化反應
隨后,為了理解中間體3在Abx(?)F的存在下如何專一性地發生oxa DA反應,我們利用理論酶模型探討了Abx(?)F可能的反應機制。假設酶促脫水與非酶促脫水的內在反應能量相同,根據理論酶模型,形成預反應態(PRS)大約需要8.7 kcal/mol的能量(圖3a,b)。結合過渡態TS0DH的能量信息,模型預測酶促反應的整體能壘不會超過16.3 kcal/mol,比非酶促反應低3.2 kcal/mol,這相當于在Abx(?)F存在下反應速率提升了約226.7倍。
為了深入了解Abx(?)F的催化機制,本研究確定了該酶的晶體結構,并通過NMR分析確定了Abx(?)F的結合位點。進一步研究表明,(?)-ABX通過π–π堆積作用與Abx(?)F的特定區域結合,關鍵的氨基酸殘基通過穩定底物構象,促進脫水和雙氧-DA反應。此外,芳香環的構象發生重要變化,旋轉約90°,使6-OH基團形成關鍵氫鍵,這一過程通過分子動力學模擬得到驗證。通過突變Abx(?)F的關鍵殘基,確認D17在脫水反應中至關重要,可能作為通用堿促進6-OH去質子化并促進8-OH的離去。W15、Y48、Y78和S60與立體控制相關,因為它們在oxa DA反應中影響(+)-ABX的生成。
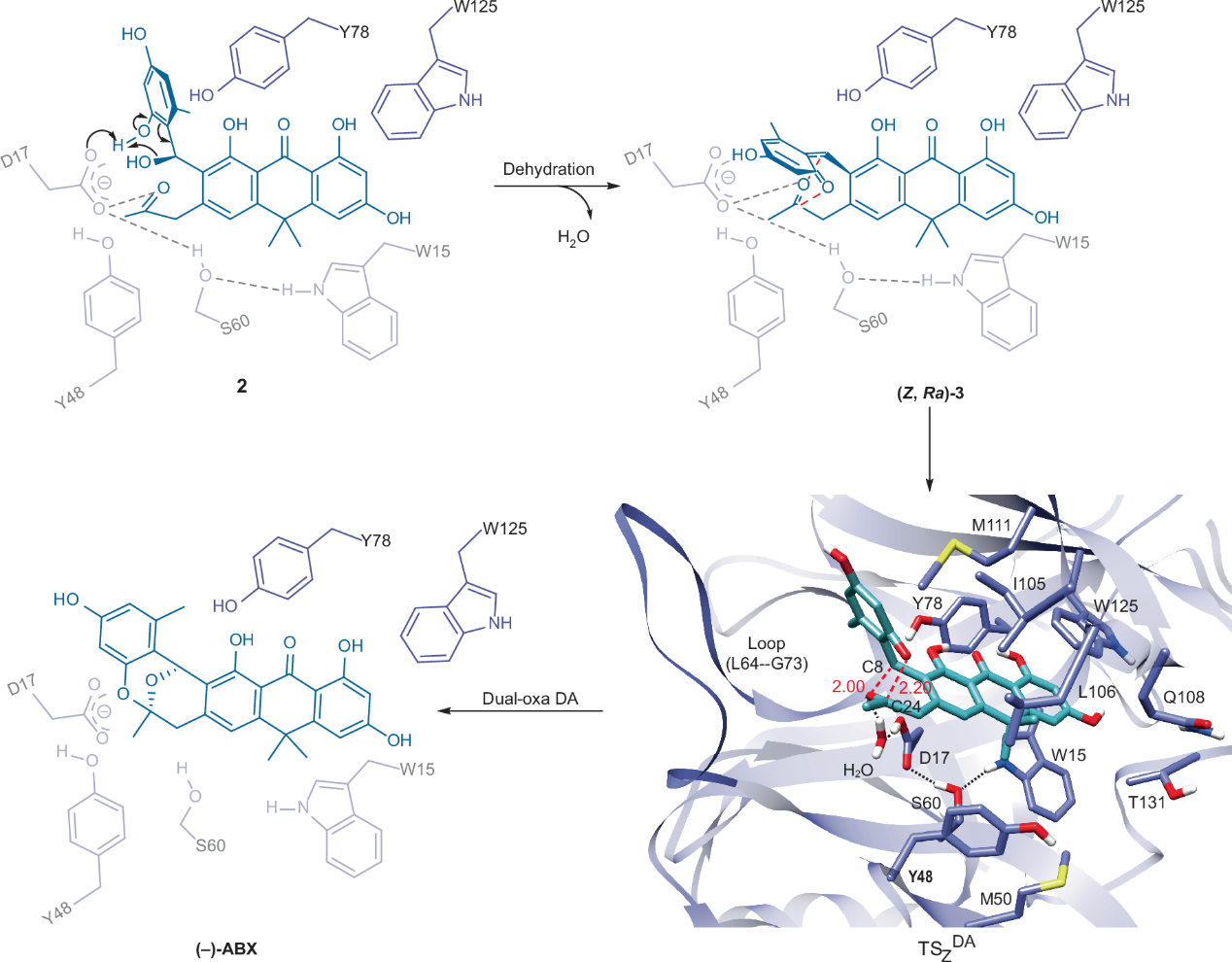
圖4 ONIOM計算Abx(-)F中的催化機理
為了進一步揭示Abx(-)F在oxa DA反應中的作用,使用ONIOM方法模擬了蛋白質中的過渡態TSZDA(圖4)。計算得出Abx(-)F中的反應勢壘為 9.6 kcal mol-1,遠低于水溶液中估計的 17.4 kcal mol-1(圖2),證實了Abx(-)F作為DA酶的作用。D17羧基的羥基通過橋接水分子與C24羧基形成氫鍵,從而降低了親二烯的電荷密度,使DA反應更加有利。W15和S60與D17形成了一個擴展的氫鍵網絡,從而提高了酶-底物復合物的幾何穩定性。此外,兩個β片上的相鄰殘基(包括 W125、I105、Y48、Y78、Q108、T131、M50、L106和M111)產生了模板效應,將TSZDA的蒽基基團緊密地固定在DA 反應中。然后,L64-G73環的動態運動為在DA反應中翻轉苯環提供了必要的空間。
通過整合實驗和計算數據,本研究提出了Abx(-)F催化的oxa DA反應的兩步機制。S60側鏈首先與D17形成氫鍵,以增強羧基的堿性,而羧基則作為一般堿基使化合物2的酚基6-OH去質子化。去質子化會引發分子內部的重排,包括新生苯氧基陰離子的電子遷移以及8-OH的質子化和脫水,從而形成能量有利的(Z,Ra)-3。最后,在Abx(-)F底物結合袋的限制下,(Z, Ra)-3采用一種特定的受限構象(TSZDA),發生oxa DA反應,生成(-)-ABX。
總結
(1)實驗首次發現并鑒定了一種可催化雙氧雜狄爾斯–阿爾德(dual-oxa DA)反應的天然酶Abx(?)F,該酶來自一種類鄰位氧螯合(VOC)蛋白家族,具備雙功能催化活性,既能催化底物脫水,又能立體選擇性地促使[4+2]環加成反應,成功構建了(-)-anthrabenzoxocinone((-)-ABX)中的氧橋三環縮醛結構。這是首次報道自然界中存在可催化含兩個氧雜原子的多雜原子DA反應的酶,突破了此前僅能處理單一雜原子DA反應的局限。
(2)實驗通過晶體結構解析、核磁共振(NMR)復合物結構分析、同位素標記實驗及密度泛函理論(DFT)計算,深入揭示了Abx(?)F催化反應的分子機制。研究發現,該酶通過Asp17殘基作為一般堿,啟動底物脫水生成o-苯醌甲基(o-QM)中間體,進而誘導雙氧雜DA反應的發生。
(3)結構分析明確了酶與底物及產物的結合方式,為其立體選擇性提供了結構基礎。該研究不僅驗證了酶催化復雜多雜原子環加成反應的可行性,也預示了自然界中或許還存在其他類似的多雜原子DA酶,為今后的酶工程和天然產物合成提供了新思路和工具。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn