



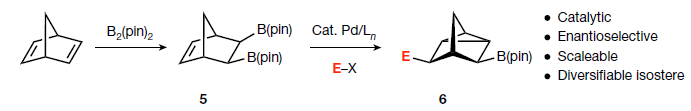
正文
雖然芳香環(huán)是藥物活性化合物中的常見(jiàn)組成部分,但這些骨架的存在給藥物的可開(kāi)發(fā)性帶來(lái)了一些不利因素。用非芳香族等排體結(jié)構(gòu)來(lái)替代芳香族結(jié)構(gòu)可以有效改善藥物的非最佳效能、代謝穩(wěn)定性、溶解度和親脂性。此外,由于芳香環(huán)是平面的且缺乏三維性,而大多數(shù)藥物靶點(diǎn)的結(jié)合位點(diǎn)是手性的。因此,所替換的電子等排體的立體化學(xué)構(gòu)型可以提供一個(gè)額外的機(jī)會(huì),來(lái)提高衍生配體對(duì)靶受體的親和力。這種方法的一個(gè)顯著不足是缺乏從簡(jiǎn)單易得的前體,利用簡(jiǎn)單和可規(guī)模化的催化手段來(lái)對(duì)映選擇性的合成候選電子等排體。最近,美國(guó)波士頓學(xué)院(Boston College)Eranthie Weerapana與James P. Morken課題組和美國(guó)斯坦福大學(xué)(Stanford University)James K. Chen聯(lián)合報(bào)道了新穎的鈀催化策略,將烴類(lèi)衍生的前體轉(zhuǎn)化為手性含硼nortricyclanes。且將nortricyclanes引入到藥物分子骨架中可以有效改善其生物物理性質(zhì)和活性(Fig. 1)。化學(xué)加——科學(xué)家創(chuàng)業(yè)合伙人,歡迎下載化學(xué)加APP關(guān)注。
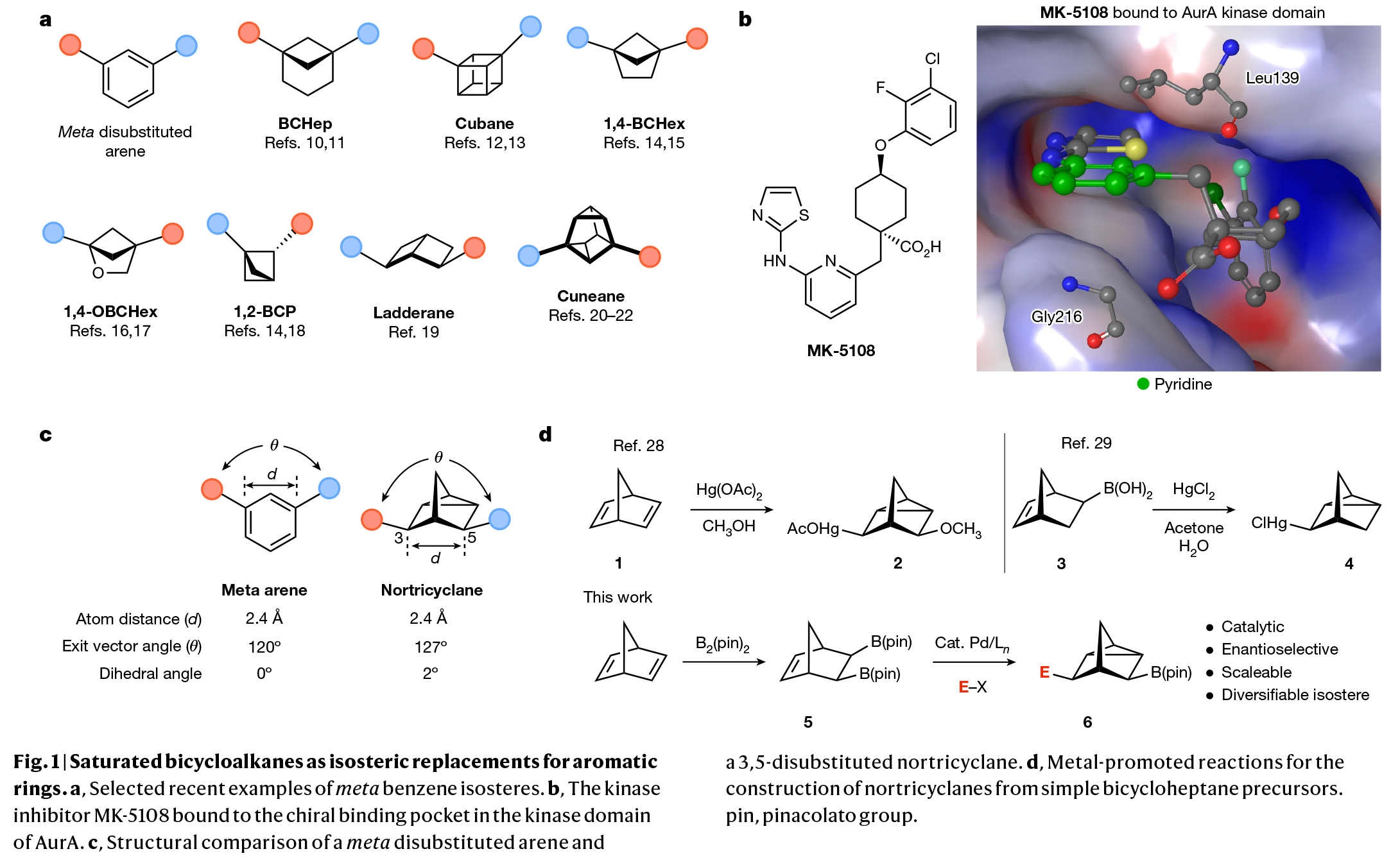
(圖片來(lái)源:Nature)
首先,作者以雙硼底物5為模板底物進(jìn)行了條件篩選。實(shí)驗(yàn)結(jié)果表明,當(dāng)使用5(1.0 equiv),溴苯(1.5 equiv),Pd(OAc)2(2 mol%),(S,S)-L1(3 mol%),Na2CO3(1.5 equiv),在THF/H2O中反應(yīng),可以以97%的產(chǎn)率,97:3 dr得到產(chǎn)物9。在得到了最優(yōu)反應(yīng)條件后,作者對(duì)此轉(zhuǎn)化的底物范圍進(jìn)行了考察(Fig. 2a)。實(shí)驗(yàn)結(jié)果表明簡(jiǎn)單取代的芳基溴均可順利參與轉(zhuǎn)化,以良好的產(chǎn)率(56-97%)和對(duì)映選擇性得到相應(yīng)的產(chǎn)物。其中缺電子親電試劑(11,12)和富電子親電試劑(13,15)均可順利實(shí)現(xiàn)轉(zhuǎn)化,但強(qiáng)吸電子的硝基芳烴親電試劑(16)產(chǎn)率有所降低。此外,雜環(huán)親電試劑同樣可以參與反應(yīng),以77-94%的產(chǎn)率得到產(chǎn)物20-23。值得一提的是,未保護(hù)的苯胺和酚似乎不會(huì)干擾該過(guò)程,并且將其擴(kuò)展到非芳香族親電試劑(24, 25)也可實(shí)現(xiàn)轉(zhuǎn)化。
為了證明此轉(zhuǎn)化的實(shí)用性,作者進(jìn)行了克級(jí)規(guī)模合成(Fig. 2b)和產(chǎn)物的合成轉(zhuǎn)化(Fig. 2c)。首先,5可以直接利用廉價(jià)的市售降冰片二烯和B2(pin)2在多克(7.3 g)規(guī)模上制備。而5的反應(yīng)可以在5.0 mmol的規(guī)模上進(jìn)行,只要將反應(yīng)時(shí)間延長(zhǎng)至24 h,鈀的用量?jī)H為0.5 mol%,就可以92%的收率得到產(chǎn)物。此外,產(chǎn)物7中的硼酯可以通過(guò)鋅催化的交叉偶聯(lián)(26, 92%)、銅催化烯丙基化和羧化(27, 90%和28, 87%)、直接胺化(29, 57%)、同系化(30, 94%)或轉(zhuǎn)化為醇(31, 98%)。
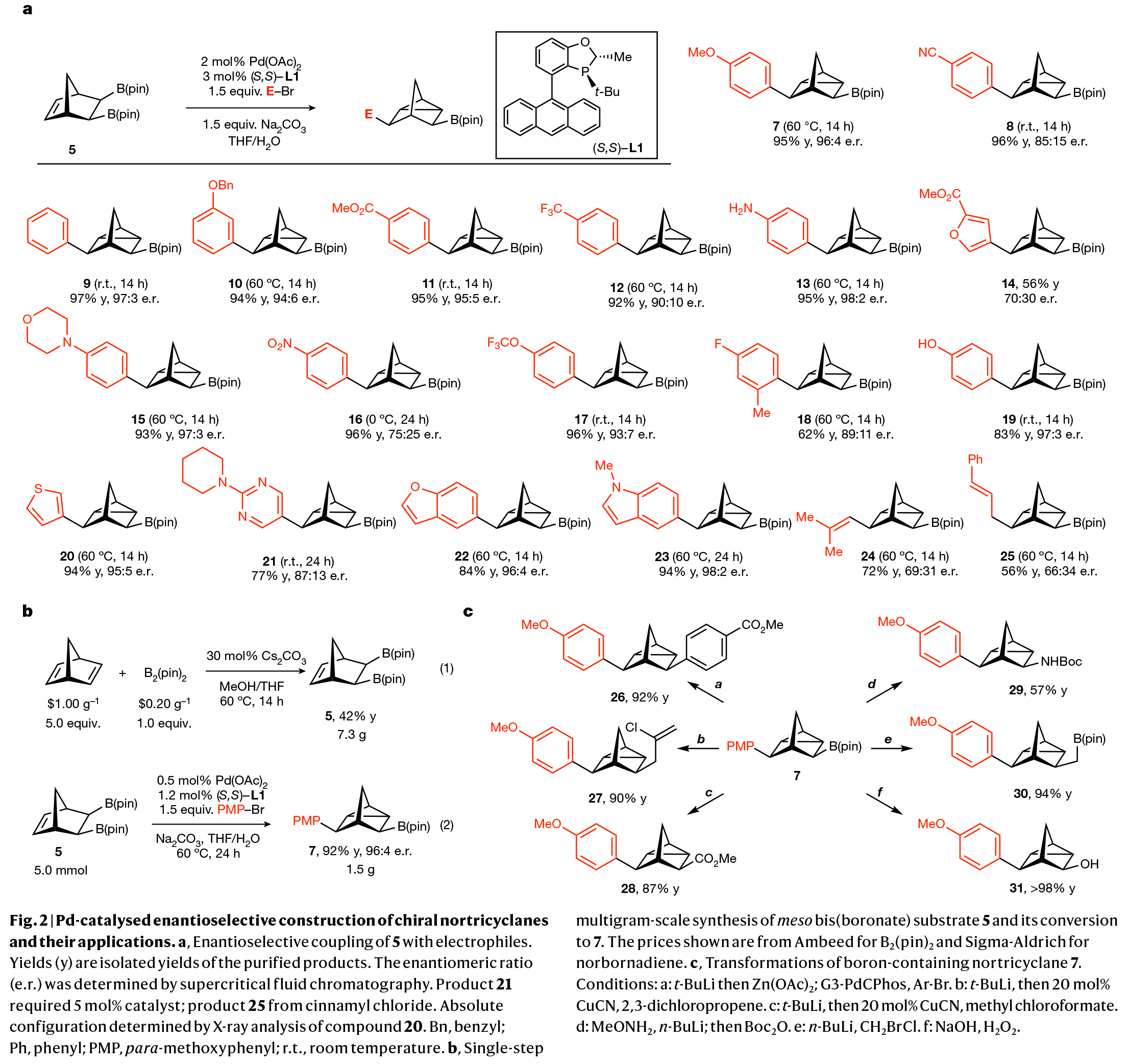
(圖片來(lái)源:Nature)
機(jī)理研究提供了一種可能的途徑,可以從底物衍生的環(huán)酸鹽絡(luò)合物32中得到產(chǎn)物(Fig. 3a),此類(lèi)化合物在作者先前的研究中有過(guò)報(bào)道(J. Am. Chem. Soc. 2022, 144, 17815)。作者利用DFT計(jì)算確定了鈀-烯烴絡(luò)合物(GS0)反應(yīng)路徑的自由能分布,該絡(luò)合物是由LPd(0)與親電試劑發(fā)生氧化加成,隨后與32結(jié)合得到的。在一種途徑(路徑A,紅色)中,烯烴(TS1a)的碳鈀化得到Pd(II)中間體GS1a,隨后GS1a可能會(huì)被TS2a置換Pd(II),其中有機(jī)硼作為親核試劑同時(shí)釋放和還原金屬。另一種途徑中(路徑B,藍(lán)色),在與Pd(II)結(jié)合時(shí),烯烴可能具有足夠的親電性經(jīng)歷與TS1b的親核鈀化得到GS1b,隨后經(jīng)歷直接的還原消除得到產(chǎn)物。計(jì)算結(jié)果表明,碳鈀化途徑的能量較低,且與親核鈀化步驟相比,烯烴遷移插入產(chǎn)生GS1a的能壘要低得多(0.7 kcal mol-1和18.7 kcal mol-1)。在GS1a中,溴的解離使得TS2a在19.4 kcal mol?1的能壘下發(fā)生Pd(II)的閉環(huán)還原取代(Fig. 3c)。值得注意的是,TS1a產(chǎn)生的13C動(dòng)力學(xué)同位素效應(yīng)的計(jì)算結(jié)果與實(shí)驗(yàn)確定的結(jié)果相吻合(Fig. 3b)。值得注意的是,鈀催化5的偶聯(lián)在C2處顯示出可忽略不計(jì)的KIE,這與基于碳鈀化的機(jī)理一致,與親核鈀化途徑不一致。根據(jù)這些實(shí)驗(yàn),作者得出碳鈀化步驟是對(duì)映選擇性的決定步驟(Fig. 3d)。
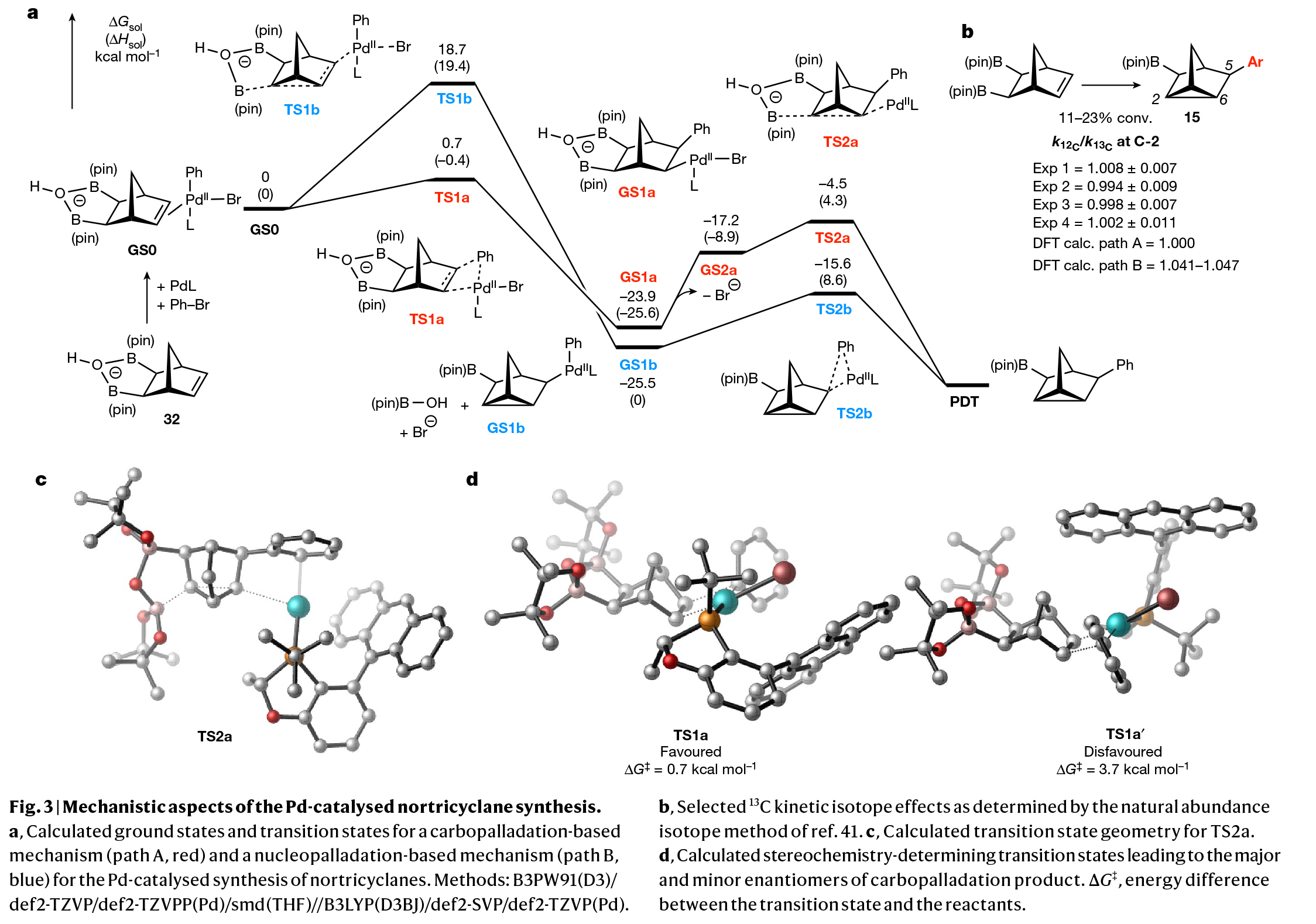
(圖片來(lái)源:Nature)
為了確定nortricyclanes骨架是否適合用于生物活性分子,作者利用33的兩個(gè)對(duì)映體分別制備了脂肪酸酰胺水解酶(FAAH)抑制劑URB597的手性電子等排體類(lèi)似物,并對(duì)其進(jìn)行分析(Fig. 4)。值得注意的是,雖然獲得的電子等排體類(lèi)似物的分子量與URB597相似,但它們?cè)谒彌_液中的溶解度提高了10倍,同時(shí)保持了相當(dāng)?shù)挠H脂性(α log D)。除此之外,通過(guò)小鼠肝微粒體測(cè)定,電子等排體類(lèi)似物相對(duì)于URB597表現(xiàn)出明顯增加的代謝穩(wěn)定性。接下來(lái),作者通過(guò)定量活性的蛋白質(zhì)譜實(shí)驗(yàn)比較了化合物(R,S)-33和(S,R)-33。雖然實(shí)驗(yàn)結(jié)果表明(R,S)-33和(S,R)-33的抑制作用不如URB597,但這兩種電子等排體類(lèi)似物仍然具有抑制FAAH的能力,并且表現(xiàn)出不同的抑制作用。
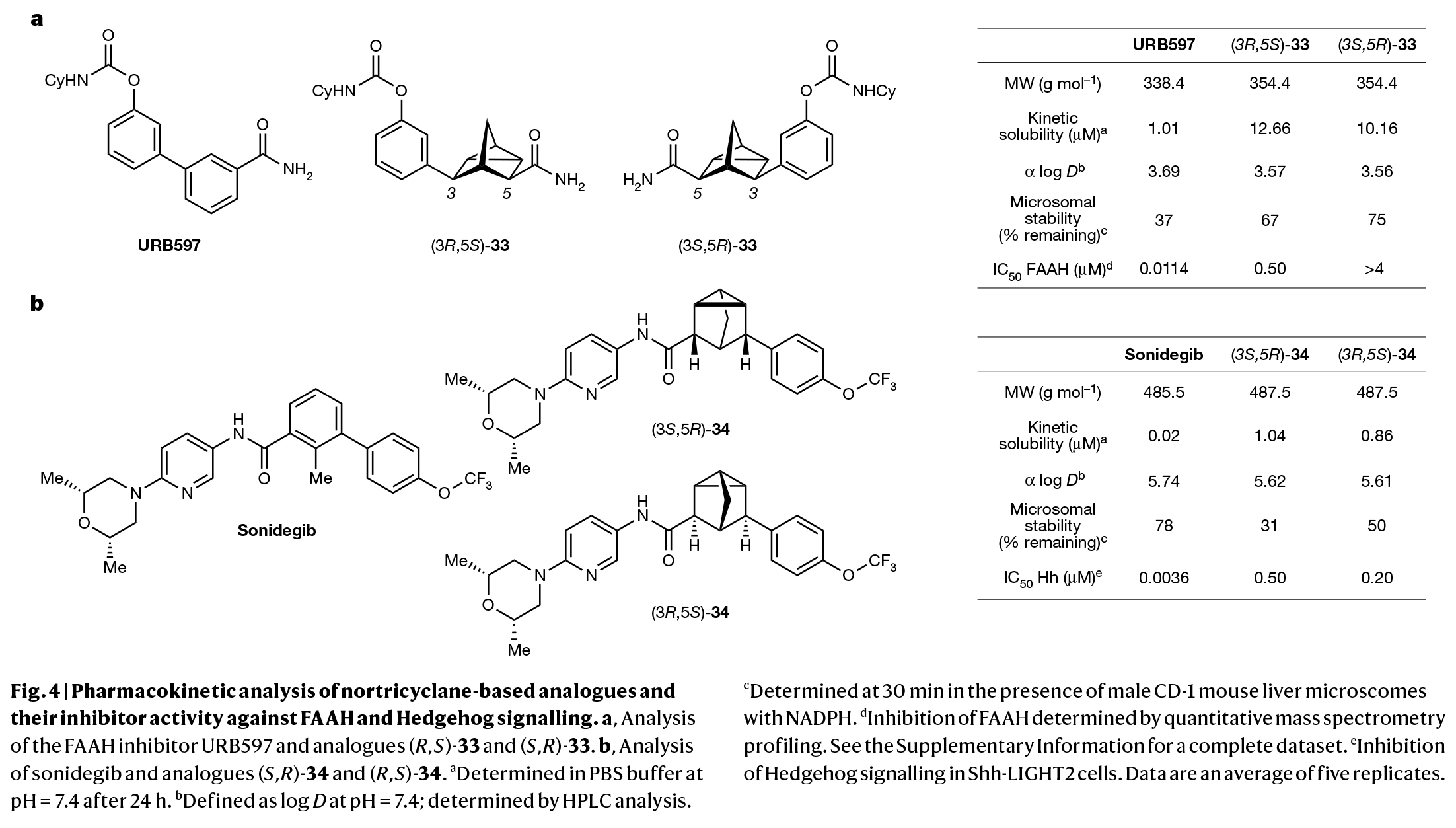
(圖片來(lái)源:Nature)
總結(jié)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn