

(圖片來源:J. Am. Chem. Soc.)
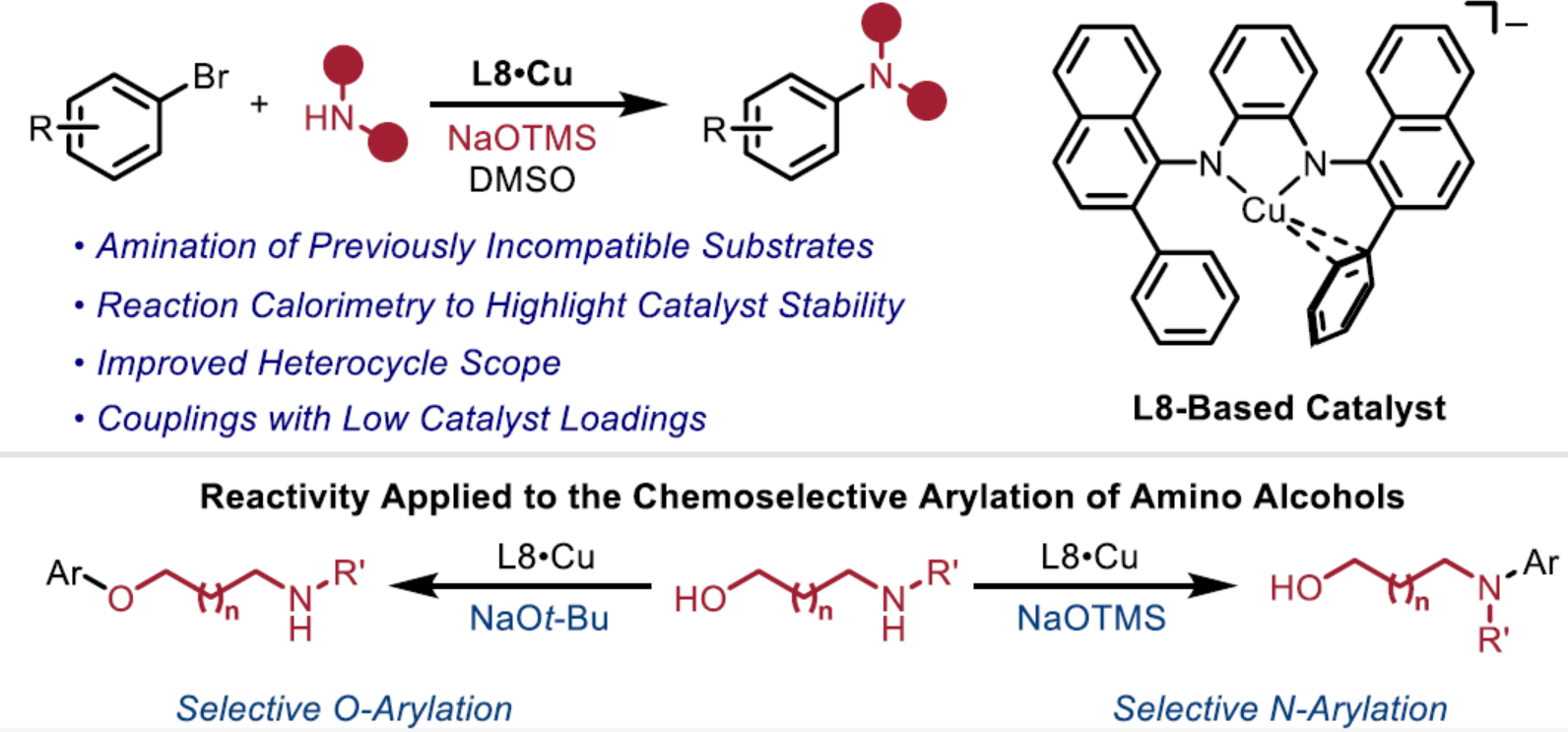
正文
(圖片來源:J. Am. Chem. Soc.)
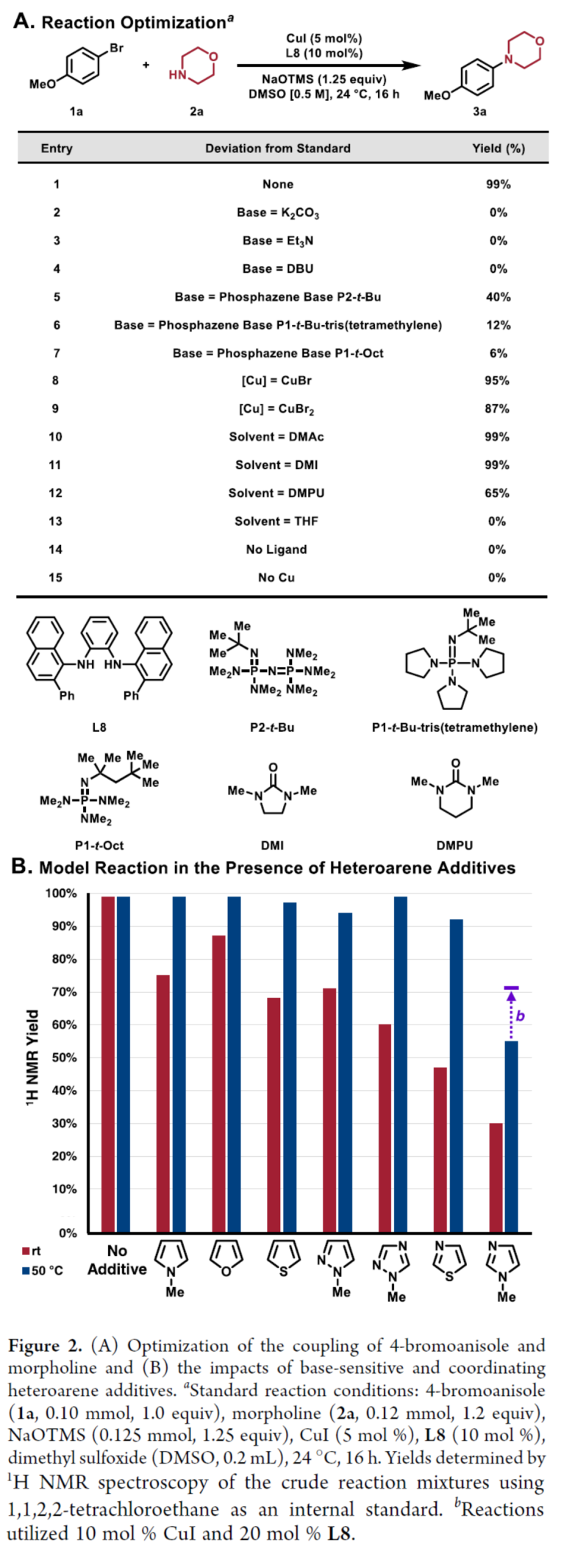
首先,作者以4-溴苯甲醚1a與嗎啉2a作為模型底物,進行了相關偶聯反應條件的篩選(Figure 2A)。當以CuI(5 mol %)作為催化劑,L8(10 mol %)作為配體,NaOTMS(1.25 equiv)作為堿,在DMSO溶劑中24 oC反應16 h,可以99%的收率得到N-芳基胺產物3a。同時,在1a與2a的標準反應體系中加入不同的五元雜芳烴添加劑的實驗結果表明,衍生自L8的催化劑阻止了由配位誘導配體置換引起的失活,并且五元雜芳基溴化物可能在50 oC進行反應(Figure 2B)。
(圖片來源:J. Am. Chem. Soc.)
在獲得上述最佳反應條件后,作者對底物范圍進行了擴展(Scheme 1)。首先,含有酰胺(1a和1e)、可烯醇化酮(1b和1d)、叔丁基酯(1g)和羧酸(1h)取代的芳烴,均可與一級或二級胺偶聯,可以良好至優異的產率得到相應的產物。堿敏感胺,也以良好至優異的產率得到相應的N-芳基胺1c和1f。三種α-三級胺,也是合適的底物,可以中等至良好的產率得到相應的產物1i、1j和1t。其次,一系列五元雜芳基鹵化物和苯稠合雜芳烴,均可順利進行反應,可以良好至優異的產率得到相應的產物1k-1t。此外,該策略還可用于一些藥物和天然產物的后期衍生化,可以良好至優異的產率得到相應的產物1u-1x。雖然R3Si-基保護基在反應條件下是不穩定的,但THP-保護的苯酚可以良好的產率進行胺化(1y)。除了N-雜環烷基化(1z)外,SEM基團的N-保護也具有良好的產率(1aa)。N-Boc和N-甲苯磺酰基在反應條件下是不穩定的,導致脫保護和催化劑抑制。由于分解,含醛的芳基溴化物與胺化方案不相容。然而,使用溴化二乙縮醛進行C?N偶聯,然后用2M HCl原位脫保護,可以兩步優異的產率得到含醛的N-芳基胺產物1ab。

(圖片來源:J. Am. Chem. Soc.)
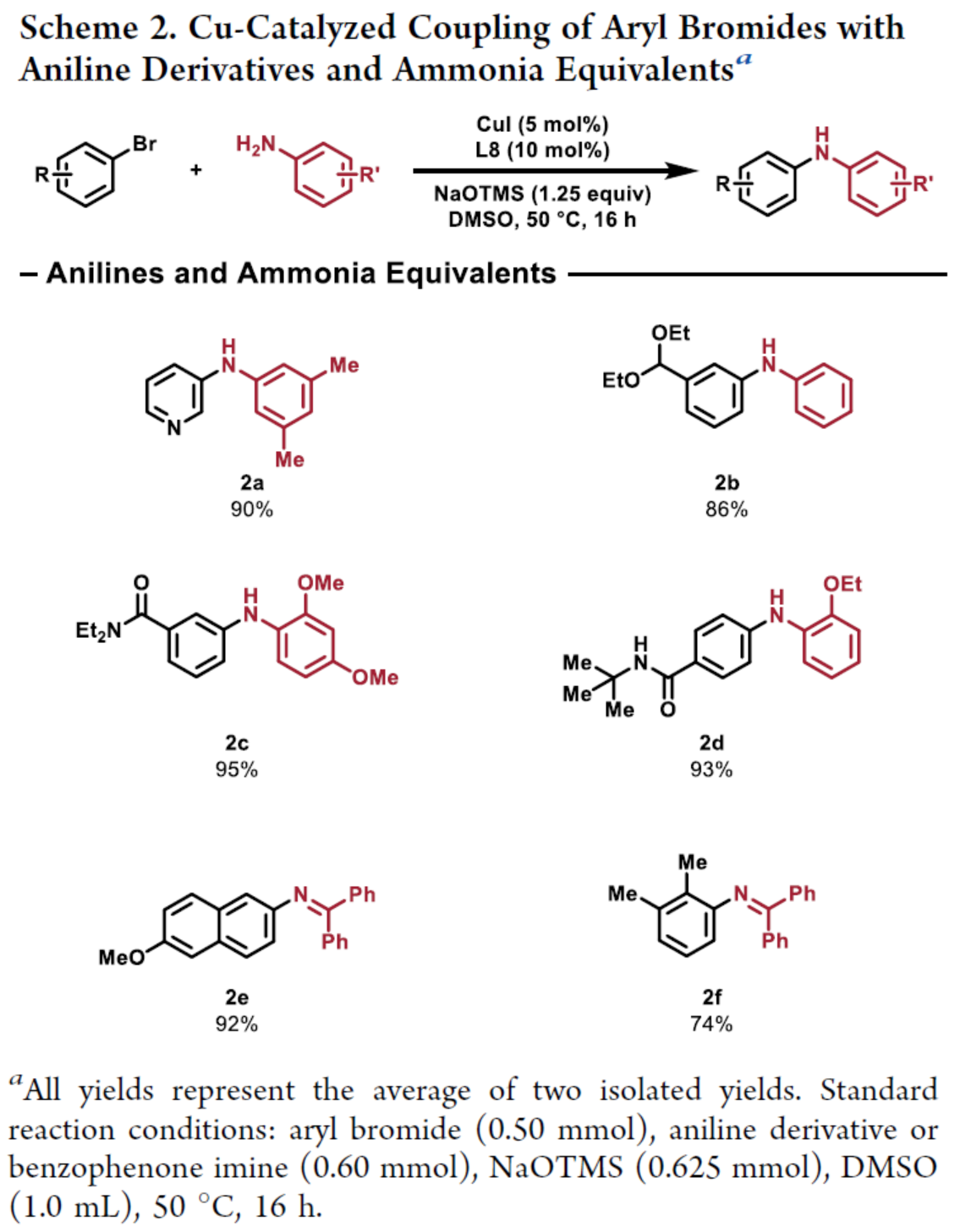
其次,作者進一步對親核試劑的底物范圍進行了擴展(Scheme 2)。研究結果表明,一系列苯胺衍生物與二苯甲酮亞胺,均可順利進行反應,獲得相應的產物2a-2f,收率為74-93%。
(圖片來源:J. Am. Chem. Soc.)
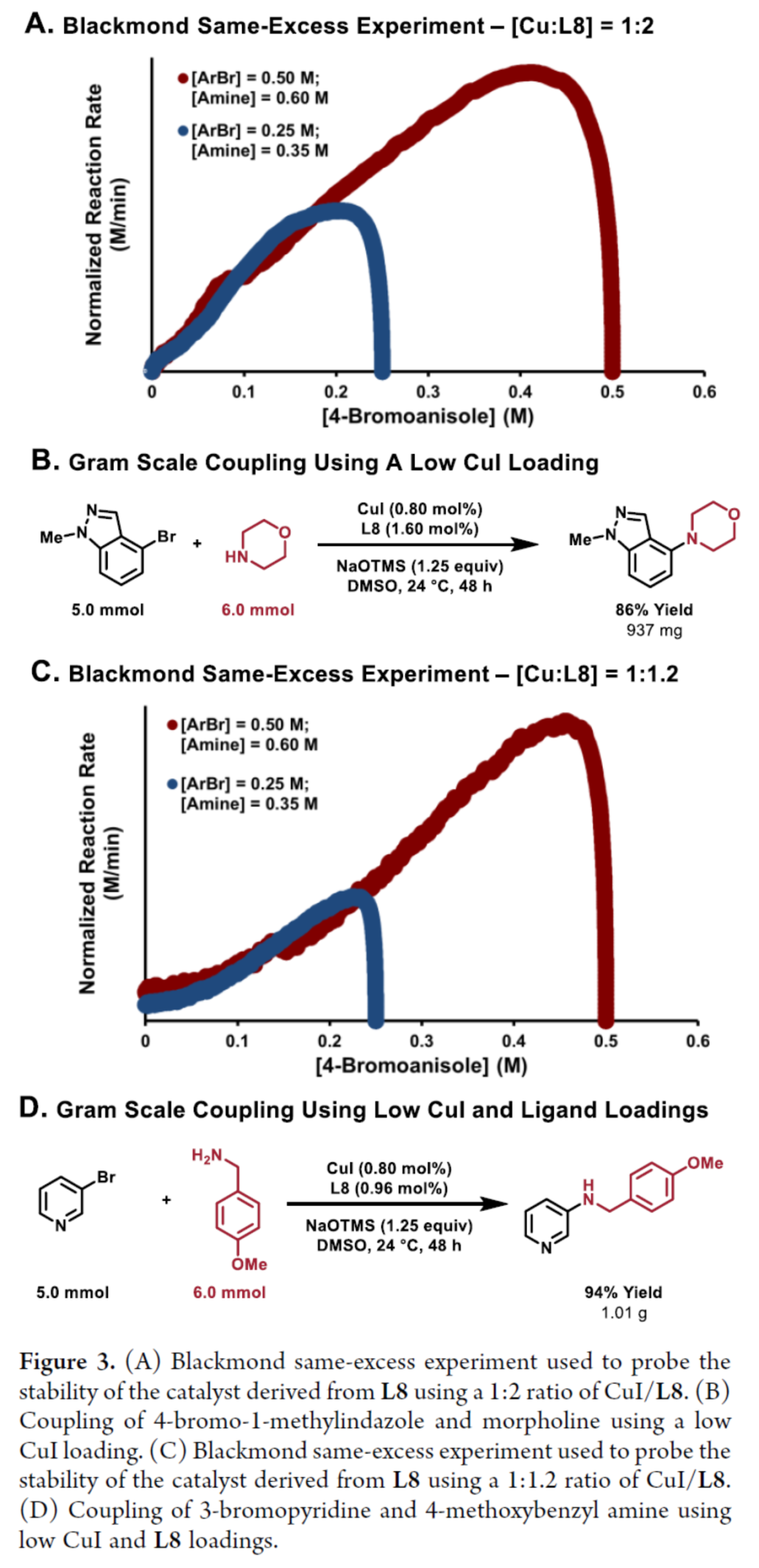
緊接著,作者對衍生自L8的催化劑的穩定性以及反應的實用性進行了研究(Figure 3)。研究結果表明,衍生自L8的銅催化劑在整個反應過程中是非常穩定的,并且可以使用較低的催化劑負載量。
(圖片來源:J. Am. Chem. Soc.)
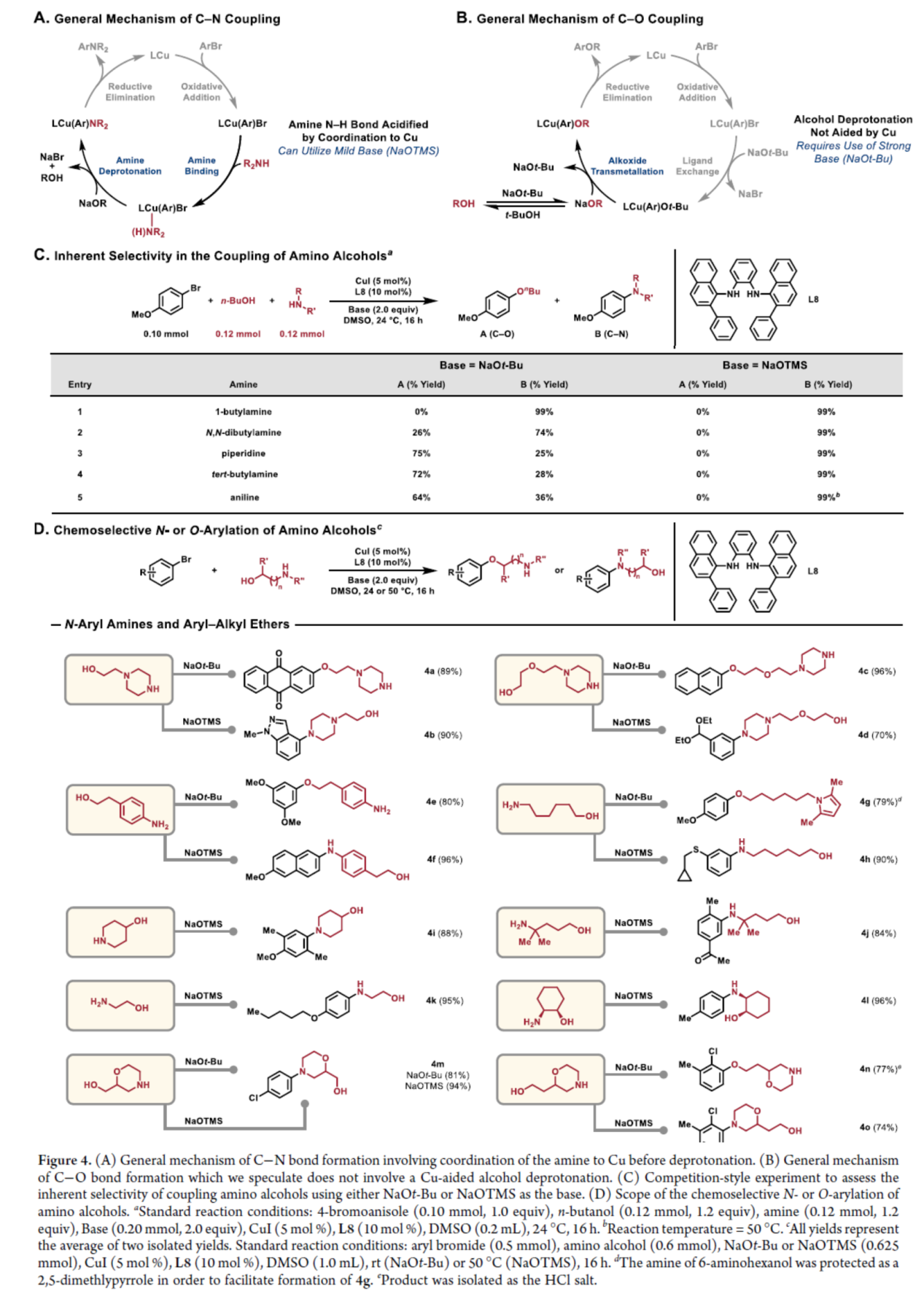
最后,作者提出了合理C-N和C-O偶聯的催化循環過程(Figure 4A與Figure 4B)。其中,C?N鍵形成的一般機理涉及去質子化前胺和銅的配位(Figure 4A),而C?O鍵形成的一般機理不涉及銅輔助的醇去質子化(Figure 4B)。基于上述的機理,作者發現,當使用不同的堿時,可進行化學選擇性N-和O-芳基化反應(Figure 4C)。研究結果表明,當氨基醇具有一級醇和位阻大的胺或苯胺基團時,使用NaOt-Bu作為堿時,僅進行C?O偶聯反應,獲得相應的產物4a、4c、4e、4g、4m和4n,收率為77-96%。當使用NaOTMS作為堿時,無論氨基醇的結構如何,僅能進行C?N偶聯反應,獲得相應的產物4b、4d、4f、4h-4m和4o,收率為70-96%。(Figure 4D)。
(圖片來源:J. Am. Chem. Soc.)
總結
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn