

合成化學為我們的“衣、食、住、行、醫”提供了重要的物質基礎,是推動人類社會進步的重要驅動力。然而傳統的化學合成存在效率低、污染嚴重等瓶頸問題,與國家所倡導的綠色發展理念相矛盾。因此更加綠色、高效的合成方法亟待開發。相較于傳統的化學催化,酶催化具有過程綠色、選擇性好、催化效率高等優勢,在功能分子例如創新藥物的工業化生產中得到了廣泛的應用,已成為傳統化學合成方法的重要替代者。然而,目前酶催化反應的工具箱還非常有限,能夠催化新穎化學轉化的酶亟待發現。
狄爾斯-阿爾德反應(Diels-Alder reaction,簡稱D-A反應)是共軛雙烯(二烯體)與取代烯烴(親二烯體)之間發生的[4+2]環加成反應,最早由德國化學家Otto Diels和他的學生Kurt Alder在1928年首次報道。D-A反應是合成化學中構建C-C鍵最常用的方法之一,在天然產物全合成、藥物分子工業化生產以及材料化學等方面得到了廣泛的應用,這兩位德國化學家也因為這些貢獻而獲得了1950年的諾貝爾化學獎。值得一提的是,2021年諾貝爾化學獎得主之一David W.C. MacMillan所開發的有機小分子催化的第一個實例也是D-A反應。
傳統化學催化的D-A反應存在著立體選擇性差、合成效率低等問題,因此從自然界中挖掘可以立體選擇性催化D-A反應的酶受到了化學家們的廣泛關注和研究。隨著測序技術和生物信息學的發展,數十種可以催化分子內D-A反應的酶被從微生物中鑒定出來,這些酶參與了微生物天然產物中茚(如SpnF)、降冰片烯(如SdnG)、十氫化萘(如PryE3、MycB、Phm7、CghA)、螺環(如PyrI4、PloI4、AbyU、VstJ)、吡啶(如TbtD、TclM、PbtD)、雙環[2.2.2]二雜辛烷(如PhqE、MalC、CtdP)等骨架結構的形成。此外,還有一些分子內D-A酶參與了植物中生物堿的生物合成(如CrCS、TiTabS)。
相較于分子內D-A酶,催化分子間D-A反應的酶非常有限,僅有macrophomate 合成酶、riboflavin 合成酶以及催化分子間氧雜Diels-Alder 反應的EupfF。這三個分子間D-A酶除了催化[4+2]環化外,還可催化其他的化學轉化,均屬于多功能D-A酶。隨著對反應機理研究的深入,有些D-A酶被發現并不是通過催化協同的D-A反應機理來構建天然產物中的C-C鍵。例如,越來越多的證據表明macrophomate 合成酶并不是一個分子間D-A酶,而是一個縮醛酶,它通過分步催化Michael加成和Aldol反應而不是D-A反應實現兩個C-C鍵的構建。因此,從最初D-A反應的發現,到目前為止超過了90年,還沒有“真正意義”催化分子間D-A反應的單功能的D-A酶從自然界中被發現。
在植物中存在大量D-A類型天然產物,在它們的生源合成過程中分子間D-A反應是構建其骨架結構的關鍵步驟,暗示著在植物中可能存在催化分子間D-A反應的酶。然而由于D-A酶的功能特殊性以及植物天然產物生物合成研究的技術難點,長期以來人們對于植物中分子間D-A酶知之甚少。
北京大學雷曉光課題組十多年前開始布局進入新的研究領域,聚焦在植物天然產物生物合成與酶催化方向。基于化學生物學的理念,以活性小分子探針的發現、制備與應用為主要研究方向,探索天然產物全合成與化學生物學、合成生物學的高度交叉與融合,將基于化學思維和手段的技術創新與解決生物學實際問題緊密結合,取得了多項開拓性研究成果。近期,該課題組應邀在Accounts of Chemical Research 雜志上發表綜述文章“Hunting for the Intermolecular Diels?Alderase”,系統地總結了課題組圍繞分子間D-A酶的發現、機制解析和合成應用等方面所做出的多項科研成果。該文章也將作為封面文章發表。
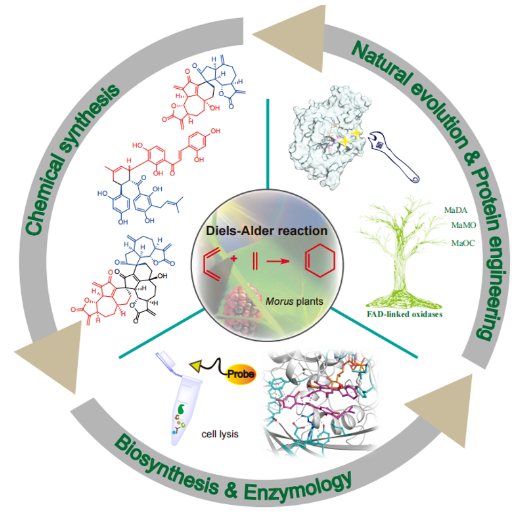
圖1. 植物來源分子間D-A類型天然產物的全合成、生物合成與D-A酶機制研究
雷曉光課題組從建組之初就關注植物來源D-A類型天然產物的生源合成研究,在早期的工作中,雷曉光課題組以分子間D-A反應為關鍵步驟實現了多個倍半萜二聚體以及三聚體的首次全合成(Org. Lett. 2010, 12, 4284?4287;J. Am. Chem. Soc. 2012, 134, 12414?12417;Chem. Sci. 2013, 4, 1163?1167.);后續雷曉光課題組還開發了手性硼酸復合物促進的不對稱D-A反應,并利用該反應實現了桑科植物中多個D-A類型天然產物的首次不對稱全合成(Angew. Chem., Int. Ed. 2014, 53, 9257?9261;Org. Lett. 2016, 18, 360?363;J. Org. Chem. 2016, 81, 458?468)。通過系統性對植物來源D-A類型天然產物進行仿生合成研究,雷曉光課題組制備了大量生物合成中間體以及產物標準品,同時確立了以桑科植物來源的黃酮類型D-A天然產物作為研究對象進行后續D-A酶的挖掘工作。
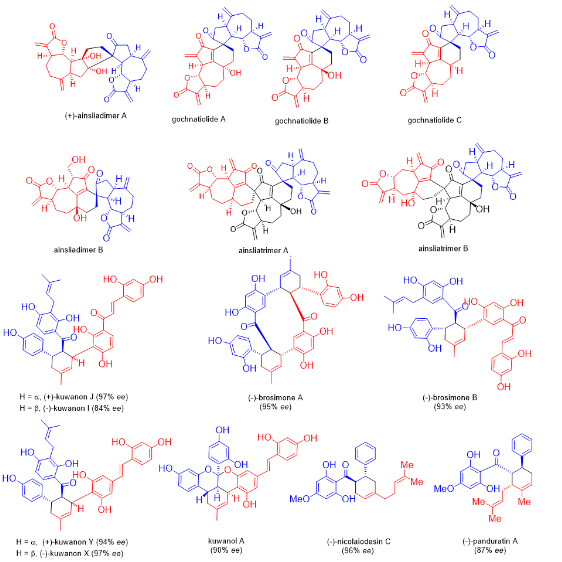
圖2. 雷曉光課題組完成的植物來源分子間D-A類型天然產物仿生合成
在前期仿生合成的基礎之上,雷曉光課題組與合作者提出了一種新穎的基于生物合成中間體探針分子(biosynthetic intermediate probe, BIP)的靶標垂釣化學生物學策略(BIP-based target identification),并結合傳統活性導向蛋白分離以及轉錄組測序等方法,在白桑愈傷組織中鑒定了自然界中首例催化分子間D-A反應的單功能酶MaDA,并解析了其晶體結構,初步闡明了其催化機制,證明了MaDA所催化的分子間 [4+2] 環加成反應是一個協同但不同步的Diels-Alder反應,由此證明了MaDA是首個真正意義上的分子間D-A酶,從而結束了學術界一直存在的“自然界是否有真正意義DA反應酶”的爭論(Nat. Chem. 2020, 12, 620?628)。
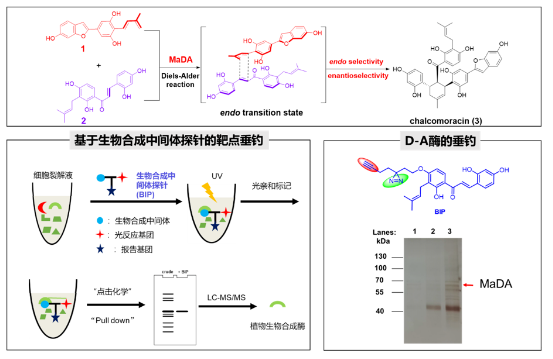
圖3. 利用生物合成中間體探針在桑樹中鑒定了首例分子間單功能D-A酶
在從桑科植物中鑒定了首例單功能分子間D-A酶MaDA之后,雷曉光課題組利用基于同源性的反向遺傳學方法對桑樹中MaDA同源蛋白進行了挖掘和功能表征,在白桑中發現了一類全新的exo選擇性分子間D-A酶,為通過酶催化的手段實現催化劑控制的exo選擇性D-A反應中提供了全新的工具。此外,雷曉光課題組還解析了exo選擇性D-A酶的晶體結構,通過結構比對、計算化學、突變實驗等手段鑒定了不同endo/exo選擇性D-A酶的催化位點,闡明了它們的不同催化機制,為D-A酶的改造應用提供了理論基礎(Nat. Catal. 2021, 4, 1059?1069)。
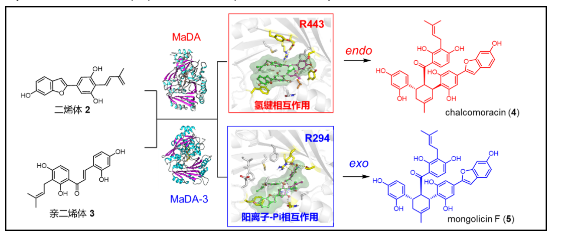
圖4. 不同endo/exo 選擇性分子間D-A酶的催化機制解析
在闡明桑科植物中分子間D-A酶的催化機制后,雷曉光課題組也針對其自然演化機制開展了研究。通過對桑樹中類BBE家族蛋白進行進化樹分析、祖先序列重構、結構解析、計算化學、突變驗證等實驗,雷曉光課題組系統揭示了桑樹中分子間D-A酶從氧化環化酶演化產生的機制。在這一過程中,氧化環化酶經過基因復制事件,形成了D-A酶及其功能相關的二烯體合成酶的共同祖先。在D-A酶演化過程中,祖先酶通過四個關鍵氨基酸殘基的替換(A357L、S348L、D389E和H418R)獲得了催化分子間Diels-Alder反應的能力。此外,突變如I417L和L387Y顯著增強了Diels-Alder活性,而I156V等突變則有效降低了原有的氧化環化活性,推動了氧化環化酶向單功能D-A酶的功能轉變。在D-A酶進化過程中,這四個關鍵突變對于祖先酶底物結合模式的微調起到了至關重要的作用。祖先氧化環化酶原本只能競爭性容納單一底物,而通過引入這些關鍵突變位點后,祖先酶能夠容納兩個底物以進行D-A反應,從而獲得D-A反應活性(Nat. Commun. 2024, 15, 2492,)。該研究不僅深化了我們對D-A酶形成機制的理解,也加深了我們對植物天然產物結構多樣性的酶學機制的認識,更重要的是,它為新穎D-A酶的理性挖掘和改造提供了重要的理論指導,對于D-A酶的進一步開發和利用具有重要科學意義。
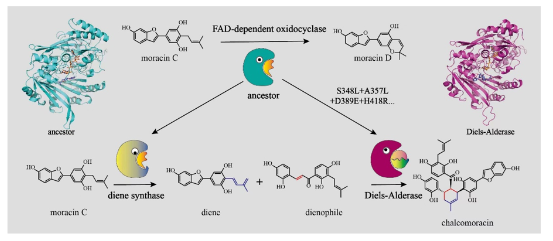
圖5. 桑樹中分子間D-A酶的自然演化機制
在獲得了可以催化不同endo/exo選擇性分子間D-A反應的新穎酶催化工具后,雷曉光課題組還系統性探索了這兩類酶的合成價值。利用這兩類酶的立體專一性和底物寬泛性,雷曉光課題組實現了四十余個桑科植物D-A類型天然產物及其類似物的高效、精準合成(Nat. Catal. 2021, 4, 1059?1069,;Biotechnol. J. 2020, 15, 2000119)。然而,這兩類酶催化工具依然具有底物局限性。為了進一步拓展D-A酶的合成應用范圍,雷曉光課題組針對D-A酶MaDA1進行了蛋白工程改造,并通過將酶催化的D-A反應與金屬催化脫羧官能團化反應巧妙結合,利用生物催化與化學催化相輔相成和優勢互補的特點,實現了環己烯骨架的多樣性導向、精準合成。該研究工作為結構多樣的六元環骨架合成提供了新思路,拓展了D-A酶的催化應用范圍。
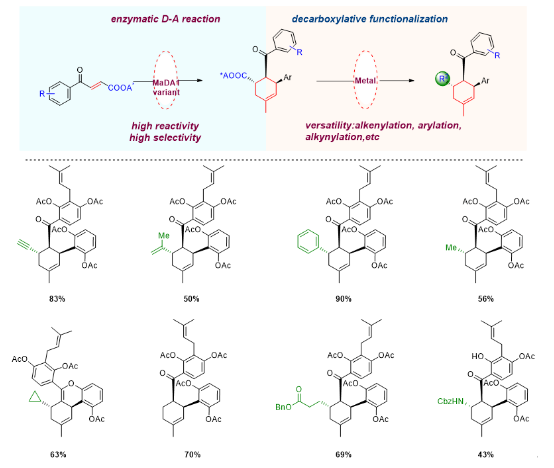
圖6. 利用多樣性導向的化學-酶法合成策略實現了結構多樣的環己烯骨架化合物的立體選擇性合成
基于在植物來源D-A酶方面所取得了重要研究成果,雷曉光課題組應邀以“Hunting for the Intermolecular Diels?Alderase”為題在美國化學會的Accounts of Chemical Research 雜志上發表綜述,詳細總結了基于仿生合成和化學蛋白質組學去發掘植物中新穎工具酶的植物天然產物生物合成研究新范式;詳細介紹了新穎D-A酶的催化以及自然演化機制,為新穎D-A酶的理性挖掘和改造提供了重要的理論指導;并提出了多樣性導向的化學-酶法合成新策略,整合脫羧官能團化反應和酶促D-A反應各自的優勢,實現了D-A產物的高效衍生和制備,為D-A類型天然產物的藥物開發奠定了重要物質基礎(Acc. Chem. Res. 2024, DOI: 10.1021/acs.accounts.4c00315)。此文章中,雷曉光課題組的特聘副研究員高磊博士為第一作者,博士畢業生丁琪博士為第二作者;雷曉光教授為該論文通訊作者。
原文(掃描或長按二維碼,識別后直達原文頁面):

Hunting for the Intermolecular Diels–Alderase
Lei Gao, Qi Ding, and Xiaoguang Lei*
Acc. Chem. Res., 2024, DOI: 10.1021/acs.accounts.4c00315
導師介紹
雷曉光
https://www.x-mol.com/groups/leigroup
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn