



(圖片來源:J. Am. Chem. Soc.)
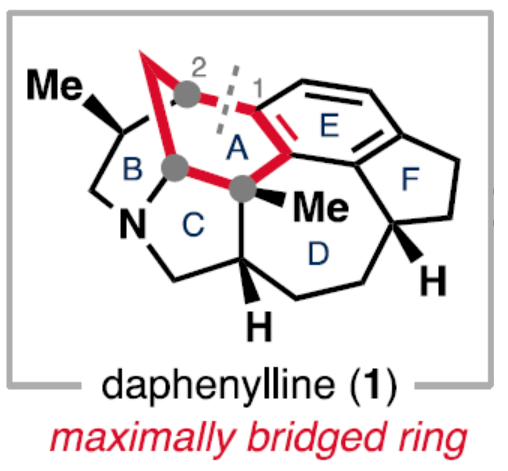
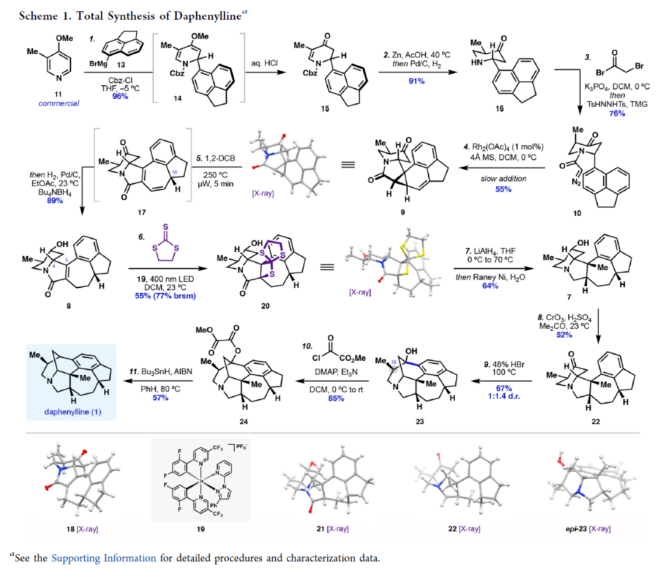
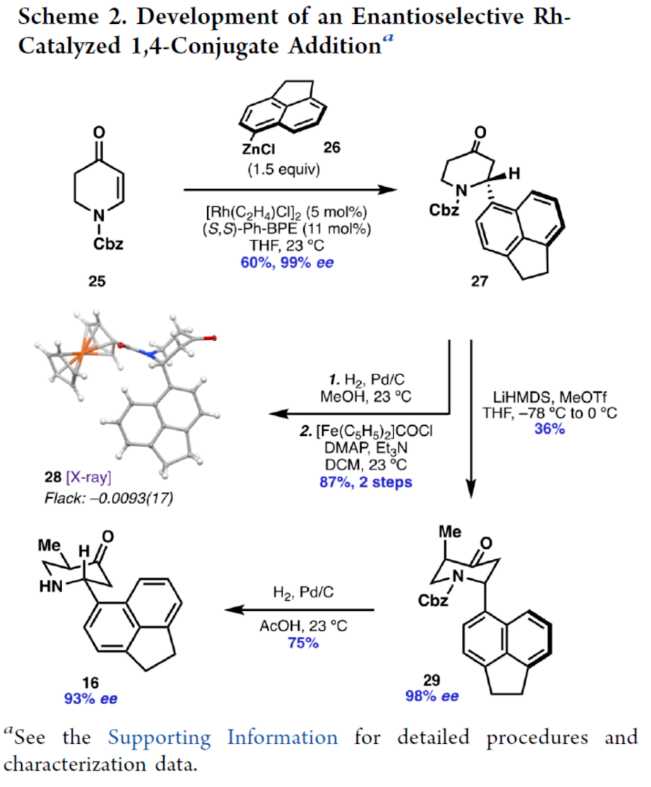
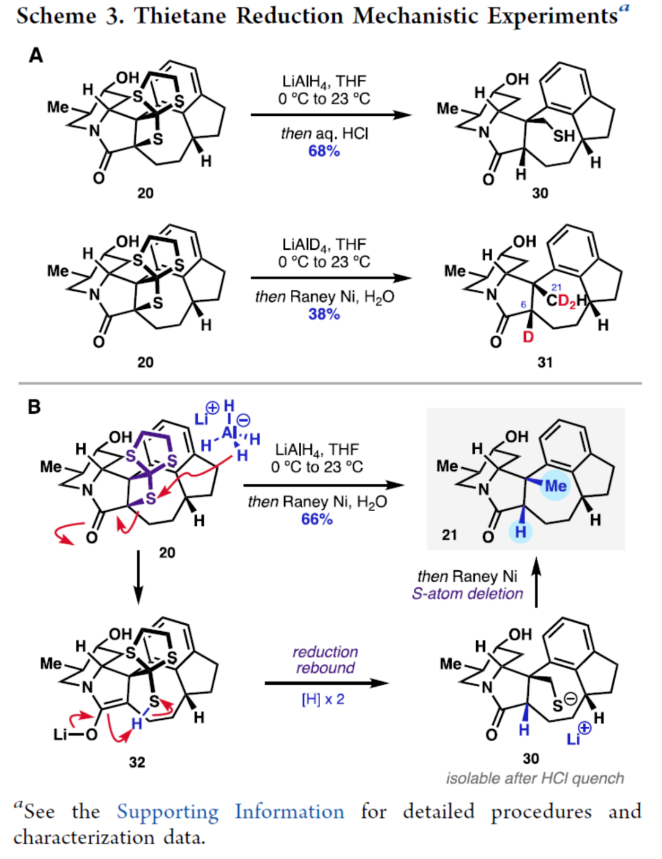
正文 前期,化學(xué)家們已經(jīng)實(shí)現(xiàn)了幾種虎皮楠屬(Daphniphyllum)生物堿的全合成(Figure 1A)。其中,從長序虎皮楠(Daphniphyllum longeracemosum)果實(shí)中發(fā)現(xiàn)的Daphenylline(1),已經(jīng)成為許多合成方法的主題。在結(jié)構(gòu)上,Daphenylline(1)具有一個(gè)2-氮雜雙環(huán)[3.3.1]壬烷核,附加在一個(gè)特征的5-7-5環(huán)骨架上,并包含六個(gè)立體中心、一個(gè)全碳季碳中心和一個(gè)稠合的苯(環(huán))型(benzenoid)核,這在其生物合成相關(guān)的Calyciphylline A-型同源物中是獨(dú)特的。下載化學(xué)加APP到你手機(jī),收獲更多商業(yè)合作機(jī)會。 通過對Daphenylline(1)的逆合成分析發(fā)現(xiàn)(Figure 1B),1可由五環(huán)中間體(7)經(jīng)陽離子芳基化制備。五環(huán)中間體7可以簡化為α,β-不飽和內(nèi)酰胺8,通過共軛加成引入必要的全碳季碳中心。砌塊8中的七元環(huán)可由砌塊9經(jīng)6π-電環(huán)開環(huán)反應(yīng)制備。砌塊9可由α-芳基化哌啶酮10經(jīng)Buchner環(huán)加成制備。α-芳基化哌啶酮10可由市售的吡啶衍生物11和苊12經(jīng)去芳構(gòu)化吡啶鎓芳基化制備。 (圖片來源:J. Am. Chem. Soc.) (±)-Daphenylline(1)的全合成(Scheme 1):吡啶衍生物11在CBz-Cl條件下活化后,加入苊Grignard試劑13,并在酸性條件下進(jìn)行水解,可以96%的收率得到二氫吡啶酮中間體15。中間體15在Zn/AcOH條件下進(jìn)行烯基的還原,并在Pd/C/H2條件下進(jìn)行脫保護(hù),可以91%的收率得到中間體16。中間體16與溴乙酰溴在K3PO4/DCM條件下進(jìn)行N-乙酰化反應(yīng),并在TsHNNHTs/TMG條件下分別進(jìn)行雙對甲苯磺酰肼加成與TMG-介導(dǎo)的雙重亞硫酸酯消除,可以76%的收率得到重氮乙酰胺中間體10。通過反應(yīng)條件的優(yōu)化后發(fā)現(xiàn),中間體10在Rh2(OAc)4/4? MS/DCM條件下進(jìn)行分子內(nèi)Buchner反應(yīng),可以55%的收率得到中間體9,其結(jié)構(gòu)通過X-射線晶體學(xué)分析進(jìn)行了表征。同時(shí),在Buchner反應(yīng)中,需緩慢加入中間體10,可減少均二聚(homodimerization)副反應(yīng)的生成。嚴(yán)格干燥的溶劑還通過防止不需要的O?H鍵插入產(chǎn)物來提高9的收率。通過對反應(yīng)條件的優(yōu)化后發(fā)現(xiàn),中間體9在1,2-DCB/250 oC條件下進(jìn)行熱解生成環(huán)庚二烯中間體17,中間體17在H2/Pd/C/EtOAc/Bu4NBH4條件下進(jìn)行氫化與還原反應(yīng),可以89%的收率得到中間體8。基于大量文獻(xiàn)的總結(jié)以及多種反應(yīng)的嘗試后發(fā)現(xiàn),中間體8在三硫代碳酸乙烯酯在藍(lán)色400 nm LED/DCM條件下進(jìn)行thia-Paterno?-Bu?chi [2 + 2]光環(huán)加成反應(yīng),可以55%的收率得到螺環(huán)硫化環(huán)丙烷中間體20,其結(jié)構(gòu)通過X-射線晶體學(xué)分析進(jìn)行了表征。重要的是,這種轉(zhuǎn)化只生成了head-to-tail的產(chǎn)物,將新形成的C-C鍵置于所需的β-位。通過反應(yīng)條件的優(yōu)化后發(fā)現(xiàn),中間體20在LiAlH/THF條件下進(jìn)行還原,并在Raney Ni/H2O條件下進(jìn)行脫硫反應(yīng),可以64%的收率得到吡咯烷中間體7。中間體7在CrO3/H2SO4/Me2CO條件下進(jìn)行二級醇的氧化反應(yīng),可以52%的收率得到酮中間體22。中間體22在48% HBr/100 oC條件下進(jìn)行還原,可以67%的收率得到氮雜雙環(huán)[3.3.1]壬烷中間體23,dr為1:1.4。中間體23與酰氯衍生物在DMAP/Et3N/DCM條件下進(jìn)行酰化反應(yīng),可以85%的收率得到中間體24。中間體24在Bu3SnH/AlBN/PhH條件下進(jìn)行Barton-McCombie還原反應(yīng),可以57%的收率得到(±)-Daphenylline(1)。 (圖片來源:J. Am. Chem. Soc.) 在實(shí)現(xiàn)了外消旋Daphenylline(1)的全合成后,作者對其的對映選擇性版本進(jìn)行嘗試(Scheme 2)。二氫吡啶酮25與芳基鋅試劑26在[Rh(C2H4)Cl]2/(S,S)-Ph-BPE條件下進(jìn)行1,4-共軛加成反應(yīng),可以60%的收率得到哌啶酮中間體27,ee為99%。將所得的對映體富集的吡啶酮衍生為二茂鐵酰胺,可以通過X-射線晶體學(xué)確認(rèn)絕對構(gòu)型,F(xiàn)lack參數(shù)接近零。中間體27與MeOTf在LiHMDS/THF條件下進(jìn)行α-甲基化反應(yīng),可以36%的收率得到中間體29,ee為98%。中間體29在H2/Pd/C/AcOH條件下進(jìn)行氫解,可以75%的收率得到中間體16,ee為93%,其作為合成(-)-1的中間體。 (圖片來源:J. Am. Chem. Soc.) 隨后,作者對硫化環(huán)丙烷還原機(jī)理實(shí)驗(yàn)進(jìn)行了研究(Scheme 3)。首先,化合物20在使用LiAlH4處理后,再用HCl淬滅,可生成硫醇化合物30,表明了該硫醇是在Raney鎳脫硫之前原位形成的。其次,為了探索syn-立體化學(xué)結(jié)果的來源和氫化物源的作用,作者使用LiAlD4進(jìn)行了同位素標(biāo)記實(shí)驗(yàn)。實(shí)驗(yàn)結(jié)果表明,氫介導(dǎo)的硫化環(huán)丙烷開環(huán),而不是脫硫步驟,是C6-處質(zhì)子引入的原因(因此也是由此產(chǎn)生的syn-立體化學(xué))。總之,作者認(rèn)為,LiAlH4進(jìn)攻硫化環(huán)丙烷化合物20上的張力硫原子,得到烯醇化物32,烯醇化物在“reduction-rebound”機(jī)理序列中通過側(cè)鏈上的硫醇進(jìn)行動力學(xué)質(zhì)子化。在原甲酸硫代酯完全還原為伯硫醇化合物30后,用Raney鎳脫硫得到化合物21。該轉(zhuǎn)化最終通過兩個(gè)步驟實(shí)現(xiàn)了不飽和內(nèi)酰胺8的形式syn-加氫甲基化,這是由thia-Paternoé-Bu?chi[2+2]光環(huán)加成和LiAlH4-介導(dǎo)的reduction-rebound轉(zhuǎn)化的立體特異性所獨(dú)特實(shí)現(xiàn)的。 (圖片來源:J. Am. Chem. Soc.) 總結(jié)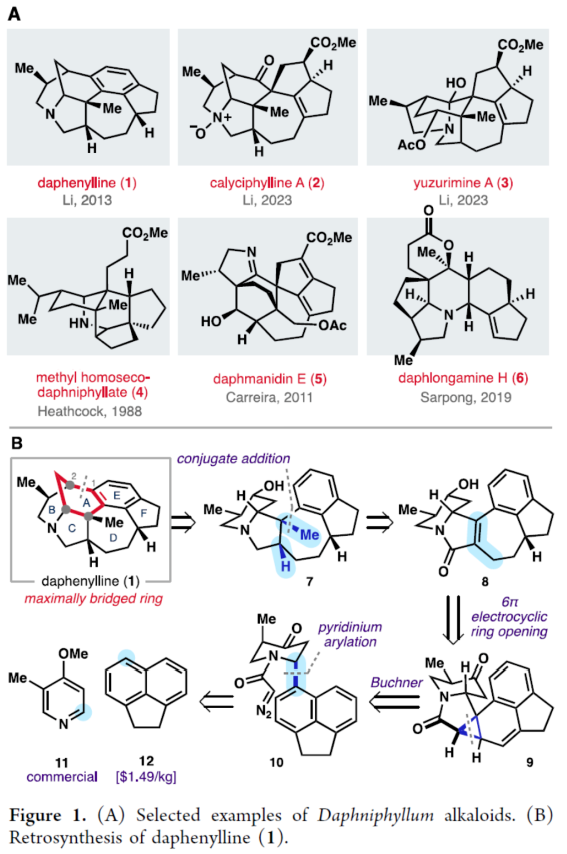
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn