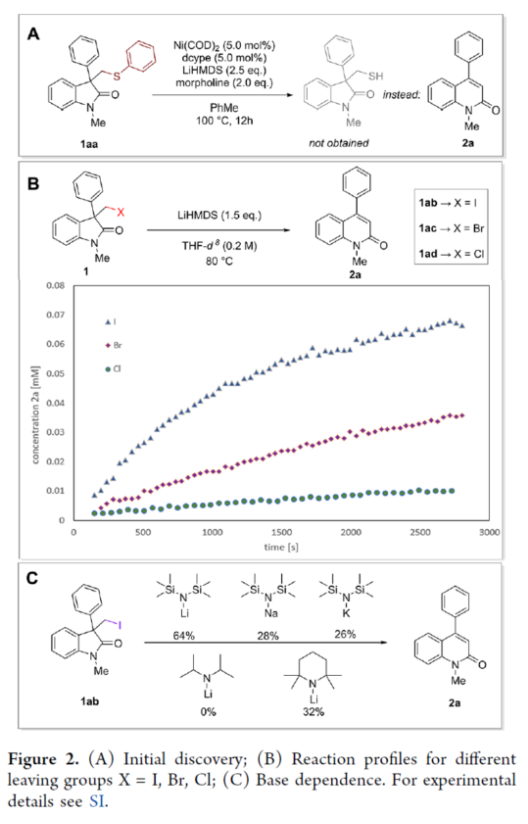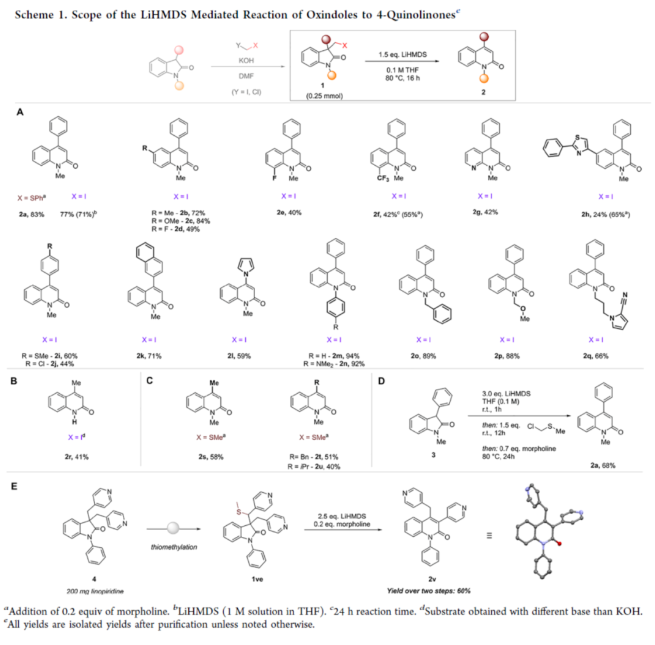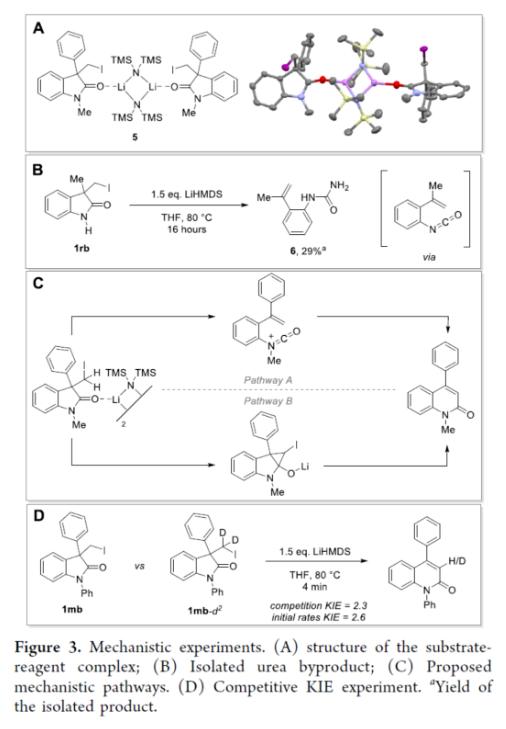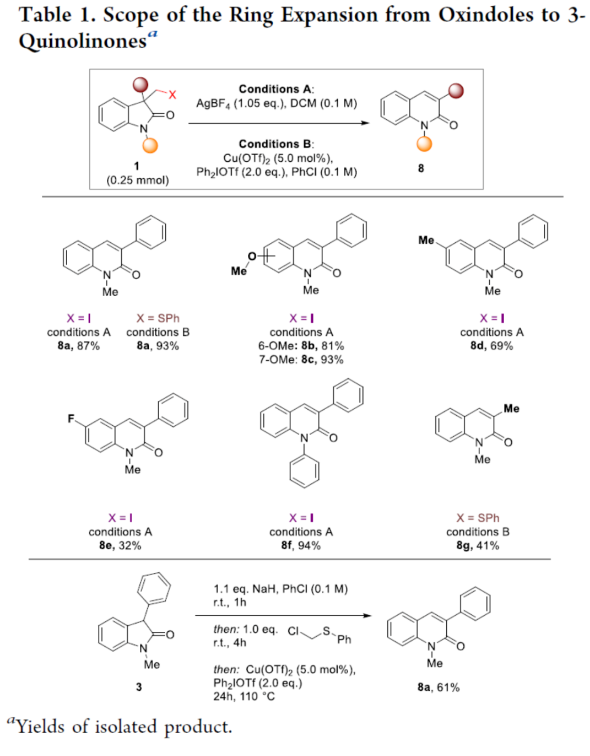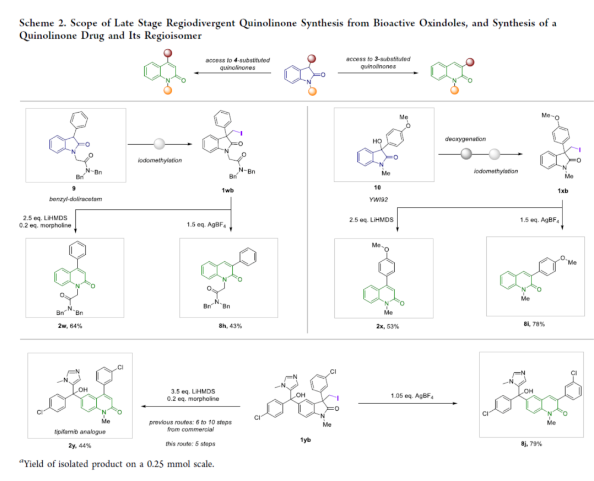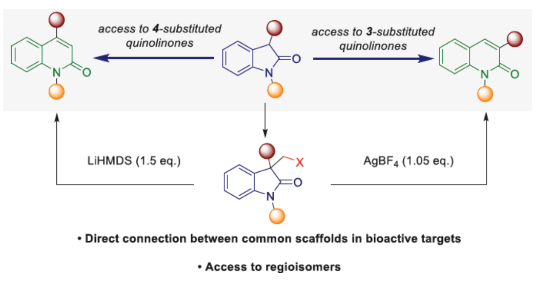
近年來,直接編輯核心骨架的新方法,如切割和縫合(cut-and-sew),以及骨架編輯策略,備受關注。然而,許多生物活性骨架目前不適合這種骨架的修飾,因此仍需開發一種更為高效的方法。到目前為止,除了經典的氮插入外,只有很少的方法可以選擇性地獲得骨架區域異構體。下載化學加APP到你手機,收獲更多商業合作機會。羥吲哚和喹啉酮骨架是兩種特殊的藥物結構單元,這兩種結構都有大量的衍生物可用于各種治療用途,從治療細菌感染到抗病毒應用和癌癥治療。因此,建立一種將羥吲哚轉化為喹啉酮的直接合成途徑,具有鑒定新型生物活性化合物的潛力。如果可以從常見的羥吲哚起始底物中直接獲得喹啉酮的區域異構體,從而進一步簡化結構-活性關系研究,那么這種分子多樣化策略將特別有吸引力。前期,將羥吲哚轉化為喹啉酮的嘗試僅限于含有強吸電子基團的底物或其他特定的起始底物,從而限制了喹啉酮產物的多樣性。同時,對于通過簡單的C1插入從相同的起始底物選擇性地獲得結構不同的喹啉酮的方法,仍有待進一步的探索。近日,蘇黎世聯邦理工學院Bill Morandi課題組開發了一種羥吲哚的區域發散性擴環反應,分別合成了一系列3-或4-取代的喹啉酮衍生物(Figure 1)。前期,Bill Morandi課題組(ACS Catal. 2022, 12, 6081.)研究發現,在鎳催化羥吲哚1aa的轉移胺化后,可獲得4-取代的喹啉酮2a,而不是游離的硫醇(Figure 2A)。進一步的研究發現,僅需LiHMDS和催化量的嗎啉即可實現這種無過渡金屬的轉化。同時,在未添加嗎啉的情況下,也可以觀察到相同的反應性,這進一步增加了該工藝的合成吸引力。其次,離去基團的性質在這種轉化中起著重要作用(Figure 2B)。進一步的對照反應表明,HMDS堿基對實現所需的擴環反應至關重要,其中Li代表了優越的抗衡離子(Figure 2C)。在進一步優化反應條件后發現(see SI,Table S1),當以3-碘甲基羥吲哚1ab為底物,LiHMDS(1.5 equiv)作為堿,在THF溶劑中80 oC反應16 h,可以77%的收率得到產物2a。在獲得上述最佳反應條件后,作者對合成4-取代喹啉酮衍生物的底物范圍進行了擴展(Scheme 1)。首先,羥吲哚底物的芳基上含有不同電性取代基以及雜環衍生物時,均可順利進行反應,獲得相應的產物2a-2h,收率為40-84%。3-取代的羥吲哚以及羥吲哚的酰胺氮上含有不同的取代基時,均與體系兼容,獲得相應的產物2i-2q,收率為44-94%(Scheme 1A)。然而,3-烷基取代的羥吲哚僅導致起始底物發生脫碘(Scheme 1B)。其次,使用-SMe代替-I的羥吲哚,也是合適的底物,獲得相應的產物2s-2u,收率為40-58%(Scheme 1C)。值得注意的是,與之前的多步合成2a的反應相比,該策略具有簡單性和適用性(Scheme 1D)。此外,該策略還可用于小分子藥物利諾吡啶(4)的后期修飾,可以兩步60%的總收率得到二取代喹啉酮產物2v(Scheme 1E)。緊接著,作者對反應的機理進行了研究(Figure 3)。首先,通過對底物-試劑配合物5之間的分子間相互作用分析發現,所使用的堿與底物中的羰基氧配位。鋰堿和酰胺的類似相互作用也很突出,它們利用這種相互作用活化酰胺部分,從而實現隨后的親核進攻或去質子化(Figure 3A)。同時,在N?H羥吲哚1rb的反應中,成功分離了一種尿素衍生物6(Figure 3B)。從機理上講,這種副產物可以通過去質子化后分子內消除串聯反應形成異氰酸酯中間體來解釋。隨后,通過環化從而獲得所需產物。或者,在副反應中,異氰酸酯中間體可以被LiHMDS親核進攻,然后在后處理中水解,從而解釋所觀察到的尿素的形成。基于上述的研究,作者提出了一種合理的反應機理(Figure 3C)。在pathway A中,涉及形成一種高能的陽離子異氰酸酯中間體的過程。在pathway B中,涉及形成一種環丙基醇化物中間體的過程。為了區分這兩種反應的機理,作者進行了相關的對照實驗。在陽離子異氰酸酯中間體的情況下,LiHMDS必須以Lewis酸的形式與酰胺結合,以使C2?C3鍵能夠相應地斷裂。然而,由于沒有其他更常見的Lewis酸能夠實現所需的反應性,并且Hammett分析沒有表明氮上有正電荷積聚,因此這種機理似乎不太可能。競爭性的KIE實驗結果表明,C?H鍵的斷裂是決速步驟(Figure 3D)。此外,通過對反應條件的再次優化后發現,當在AgBF4/DCM或Cu(OTf)2/ Ph2IOTf/PhCl條件下,一系列不同取代的羥吲哚底物,均可順利反應,獲得相應的3-取代喹啉酮產物8a-8g,收率為32-94%(Table 1)。同時,與之前的合成8a的多步反應相比,該策略的操作更為簡單與高效。最后,作者對反應的實用性進行了研究(Scheme 2)。首先,多拉西坦(Doliracetam)衍生物9經兩步反應,可分別以64%的總收率得到4-取代的喹啉酮化合物2w,以43%的總收率得到3-取代的喹啉酮化合物8h。其次,YWI92(10,一種由3-羥基-3-取代的羥吲哚組成的癲癇抑制劑)經三步反應,可分別以53%的總收率得到4-取代的喹啉酮化合物2x,以78%的總收率得到3-取代的喹啉酮化合物8i。此外,以1yb為底物,可直接合成替吡法尼類似物(Tipifarnib)2y,收率為79%,這也是其最短的合成路線。蘇黎世聯邦理工學院Bill Morandi課題組開發了一種全新的方法,通過區域發散性骨架的編輯實現了羥吲哚至3-或4-取代的喹啉酮衍生物的轉化。同時,該方法在生物活性羥吲哚的后期官能團化反應中具有出色的兼容性,并適用于喹啉衍生物的合成。文獻詳情:
Hendrik L. Schmitt, Den Martymianov, Ori Green, Tristan Delcaillau, Young Seo Park Kim, Bill Morandi*. Regiodivergent Ring-Expansion of Oxindoles to Quinolinones. J. Am. Chem. Soc. 2024, https://doi.org/10.1021/jacs.3c12119