



(圖片來源:J. Am. Chem. Soc.)
正文
發(fā)展有機(jī)氟化合物的新合成方法具有重要意義,因?yàn)樗鼈冊谵r(nóng)用化學(xué)品、材料化學(xué)、醫(yī)學(xué)診斷(正電子發(fā)射斷層掃描)和制藥(2018年和2019年FDA批準(zhǔn)的小分子藥物中,超過40%至少有一個碳-氟鍵)等領(lǐng)域均具有重要的應(yīng)用價值。就藥物而言,碳-氟鍵的存在可以使藥物具有良好的代謝穩(wěn)定性和生物利用度等優(yōu)勢。目前,化學(xué)家們已經(jīng)發(fā)展了多種機(jī)理來構(gòu)建碳-氟鍵,包括親核氟化、自由基氟化和親電氟化。下載化學(xué)加APP到你手機(jī),更加方便,更多收獲。
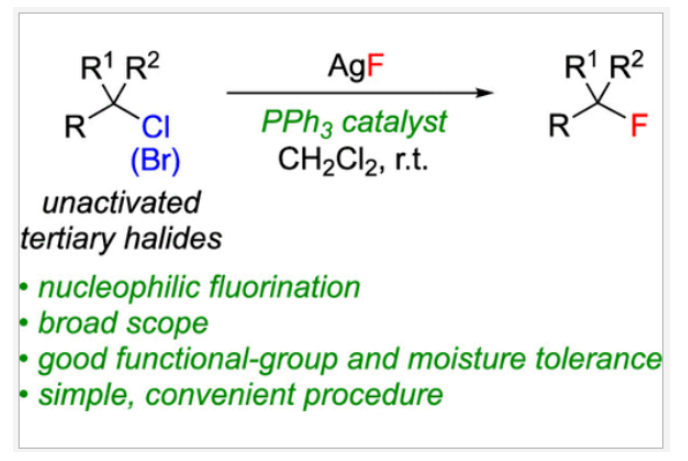
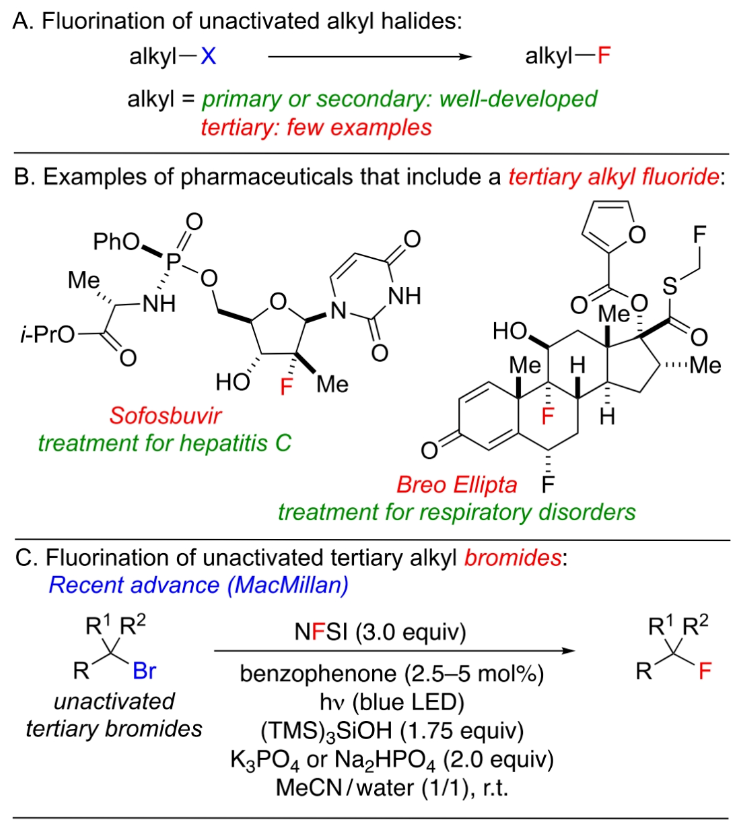
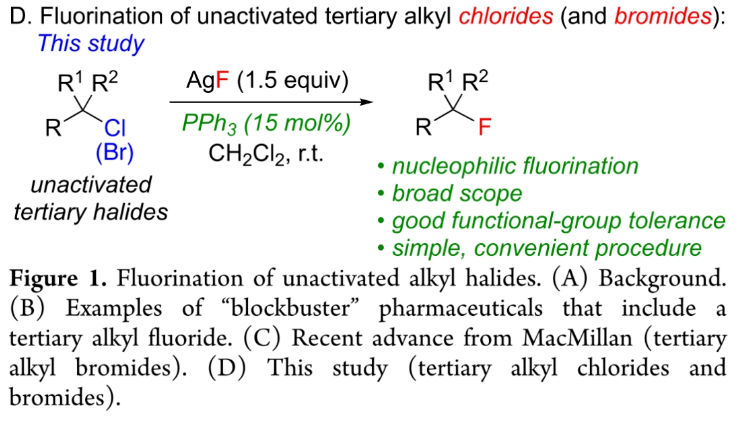
用氟來取代非活化的烷基鹵化物種的鹵原子是合成有機(jī)氟化合物的方法之一。雖然化學(xué)家們在一級鹵化物和二級鹵化物的氟化方面已經(jīng)取得了重大進(jìn)展,但對于三級鹵化物,特別是氯化物的氟化方法相對較少(Figure 1A)。因此Figure 1B中所展示的含有三級烷基氟骨架的藥物分子的合成則具有一定的挑戰(zhàn)性。最近,MacMillan課題組使用親電氟化劑NFSI,通過光誘導(dǎo)的自由基途徑實(shí)現(xiàn)了非活化三級烷基溴的氟化反應(yīng)(Figure 1C)。然而,文中僅有零星幾個例子實(shí)現(xiàn)了三級烷基溴化物和碘化物的氟化過程。而非活化三級烷基氯化物的氟化更是非常罕見的。目前僅可以實(shí)現(xiàn)金剛烷基氯的氟化(不容易消除H-Cl),以及通過使用HF作為氟源來實(shí)現(xiàn)非官能團(tuán)化氯化物的氟化反應(yīng)。近期,美國加州理工學(xué)院Gregory C. Fu課題組發(fā)展了一種溫和的方法,利用廉價的PPh3催化,商業(yè)可得的AgF作為氟源,在室溫下實(shí)現(xiàn)了非活化三級烷基氯化物和溴化物的氟化反應(yīng)(Figure 1D)。
(圖片來源:J. Am. Chem. Soc.)
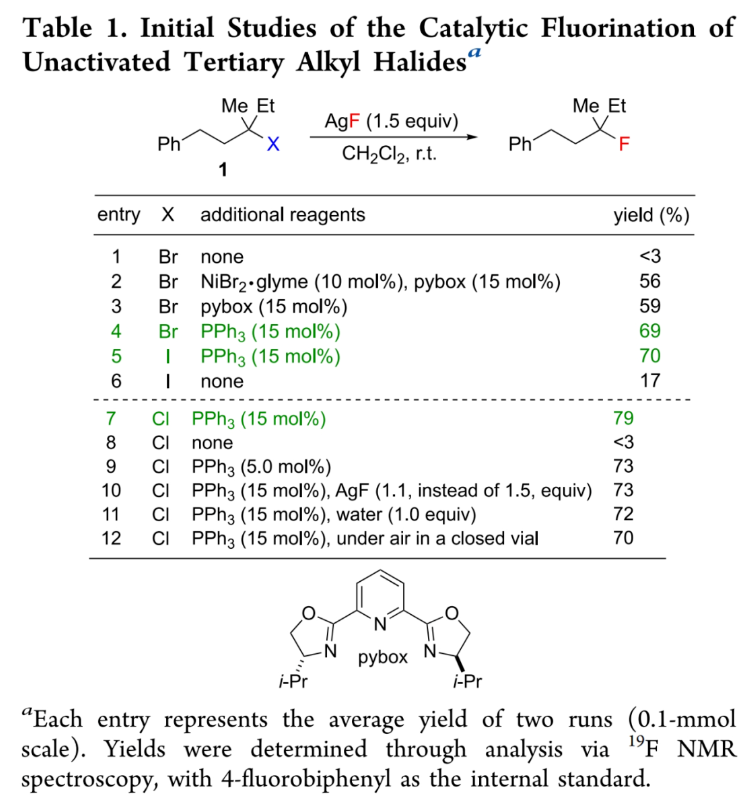
首先,作者選擇三級烷基鹵化物1作為模板底物進(jìn)行反應(yīng)探索(Table 1)。通過一系列反應(yīng)參數(shù)優(yōu)化,作者得出當(dāng)使用三級烷基氯化物1 (1.0 equiv), PPh3 (15 mol%), AgF (1.5 equiv) 在CH2Cl2中室溫反應(yīng)可以以79%的產(chǎn)率得到目標(biāo)氟化產(chǎn)物(entry 7)。此外,當(dāng)使用三級烷基溴化物和三級烷基碘化物作起始原料時,在相同的條件下可以分別以69%和70%的產(chǎn)率得到相應(yīng)的三級烷基氟化物(entries 4,5)。空白實(shí)驗(yàn)表明反應(yīng)在不存在PPh3時是不能發(fā)生的(entry 8)。
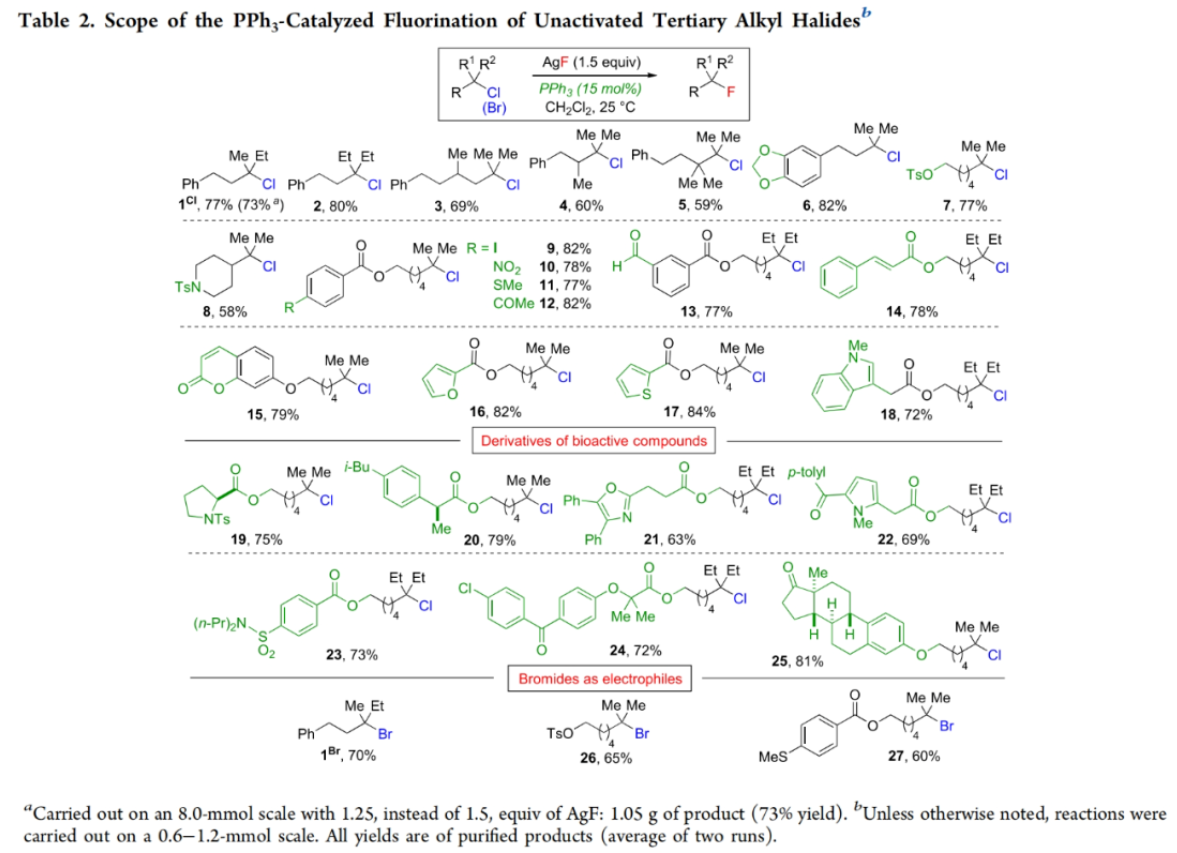
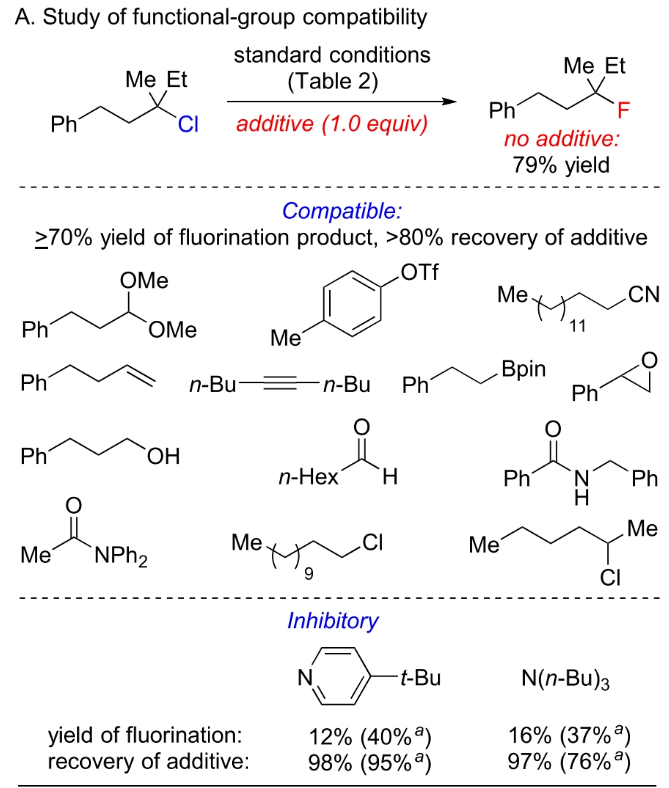
在得到了最優(yōu)反應(yīng)條件后,作者對此反應(yīng)的底物范圍進(jìn)行了探索(Table 2)。該轉(zhuǎn)化對具有不同空間位阻的非活化三級烷基氯化物的氟化過程均是有效的,包括與季碳相連的三級烷基氯化物5也可兼容,以59%的產(chǎn)率得到相應(yīng)的氟化產(chǎn)物。此外,此反應(yīng)可以放大至克級規(guī)模而產(chǎn)率基本不變(1,8 mmol,73%),證明了此轉(zhuǎn)化的實(shí)用性。值得注意的是,此碳-氟鍵形成反應(yīng)可以兼容一系列官能團(tuán),包括縮醛、非活化三級烷基甲磺酸酯、磺酰胺、酯、芳基碘、硝基芳烴、硫醚、酮、醛、α, β-不飽和酯以及各種氧、硫和氮雜環(huán)。通過添加劑研究,作者發(fā)現(xiàn)三氟甲磺酸酯、腈、烯烴、內(nèi)炔、烷基硼酸酯、環(huán)氧化物、醇、二級酰胺和三級酰胺等基團(tuán)也可兼容此氟化體系,而吡啶和三級胺則不能兼容,這可能是由于它們與銀的強(qiáng)結(jié)合能力所致(Figure 2A)。值得注意的是,此反應(yīng)還可以兼容一系列天然產(chǎn)物和生物活性分子19-25,以63-81%的產(chǎn)率得到相應(yīng)的氟化產(chǎn)物。此外,此轉(zhuǎn)化對一系列三級烷基溴化物(1Br, 26, 27)同樣兼容性良好,以60-70%的產(chǎn)率得到相應(yīng)的氟化產(chǎn)物。
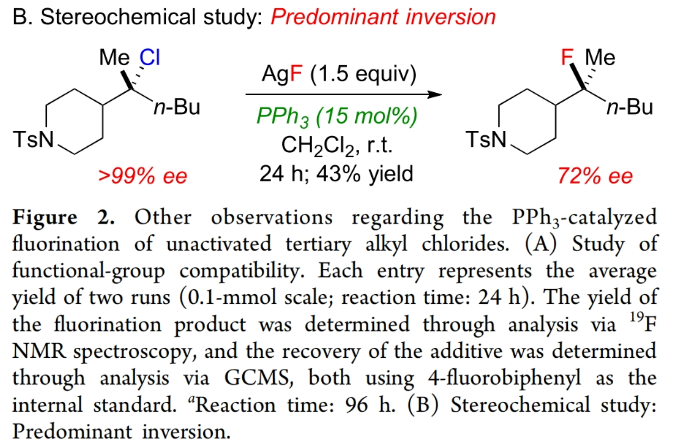
機(jī)理方面,作者認(rèn)為此膦催化烷基氯的氟化反應(yīng)可能是通過銀輔助氯與叔烷基親電試劑解離進(jìn)行的,其中PPh3可以與AgF形成[Ag(PPh3)n]X。確實(shí),作者在反應(yīng)起始階段通過31P NMR和高分辨質(zhì)譜觀察到了[Ag(PPh3)4]+的存在。有趣的是,當(dāng)對映體富集的非活化三級烷基氯化物進(jìn)行氟化反應(yīng)時,取代過程主要經(jīng)歷了反轉(zhuǎn)的立體化學(xué),這可能是由于氯離子解離后形成的銀絡(luò)合物屏蔽了陽離子的一個面所致(Figure 2B)。
(圖片來源:J. Am. Chem. Soc.)
總結(jié)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn