



帕金森癥(Parkinson’s disease)是一種常見的神經(jīng)退行性疾病,其典型病理特征為腦黑質(zhì)致密部病變和多巴胺濃度顯著降低。帕金森癥會引起運動障礙/遲緩、靜息性震顫、認(rèn)知障礙等癥狀。帕金森癥無法治愈,嚴(yán)重危害患者生命。而該疾病的早期、準(zhǔn)確診斷和合理的治療是減緩病情發(fā)展和延長患者生命的重要途徑。目前,帕金森癥的診斷方法包括影像學(xué)、腦脊液分析、基因檢查等,存在滯后、間接、主觀性強、受其它腦部疾病干擾等缺點,容易造成誤診、漏診和延遲診斷。帕金森癥治療方式主要為口服左旋多巴(Levodopa, L-Dopa)。左旋多巴能夠在腦組織內(nèi)被單胺能神經(jīng)元轉(zhuǎn)化為多巴胺,從而達(dá)到治療帕金森癥的目的。但受個體差異、病程和耐藥性影響,左旋多巴藥物劑量較難準(zhǔn)確控制,治療過程易引起嚴(yán)重副反應(yīng)。針對上述問題,蘇彬課題組將腦電化學(xué)測量和動態(tài)給藥系統(tǒng)結(jié)合,發(fā)展了一種帕金森癥閉環(huán)診斷和治療方法,該方法不僅能夠通過腦內(nèi)多巴胺濃度水平診斷/跟蹤帕金森癥,還能夠通過實時測量的濃度信息動態(tài)調(diào)節(jié)左旋多巴給藥速度和劑量,有效提高左旋多巴治療效果。該研究工作為帕金森癥的診斷和治療提供了新思路。相關(guān)成果最近發(fā)表在美國化學(xué)會志期刊上(J. Am. Chem. Soc., doi.org/10.1021/jacs.3c08256)。
作者首先將共價有機(jī)框架材(COF)薄膜修飾于碳纖維微電極表面(電極簡稱為cCFE,圖1),利用COF薄膜親水性、電荷選擇性和納米孔道空間限域作用提高腦內(nèi)多巴胺測量準(zhǔn)確性和穩(wěn)定性(圖2)。具體如下所述:(1)抗生物污染性能。生物污染,包括蛋白質(zhì)非特異性吸附、細(xì)胞黏附和生物免疫反應(yīng),會污染電極表面,影響傳荷/傳質(zhì)過程,大幅降低植入電極性能。COF薄膜能夠通過納米孔道尺寸選擇性、表面親水性和電荷選擇性抑制電極表面蛋白質(zhì)非特異性吸附、細(xì)胞黏附和生物免疫反應(yīng),大幅提高電極抗生物污染性能和腦內(nèi)穩(wěn)定性;(2)抗化學(xué)污染性能。多巴胺和其氧化產(chǎn)物容易在電極表面發(fā)生化學(xué)聚合,形成聚多巴胺,極大影響電極多巴胺檢測性能。COF的納米孔道可以通過納米限域作用控制多巴胺分子構(gòu)象,調(diào)控其氧化過程,避免氧化產(chǎn)物或聚多巴胺在電極表面形成和吸附,抑制電極表面化學(xué)污染;(3)多巴胺選擇性。腦內(nèi)存在多種與多巴胺結(jié)構(gòu)、電荷和電化學(xué)性質(zhì)相似的神經(jīng)遞質(zhì),主要包括血清素(Serotonin, 5-HT)、腎上腺素(Epinephrine, EP)和去甲腎上腺素(Norepinephrine, NE)。這些遞質(zhì)信號與多巴胺信號重合,會影響電化學(xué)測量結(jié)果準(zhǔn)確性。作者利用不同種類神經(jīng)遞質(zhì)與COF孔道間吸附能的差異,調(diào)控不同神經(jīng)遞質(zhì)通過孔道到達(dá)電極表面的難易程度,從而實現(xiàn)cCFE對多巴胺的選擇性測量。
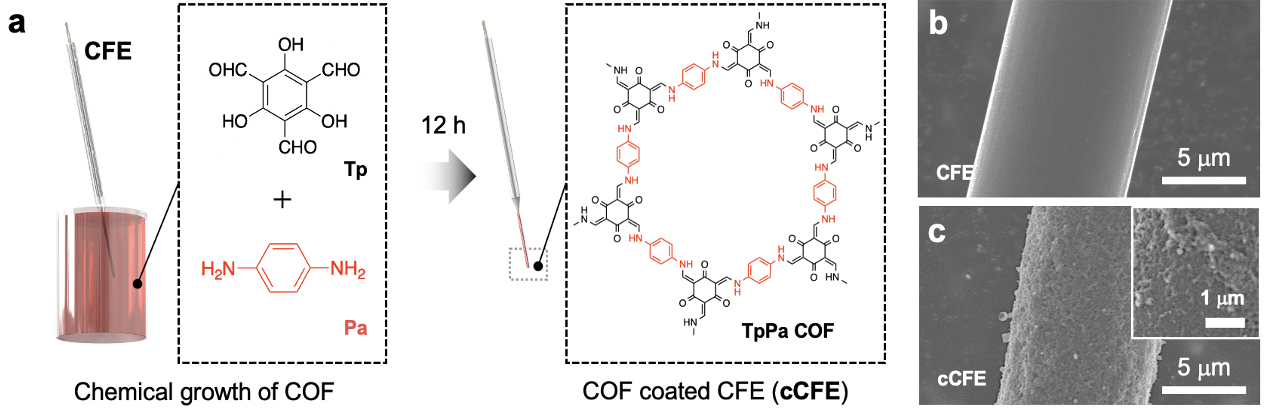
圖1.(a)共價有機(jī)框架薄膜修飾碳纖維電極(cCFE)的制備;(b, c)碳纖維微電極(CFE)和cCFE的掃描電子顯微鏡圖。
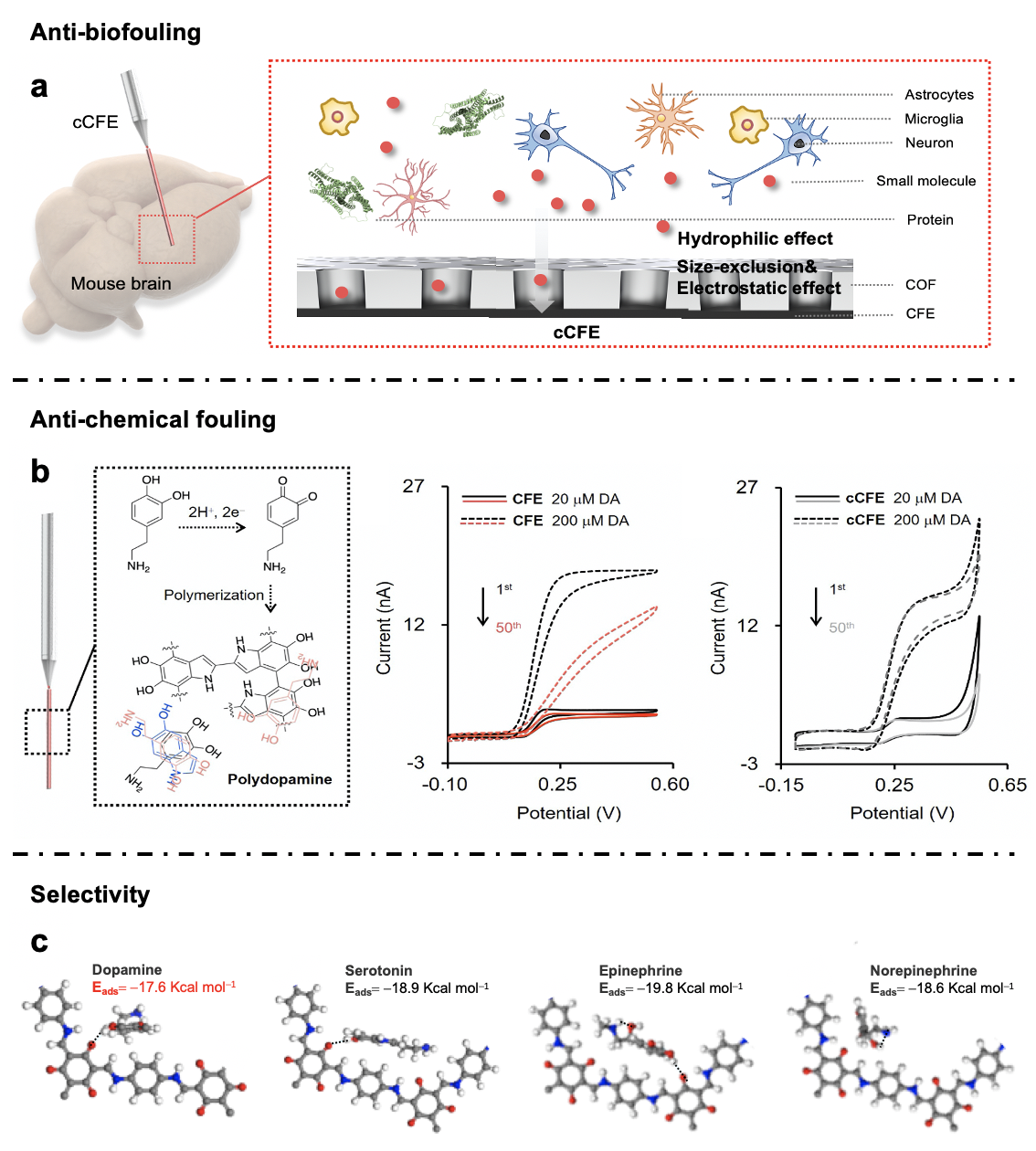
圖2. cCFE的抗生物污染性能(a)、抗化學(xué)污染性能(b)和多巴胺選擇性(c)。
最后,作者將腦電化學(xué)測量與動態(tài)給藥系統(tǒng)結(jié)合,發(fā)展一種帕金森癥閉環(huán)診斷和治療方法(圖3a)。由于多巴胺能神經(jīng)元凋亡,帕金森病模型小鼠腦內(nèi)缺少有效的多巴胺調(diào)節(jié)機(jī)制,在單次注射高劑量左旋多巴后帕金森模型鼠腦紋狀體中多巴胺濃度大幅上升,遠(yuǎn)高于正常范圍,進(jìn)而引起心率異常等不良藥物反應(yīng)(圖3b)。而該閉環(huán)系統(tǒng)能夠利用實時測量的腦內(nèi)多巴胺濃度信息動態(tài)調(diào)節(jié)左旋多巴給藥速度和劑量,有效提高左旋多巴治療效果、避免不良藥物反應(yīng)。在該閉環(huán)治療模式下,帕金森病模型小鼠腦多巴胺濃度均位于正常水平范圍(圖3c)。此外,帕金森患者腦黑質(zhì)致密部多巴胺能神經(jīng)元大量凋亡會引起紋狀體內(nèi)多巴胺濃度顯著降低。通過直接測量的狀體內(nèi)多巴胺濃度還可輔助帕金森癥診斷。
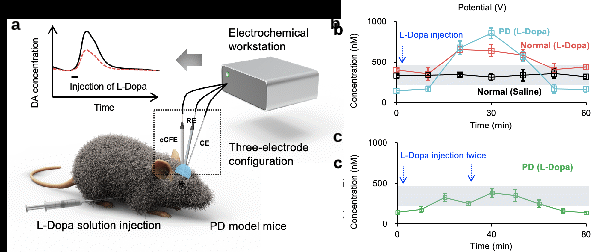
圖3.(a)帕金森癥閉環(huán)診斷和治療方法示意圖;(b)單次注射高劑量左旋多巴或生理鹽水后健康鼠和帕金森模型小鼠紋狀體中多巴胺濃度隨時間變化;(c)采用閉環(huán)方法多次注射低劑量左旋多巴后帕金森模型小鼠紋狀體中多巴胺濃度隨時間變化。
小結(jié):在本工作中,作者首先發(fā)展了一種兼具優(yōu)良電化學(xué)性能、抗生物污染性能、抗化學(xué)污染性能和選擇性的腦多巴胺測量電極,實現(xiàn)小鼠腦內(nèi)多巴胺濃度的長時、連續(xù)、穩(wěn)定和靈敏測量。然后,將腦電化學(xué)測量技術(shù)與動態(tài)給藥結(jié)合,發(fā)展了一種帕金森癥閉環(huán)治療方法,并探究了新療法在療效和避免不良反應(yīng)中的優(yōu)勢。該研究工作可為帕金森癥的診斷和治療提供指導(dǎo)。
浙江大學(xué)化學(xué)系博士后周璘和博士研究生楊蓉婕為本文的共同第一作者,通訊作者是浙江大學(xué)蘇彬教授。該項目受到國家自然科學(xué)基金等經(jīng)費資助。
文章鏈接:https://pubs.acs.org/doi/10.1021/jacs.3c08256?ref=PDF
蘇彬教授課題組鏈接:https://person.zju.edu.cn/binsu
T細(xì)胞表位抗原疫苗與T細(xì)胞受體(TCR)-T細(xì)胞療法是抗腫瘤領(lǐng)域兩種新穎的免疫治療策略,顯示出極為優(yōu)越的療效。T細(xì)胞表位抗原疫苗是通過引入特定腫瘤抗原多肽,刺激患者體內(nèi)自身T細(xì)胞產(chǎn)生高效腫瘤免疫應(yīng)答;而TCR-T細(xì)胞療法則利用基因工程技術(shù)使T細(xì)胞表達(dá)特定腫瘤特異性TCR克隆,高效識別腫瘤抗原并殺死腫瘤細(xì)胞。準(zhǔn)確篩選并鑒定有效腫瘤特異性抗原多肽及TCR克隆是腫瘤治療領(lǐng)域的一大難點。
近日,蘇彬課題組通過免疫突觸的電化學(xué)發(fā)光(ECL)成像,實現(xiàn)了T細(xì)胞腫瘤抗原識別的免標(biāo)記分析(圖1)。將特異性刺激分子修飾在基底電極表面,刺激并激活T細(xì)胞,使其形成免疫突觸。由于細(xì)胞粘附抑制ECL反應(yīng),因此ECL圖像中免疫突觸形成區(qū)域表現(xiàn)為暗斑。通過分析細(xì)胞的鋪展面積和識別強度來評估免疫突觸的結(jié)合特性,實現(xiàn)了對不同種類腫瘤抗原(pMHC)、不同抗原反應(yīng)性的TCR以及形成免疫突觸所需的相關(guān)輔助分子(如信號傳遞分子CD3、共刺激分子CD28和粘附分子LFA1)的區(qū)分。這種免標(biāo)記的成像策略有望應(yīng)用于高效腫瘤特異性抗原多肽及TCR克隆的篩選與鑒定。相關(guān)成果最近發(fā)表在德國應(yīng)用化學(xué)期刊上(Angew. Chem. Int. Ed. doi.org/10.1002/anie.202314588)。
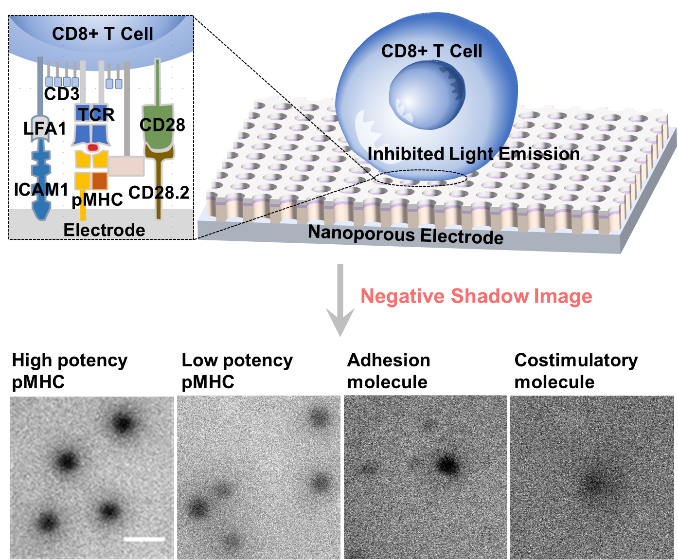
圖1. T細(xì)胞抗原識別和區(qū)分的免標(biāo)記ECL成像示意圖
T細(xì)胞通過其表面的TCR識別腫瘤細(xì)胞上的特異性抗原,與腫瘤細(xì)胞形成穩(wěn)定免疫突觸,從而釋放穿孔蛋白酶和細(xì)胞因子等,以達(dá)到殺傷腫瘤細(xì)胞的目的。鑒于免疫突觸結(jié)構(gòu)決定著T細(xì)胞對腫瘤細(xì)胞的殺傷,可將其作為T細(xì)胞腫瘤特異性抗原識別的特征。目前,通常運用熒光成像技術(shù)(如全內(nèi)反射熒光成像)來表征免疫突觸的形成。但其需要額外的熒光標(biāo)記,且易受細(xì)胞自體熒光和熒光分子光漂白特性的限制。因此,迫切需要開發(fā)快速和免標(biāo)記的成像方法來表征免疫突觸的形成,用于鑒定有效的腫瘤特異性抗原多肽及TCR克隆。
課題組前期工作采用ECL成像技術(shù)實現(xiàn)了對細(xì)胞黏著和細(xì)胞間連接的順次成像。在此基礎(chǔ)上,該工作通過改變ECL分子與共反應(yīng)劑的濃度比來調(diào)控ECL反應(yīng)路徑,以獲得限域或延展的發(fā)光層(分別對應(yīng)氧化還原路徑和催化路徑),并將其應(yīng)用于T細(xì)胞免疫突觸成像。實驗結(jié)果表明氧化還原路徑主導(dǎo)的電化學(xué)發(fā)光更適合成像免疫突觸(圖2)。這是因為免疫突觸是在T細(xì)胞基底膜與電極表面接觸的微區(qū)內(nèi)形成,表面限域的發(fā)光層才能有效地對免疫突觸這一界面結(jié)構(gòu)進(jìn)行良好觀察。

圖2. 調(diào)控發(fā)光層厚度,成像T細(xì)胞免疫突觸
隨后采用上述表面限域ECL成像體系對多種腫瘤抗原多肽及不同克隆TCR-T細(xì)胞進(jìn)行配對識別驗證。結(jié)果顯示,ECL可對TCR-T細(xì)胞與對應(yīng)的特異性腫瘤抗原形成穩(wěn)定的免疫突觸結(jié)構(gòu)進(jìn)行成像;通過對ECL圖像進(jìn)行分析,定量評估免疫突觸形成的面積和強度,實現(xiàn)了T細(xì)胞抗原識別強弱的區(qū)分(圖3)。
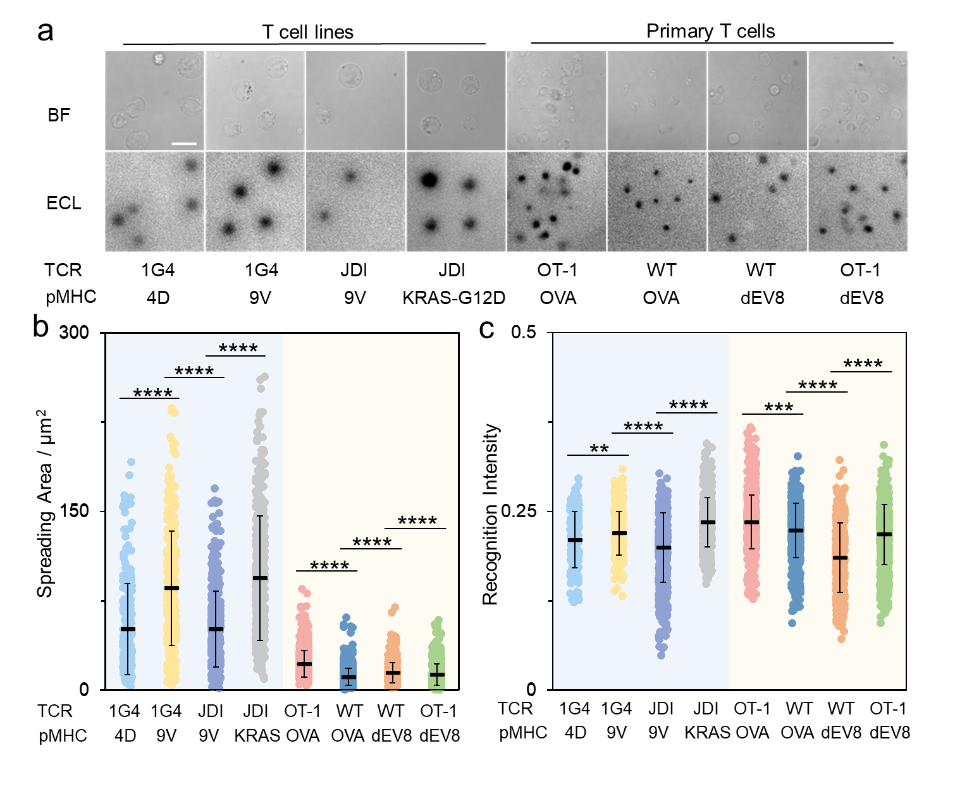
圖3. 對多種腫瘤抗原多肽及不同克隆TCR-T細(xì)胞進(jìn)行配對識別驗證
綜上所述,該工作開發(fā)了一種T細(xì)胞免疫突觸的免標(biāo)記ECL成像技術(shù),并將其用于腫瘤特異性抗原多肽及TCR克隆的鑒定。該技術(shù)有望用于腫瘤特異性抗原及TCR克隆的篩選,這對T細(xì)胞表位抗原疫苗與TCR-T細(xì)胞療法的發(fā)展至關(guān)重要。
本文的作者是浙江大學(xué)化學(xué)系博士研究生顏亞娟(化學(xué)系21級直博生)、浙江大學(xué)生物系統(tǒng)工程與食品科學(xué)學(xué)院博士后周萍和浙江大學(xué)化學(xué)系博士研究生丁鷺榕(化學(xué)系23級碩博連讀生)。通訊作者是浙江大學(xué)化學(xué)系蘇彬教授、基礎(chǔ)醫(yī)學(xué)院陳偉教授和醫(yī)學(xué)院附屬第一醫(yī)院胡煒特聘研究員。該項目受到國家自然科學(xué)基金的經(jīng)費資助。
文章鏈接:https://doi.org/10.1002/anie.202314588
課題組鏈接:https://mypage.zju.edu.cn/binsu/696525.html
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點或證實其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn