

(圖片來源:Nat. Commun.)
正文
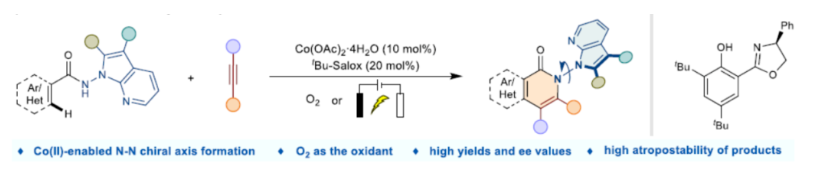
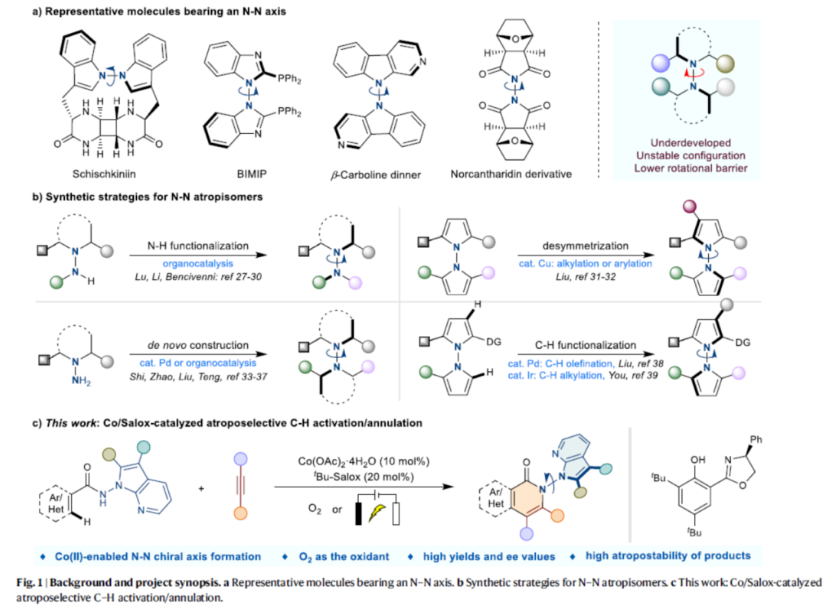
阻轉異構體是一類有趣的軸手性化合物,在藥物開發以及功能材料開發中備受關注。在過去的二十年中,化學家們已開發多種構建C-C和C-N阻轉異構體的方法,包括軸手性聯芳基、芳基胺和芳基酰胺等。雖然N-N軸骨架廣泛存在于各類天然產物、生物活性分子、功能材料和配體中(Fig. 1a),但對于N-N軸手性骨架構建目前卻較少有相關的研究報道(Fig. 1b)。目前,N-N軸手性骨架構建主要涉及四類反應,即阻轉選擇性N-H官能團化、去對稱化、從頭合成和C-H官能團化反應。然而,對于N-N軸手性骨架構建的高效且簡便的合成方法,仍有待進一步探索。近日,鄭州大學牛俊龍與楊丹丹團隊報道了一種鈷/Solox催化阻轉選擇性C-H活化/環化反應,高效構建了一系列N-N軸手性骨架,具有良好的官能團兼容性、溫和的反應條件、優異的收率以及對映選擇性等特點(Fig. 1c)。下載化學加APP到你手機,更加方便,更多收獲。
(圖片來源:Nat. Commun.)
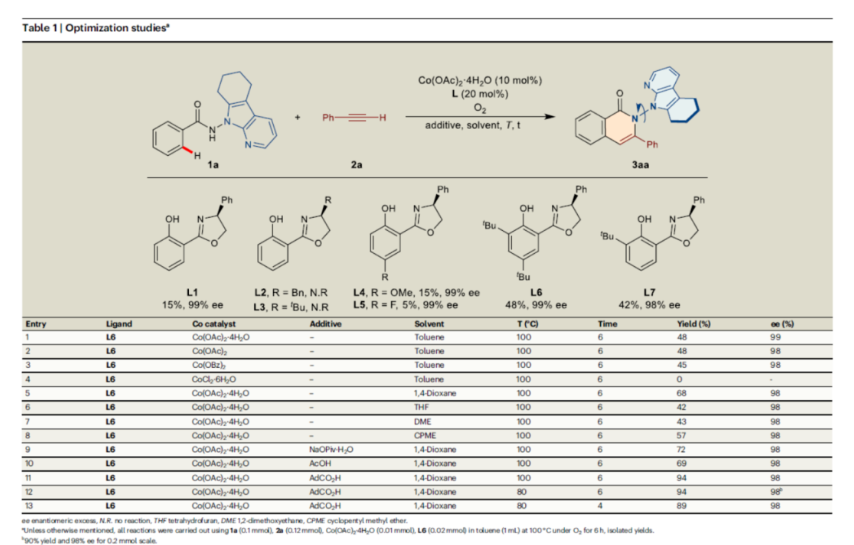
首先,作者以N-(7-氮雜吲哚)苯甲酰胺1a與苯乙炔2a作為模型底物,進行了相關反應條件的篩選(Table 1)。當以Co(OAc)2·4H2O(10 mol %)作為催化劑,L6(20 mol %)作為配體,O2作為氧化劑,AdCO2H(1.0 equiv)作為添加劑,在1,4-二氧六環溶劑中80 oC反應6 h,可以94%的收率得到產物3aa,ee為98%。
(圖片來源:Nat. Commun.)
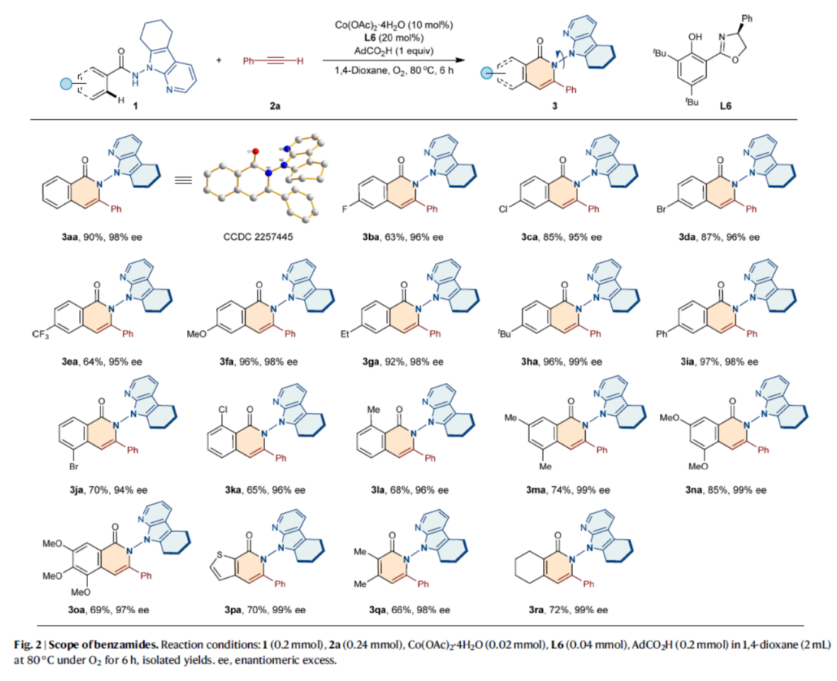
在獲得上述最佳反應條件后,作者對苯甲酰胺類的底物范圍進行了擴展(Fig. 2)。首先,苯甲酰胺底物的芳基上含有不同電子性質的取代基時,均可順利反應,獲得相應的產物3aa-3oa,收率為63-97%,ee為94-99%。值得注意的是,含有噻吩基取代的雜環底物1p,也是合適的底物,可以70%的收率和99% ee得到產物3pa。其次,具有挑戰性的乙烯酰胺1q和1r,也能夠順利進行反應,獲得相應的產物3qa-3ra,收率為66-72%,ee為98-99%。
(圖片來源:Nat. Commun.)
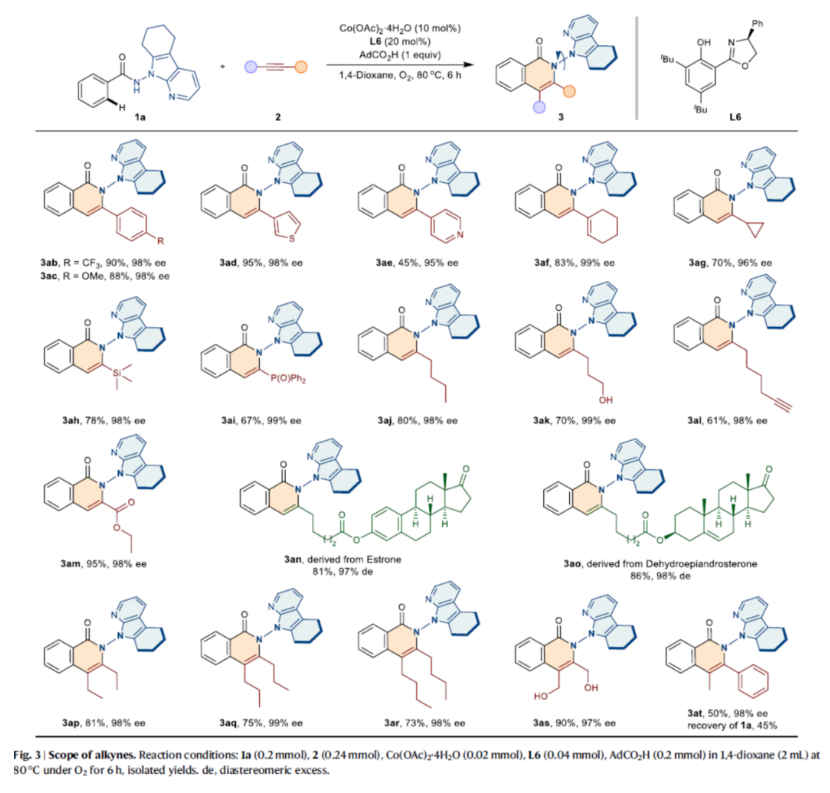
緊接著,作者對炔烴的底物范圍進行了擴展(Fig. 3)。首先,乙炔的末端含有芳基、雜芳基、環烷基、硅基、烷基、烷氧羰基等時,均可順利反應,獲得相應的產物3ab-3am,收率為45-95%,ee為95-99%。值得注意的是,該策略還可用于天然產物的后期修飾,獲得相應的產物3an-3ao,收率為81-86%,de為97-98%。其次,對于對稱的脂肪族內炔烴,也能夠順利反應,獲得相應的產物3ap-3as,收率為73-90%,ee為97-99%。此外,對于非對稱內炔烴底物,可以50%的收率和98% ee得到產物3at。
(圖片來源:Nat. Commun.)
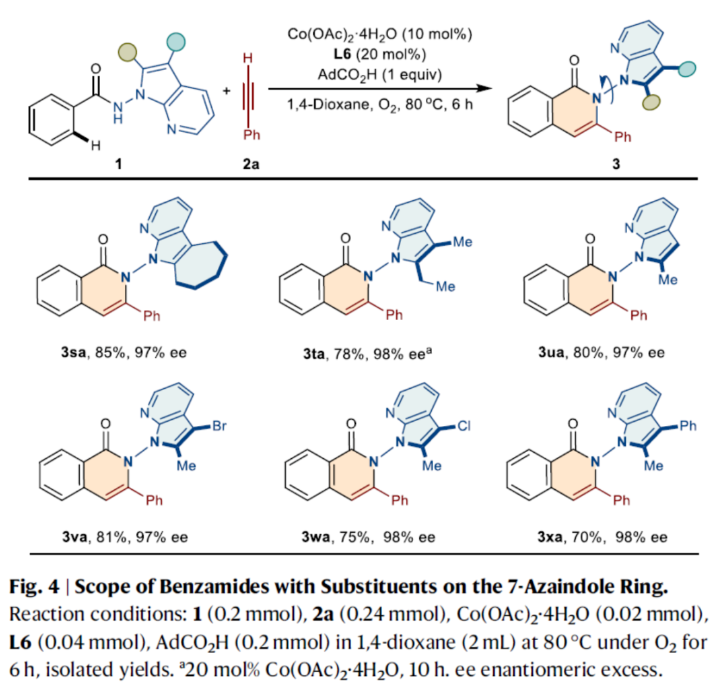
隨后,作者對底物1中7-氮雜吲哚環上取代基的范圍進行了擴展(Fig. 4)。研究表明,含有環己烷、2-乙基、2-甲基取代的氮雜吲哚底物,均可順利反應,獲得相應的產物3sa-3ua,收率為78-85%,ee為97-98%。同時,在氮雜吲哚環C2-和C3-位含有不同官能團的苯甲酰胺,也能夠順利進行反應,獲得相應的產物3va-3xa,收率為70-81%,ee為97-98%。
(圖片來源:Nat. Commun.)
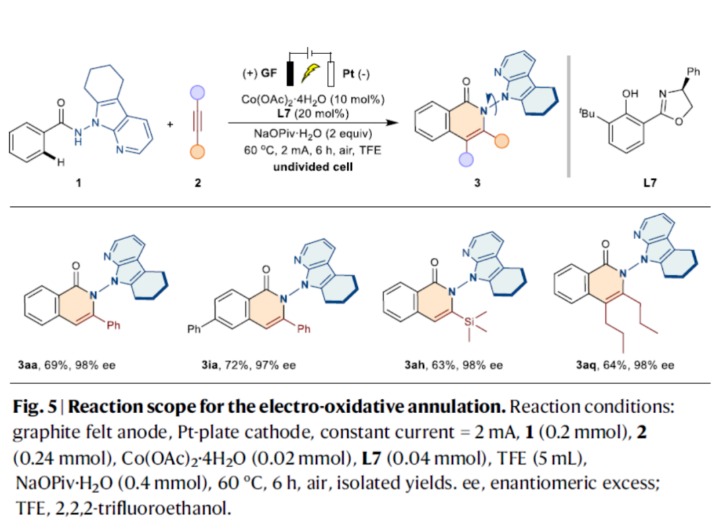
為了進一步提高反應的實用性,作者進行了相關的電化學實驗(Fig. 5)。研究結果表明,在該電化學條件下,同樣可獲得所需的產物3aa、3ia、3ah和3aq,收率為63-69%,ee為97-98%。
(圖片來源:Nat. Commun.)
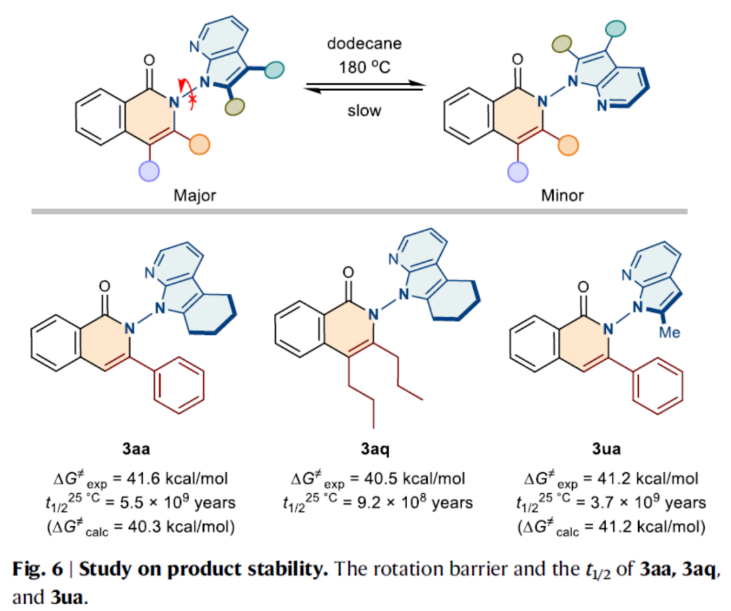
此外,作者還對產物的穩定性進行了研究(Fig. 6)。研究結果表明,N-N軸手性異喹啉酮具有高度的阻轉穩定性。
(圖片來源:Nat. Commun.)
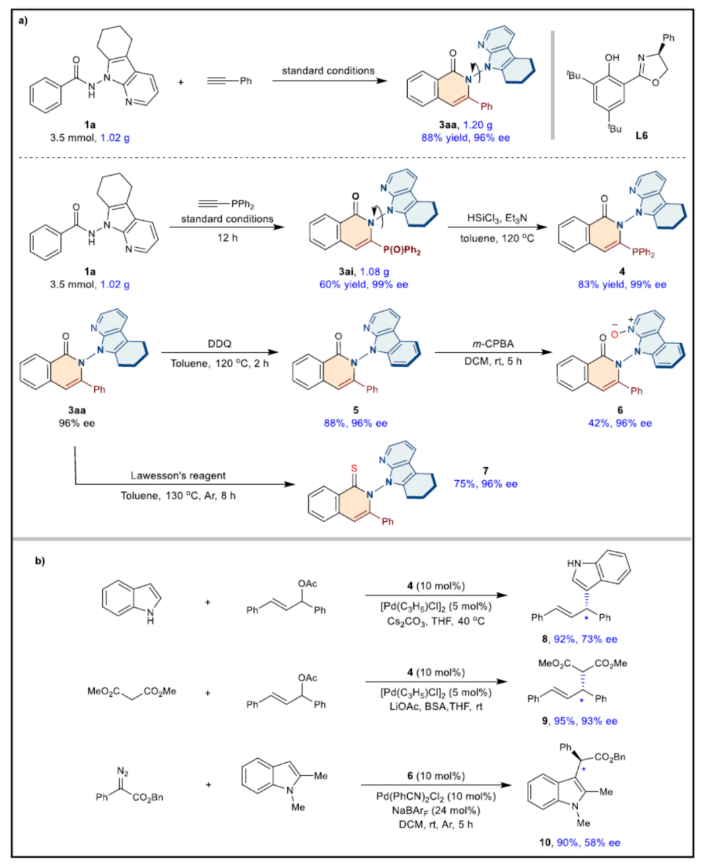
隨后,作者對反應的實用性進行了研究(Fig. 7)。首先,克級規模實驗,同樣能夠以88%收率和96%ee得到產物3aa以及以60%收率和99%ee得到產物3ai。其次,3ai經還原反應,可以83%收率和99%ee得到單膦產物4。3aa經氧化反應,可以88%收率和96%ee得到化合物5。化合物5在m-CPBA條件下進行反應,可以42%收率和96%ee得到N-氧化物6。3aa與Lawesson’s試劑反應,可以75%收率和96%ee得到硫代化合物7。此外,合成的產物4和6可作為合適的手性配體,并可用于不對稱鈀催化的吲哚烯丙基取代反應、Tsuji-Trost反應等,獲得相應的化合物8-10,收率為90-95%,ee為58-93%。

(圖片來源:Nat. Commun.)
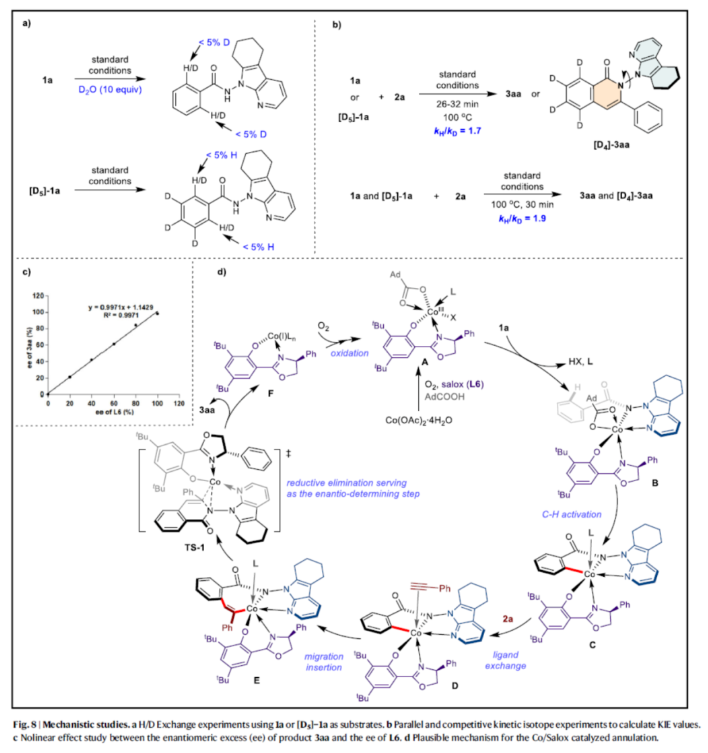
最后,作者還對反應機理進行了進一步的研究(Fig. 8)。H/D交換實驗結果表明,C-H鍵的斷裂是不可逆的(Fig. 8a)。KIE實驗結果表明,C-H鍵的斷裂可能參與了決速步驟(Fig. 8b)。產物3aa的ee和L6的ee之間的非線性效應研究表明,單個手性配體與鈷原子配位以生成有效的催化劑(Fig. 8c)。基于上述的研究以及相關文獻的查閱,作者提出了一種合理的催化循環過程(Fig. 8d)。首先,Co(OAc)2·4H2O與L6和AdCO2H配位,并通過O2進行氧化,生成活性Co(III)-配合物A。配合物A與底物1a進行配體交換,生成Co(Ⅲ)-中間體B。中間體B通過C-H鍵的活化,生成關鍵的中間體C。值得一提的是,不能完全排除涉及第一個C-H活化步驟和隨后的氧化步驟以形成中間體C的另一途徑。隨后,炔烴2a與中間體C配位,并通過配體交換生成中間體D。中間體D中的炔基遷移插入到C-Co鍵中,生成中間體E。中間體E通過還原消除,生成N-N軸手性產物3aa以及Co(I)中間體F。值得注意的是,該過程通過過渡態TS-1的還原消除進行,由于L6的苯基與1a的7-氮雜吲哚導向基團之間的π-π堆積相互作用,其具有最低的能量,可以作為對映體的決定步驟。
(圖片來源:Nat. Commun.)
總結
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn