

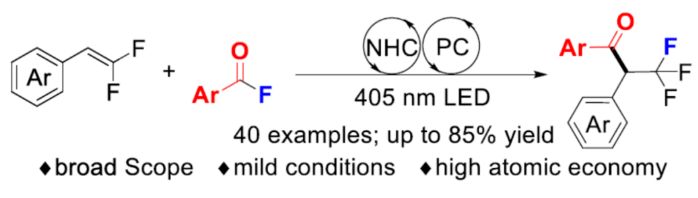
(圖片來源:Angew. Chem. Int. Ed.)
正文
眾所周知,與相應的非氟同源物相比,在有機化合物中引入三氟甲基可以顯著改善其藥代動力學特征。因此,化學家們一直致力于開發可持續和通用的合成含三氟甲基化合物的方法。近年來,α-CF3取代酮是含氟化合物的一個重要亞類,并得到了廣泛的研究。目前,化學家們已開發多種合成α-CF3取代酮的方法(Scheme 1a)。傳統上,通過預形成的硅基烯醇醚或衍生自相應酮的烯醇化物的親電或自由基三氟甲基化反應是合成α-CF3取代酮的常用方法。作為一種替代的策略,Grushin課題組利用CuCF3試劑實現了α-鹵代酮的親核三氟甲基化反應。其次,烯烴或炔烴的氧化三氟甲基化反應已成功應用于α-CF3取代酮的合成。然而,大多數的合成方法都需要過量使用昂貴或敏感的三氟甲基試劑,導致產生大量廢物。同時,利用含有CF3砌塊構建三氟甲基化合物的自由基偶聯方法是另一種互補性的方法。在這種情況下,CF3基團需預先引入至底物中,并且在此過程中不會形成C-F鍵。然而,含有CF3的單元的有限選擇和高成本,從而限制了該方法的通用性。近年來,偕-二氟烯烴可與外部氟化物源進行1,2-雙官能團化反應,實現三氟甲基化合物的合成,涉及自由基、陰離子或陽離子途徑。同時,基于Armido Studer課題組對于NHC催化芳酰基氟化物的反應以及NHC/光氧化還原催化自由基-自由基交叉偶聯反應的啟發,近日,德國明斯特大學Armido Studer課題組報道了一種利用芳酰基氟化物作為雙官能團化試劑,通過協同光氧化還原和NHC催化實現了α-CF3羰基化合物的合成(Scheme 1b)。下載化學加APP到你手機,更加方便,更多收獲。
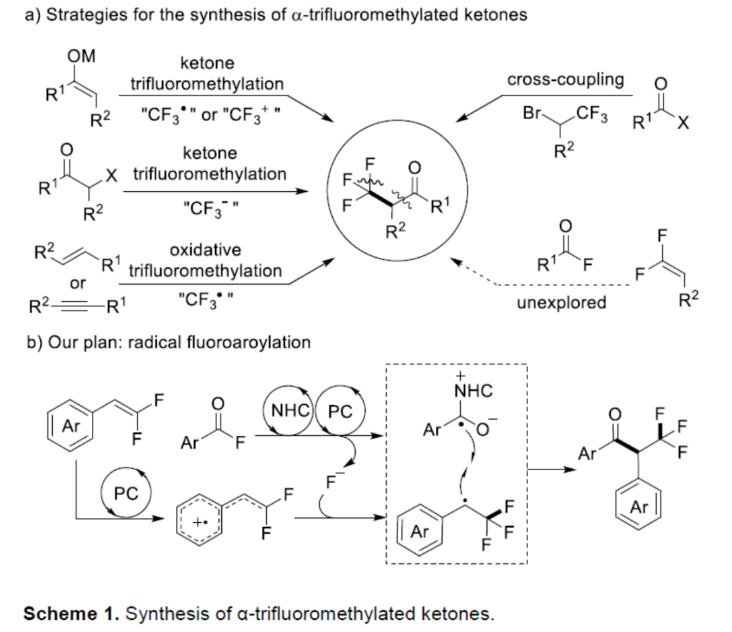
(圖片來源:Angew. Chem. Int. Ed.)
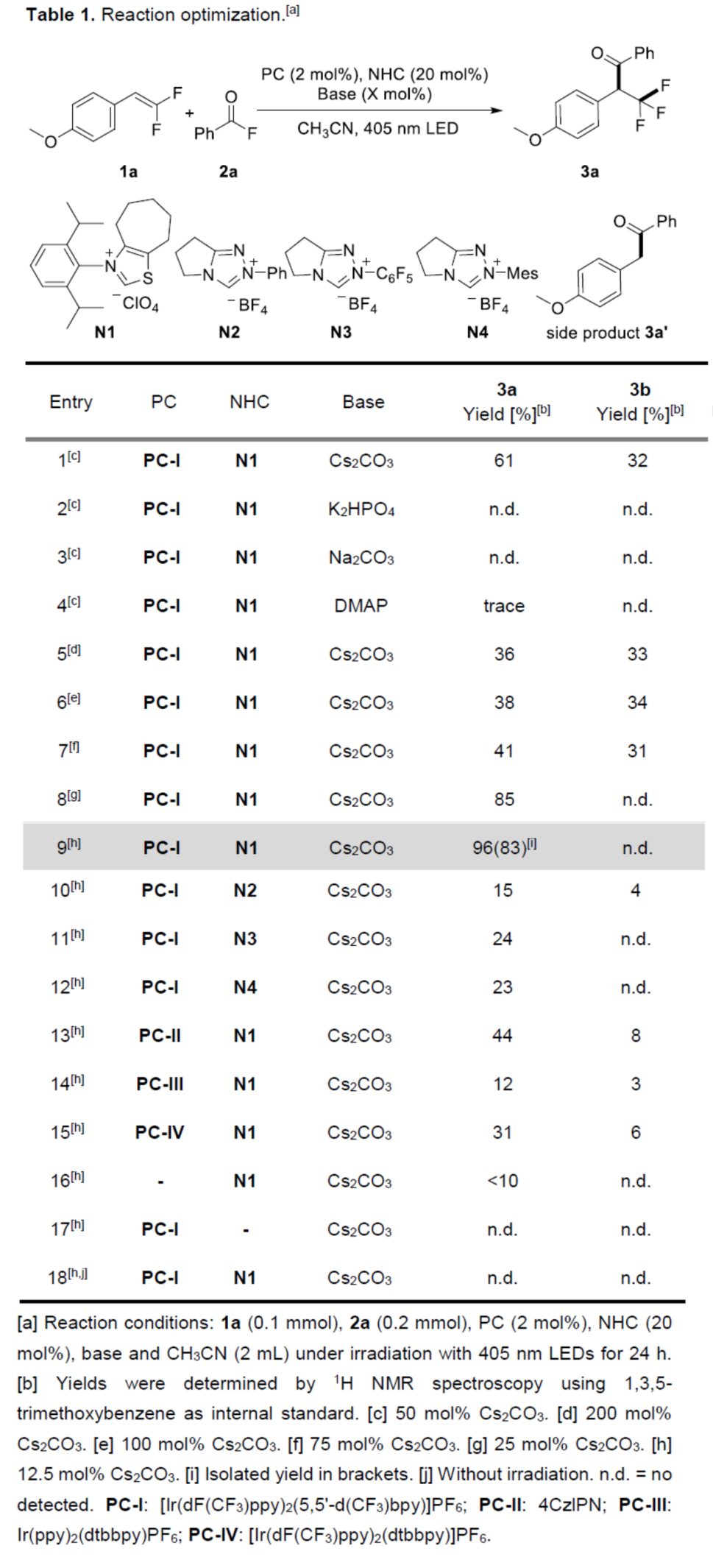
首先,作者以偕-二氟烯烴1a與苯甲酰氟2a作為模型底物,進行了相關反應條件的篩選(Table 1)。當以[Ir(dF(CF3)ppy)2(5,5'-d(CF3)bpy)]PF6 PC-I(2 mol %)作為光催化劑,NHC N1(20 mol %)作為NHC催化劑,Cs2CO3(12.5 mol%)作為堿,405 nm LEDs作為光源,在CH3CN溶劑中反應,可以83%的分離收率得到產物3a。
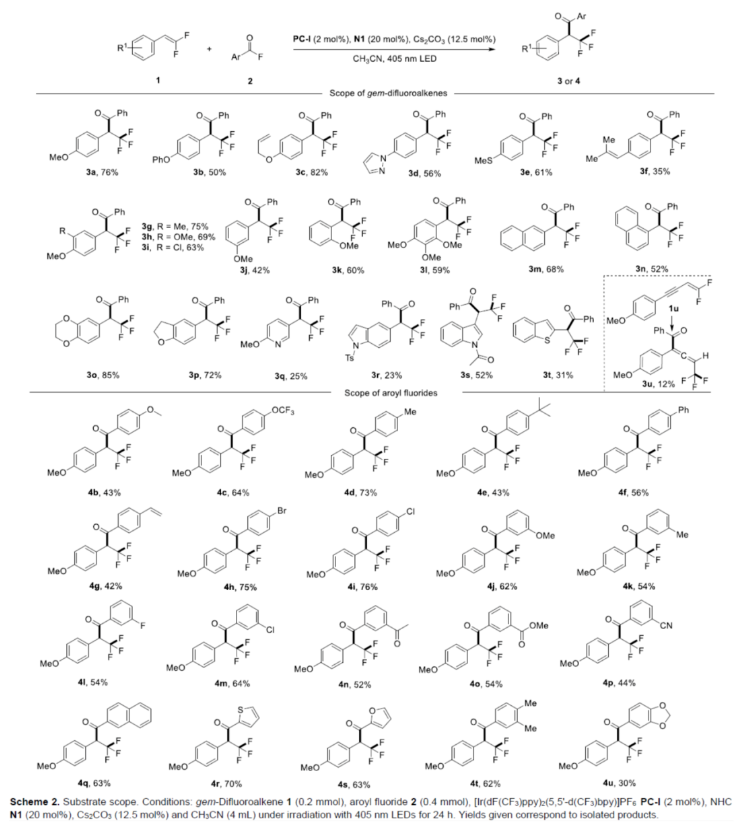
在獲得上述最佳反應條件后,作者對底物范圍進行了擴展(Scheme 2)。首先,當二氟烯烴底物中的芳基上含有烷氧基、吡唑基、烷基硫基、烯基等時,均可順利反應,獲得相應的產物3a-3l,收率為35-82%。然而,在芳環的對位帶有吸電子基團(如氰基、硝基和酰基)的二氟烯烴在該轉化中是不活潑的,因為它們在標準條件下不被氧化。其次,二氟烯烴底物中含有萘基與雜芳基時,也與體系兼容,獲得相應的產物3m-3t,收率為23-85%。同時,烯炔衍生的二氟烯烴1u也是合適的底物,可以12%的收率得到產物3u。此外,甲酰氟底物中含有不同電性取代的芳基、萘基以及雜芳基時,均可順利反應,獲得相應的產物4b-4u,收率為30-73%。然而,脂肪族酰基氟化物,未能有效的進行反應。
(圖片來源:Angew. Chem. Int. Ed.)
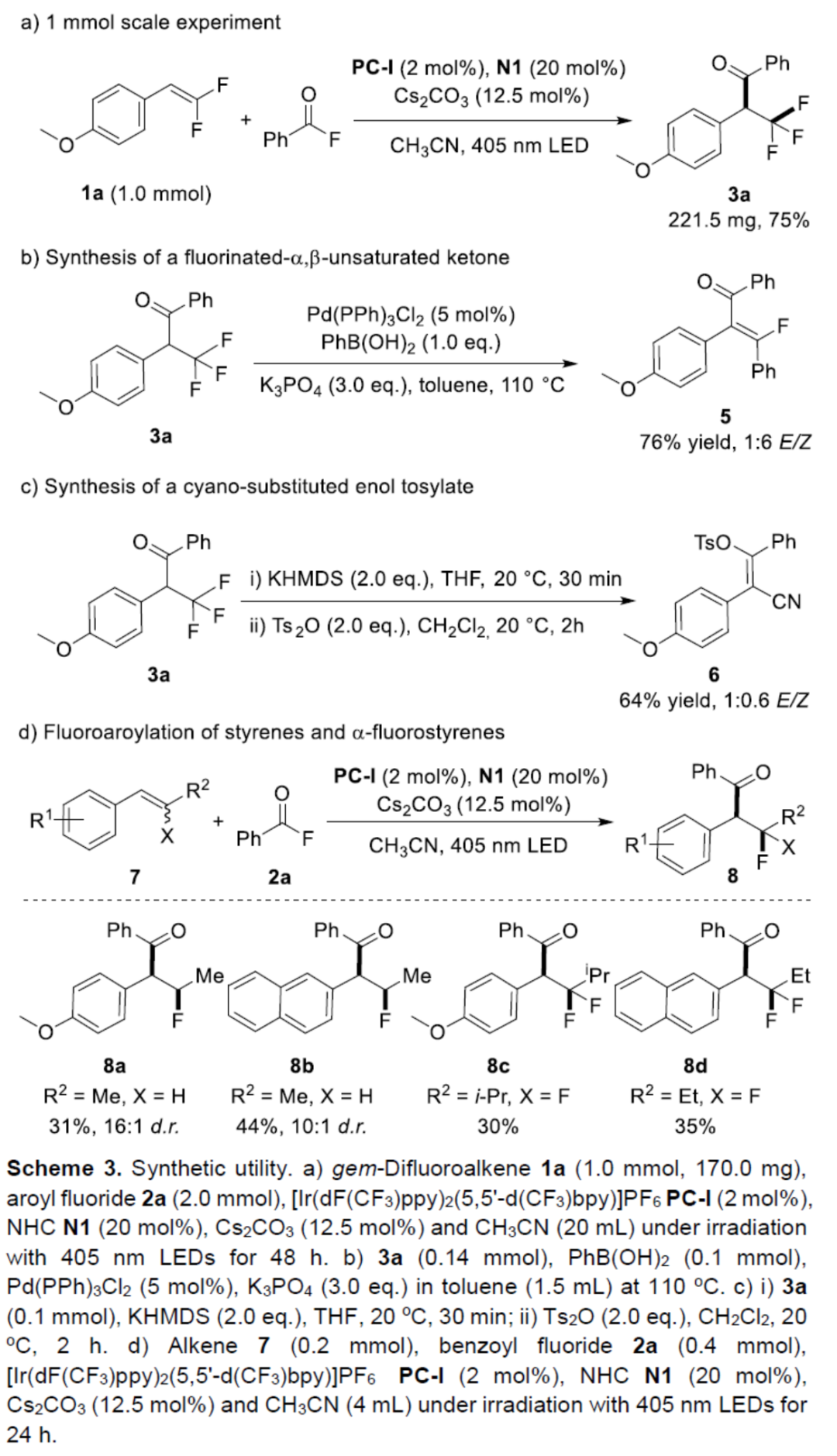
緊接著,作者對反應的實用性進行了研究(Scheme 3)。首先,將反應規模放大至1 mmol時,同樣能夠以75%收率得到產物3a(Scheme 3a)。其次,3a與PhB(OH)2在Pd(PPh)3Cl2/K3PO4條件下通過脫氟/芳基化串聯反應,可以76%的收率得到氟化的-α,β-不飽和酮5,E/Z為1:6(Scheme 3b)。3a在KHMDS/THF以及Ts2O/CH2Cl2條件下反應,可以64%的收率得到氰基取代的烯醇甲苯磺酸酯6,E/Z為1:0.6(Scheme 3c)。此外,簡單的苯乙烯以及α-氟苯乙烯衍生物,也能夠與2a順利進行氟代芳酰化反應,獲得相應的產物8a-8d,收率為30-44%(Scheme 3d)。
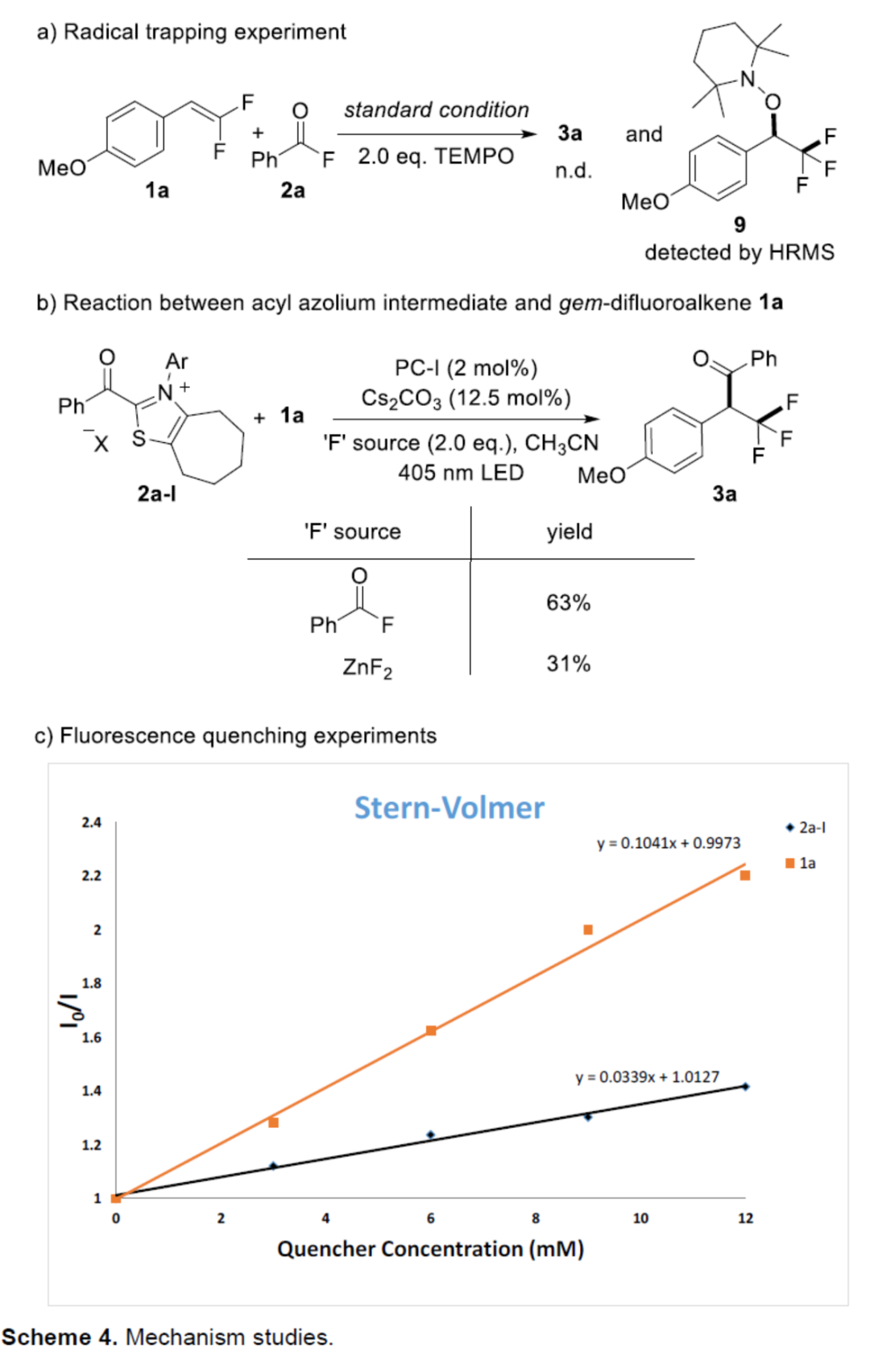
隨后,作者還對反應機理進行了進一步的研究(Scheme 4)。首先,自由基捕獲實驗結果表明,α-三氟甲基芐基自由基作為中間體參與了反應(Scheme 4a)。其次,酰基唑鎓離子中間體2a-l與偕-二氟烯烴1a的對照實驗結果表明,酰基唑鎓離子2a-l是反應的有效中間體(Scheme 4b)。此外,Stern-Volmer熒光淬滅實驗結果表明,底物1a和酰基唑鎓離子2a-I可以淬滅光催化劑PC-I的激發態。然而,發現1a的淬滅效率明顯高于2a-I(Scheme 4c)。
(圖片來源:Angew. Chem. Int. Ed.)
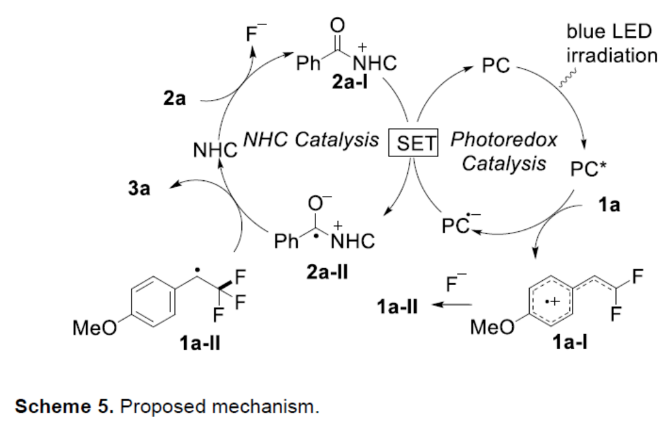
基于上述的研究以及相關文獻的查閱,作者提出了一種合理的催化循環過程(Scheme 5)。首先,光激發的Ir(III)*催化劑可對偕-二氟烯烴1a進行可見光誘導的SET氧化,生成相應的自由基陽離子1a-I以及還原的Ir(II)-配合物。然后,中間體1a-I可被氟陰離子區域選擇性地捕獲,生成芐基自由基1a-II。考慮到兩個氟原子的誘導作用和芐基自由基的穩定性,可以解釋反應的區域選擇性。同時,芳酰基氟化物2a與NHC催化劑的反應生成酰基唑鎓離子2a-I,其用還原的光氧化還原催化劑Ir(II)進行SET還原以再生基態Ir(III),并形成烯酮型自由基2a-II。最后,由持續自由基效應控制的烯酮基自由基2a-II與芐基自由基1a-II的交叉偶聯以及隨后是NHC斷裂,從而生成目標產物3a,并關閉NHC催化循環。
(圖片來源:Angew. Chem. Int. Ed.)
總結
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn