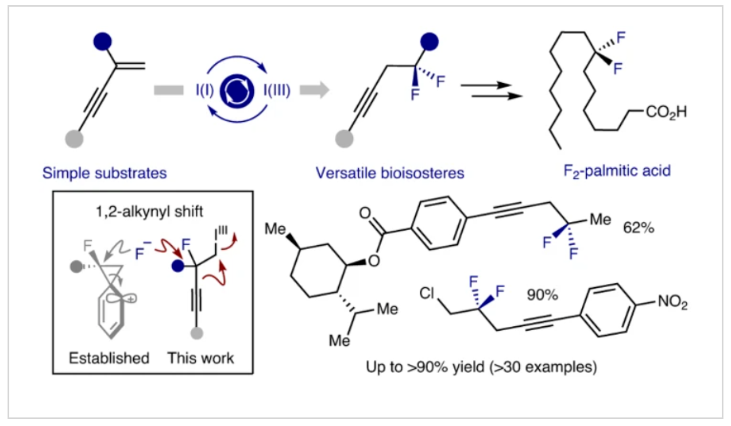
氟化小分子在功能小分子中普遍存在,但其天然來源較為缺乏,這為創(chuàng)造性地開發(fā)獲取這些重要材料的途徑創(chuàng)造了機(jī)會(huì)。I(I)/I(III)催化是構(gòu)建氟化產(chǎn)物的重要途徑,其使用簡單易得的烯烴被原位形成的λ3-碘烷捕獲,從而實(shí)現(xiàn)高價(jià)值的(二)氟化產(chǎn)物的合成。此類有機(jī)催化模式通常通過π鍵的參與來模擬基于金屬的反應(yīng)過程。以苯乙烯為例,其可以促進(jìn)氟化的苯橋正離子(phenonium-ion)重排從而構(gòu)建二氟乙烯基骨架。最近,德國明斯特大學(xué)Ryan Gilmour課題組證明了烯炔是苯乙烯的有效替代品,從而減弱了對(duì)芳基取代基的需求,并能夠以操作簡單的方式生成多樣的高炔丙基二氟化物(Fig. 1)。下載化學(xué)加APP到你手機(jī),更加方便,更多收獲。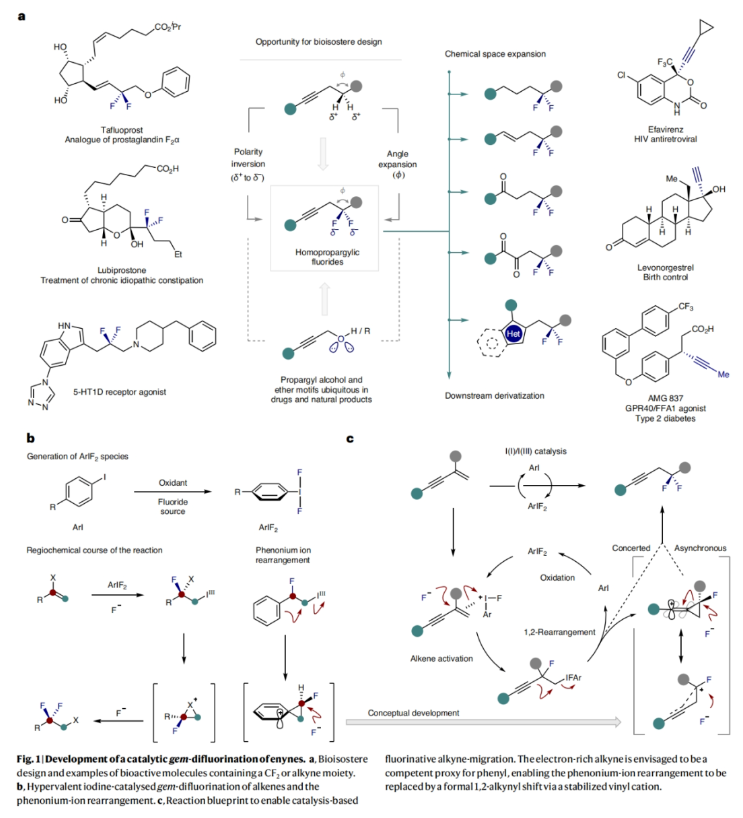
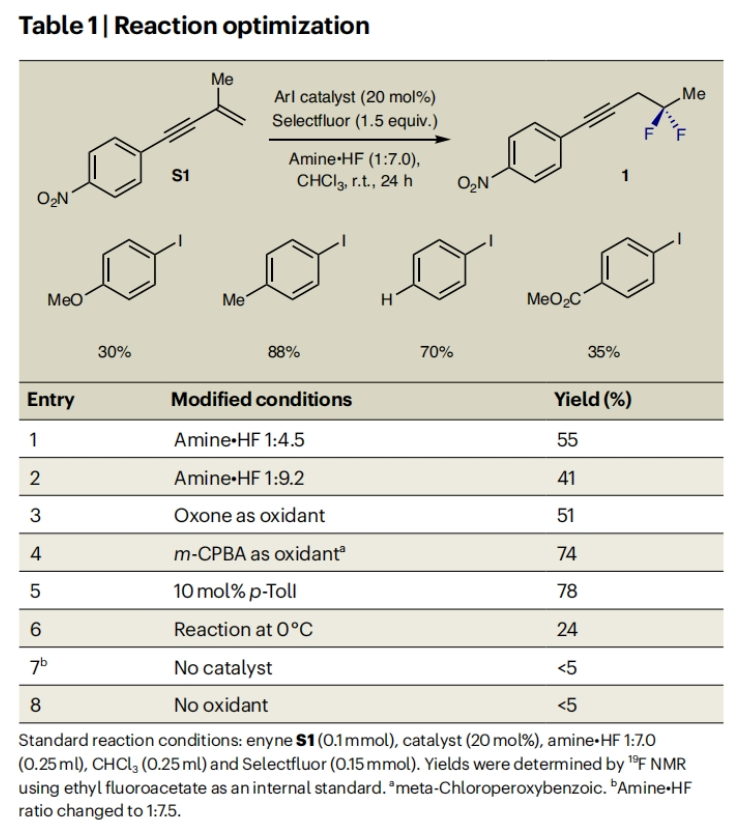
首先,作者選擇烯炔S1作為模板底物對(duì)反應(yīng)條件進(jìn)行了優(yōu)化,當(dāng)使用對(duì)甲基碘苯p-TolI, (20 mol%), Selectfluor (1.5 equiv), amine?HF (1:7.0),在CHCl3中室溫反應(yīng)24小時(shí)可以以88%的產(chǎn)率得到高炔丙基二氟化物1(Table 1)。隨后,作者對(duì)此轉(zhuǎn)化的底物范圍進(jìn)行了考察(Table 2)。實(shí)驗(yàn)結(jié)果表明,一系列不同芳基取代的烯炔底物均可兼容此轉(zhuǎn)化,以42-91%的產(chǎn)率得到相應(yīng)的產(chǎn)物2-19,且產(chǎn)物2的結(jié)構(gòu)通過X-射線單晶衍射得到了證實(shí)。值得注意的是,此轉(zhuǎn)化對(duì)一系列生物活性分子骨架如L-menthol、dihydrocholesterol、estrone等均可兼容,證明了此轉(zhuǎn)化的良好兼容性。此外,烯炔底物中的R基還可以變換為CH2X(X= Br, Cl)(15, 91%;16, 90%)。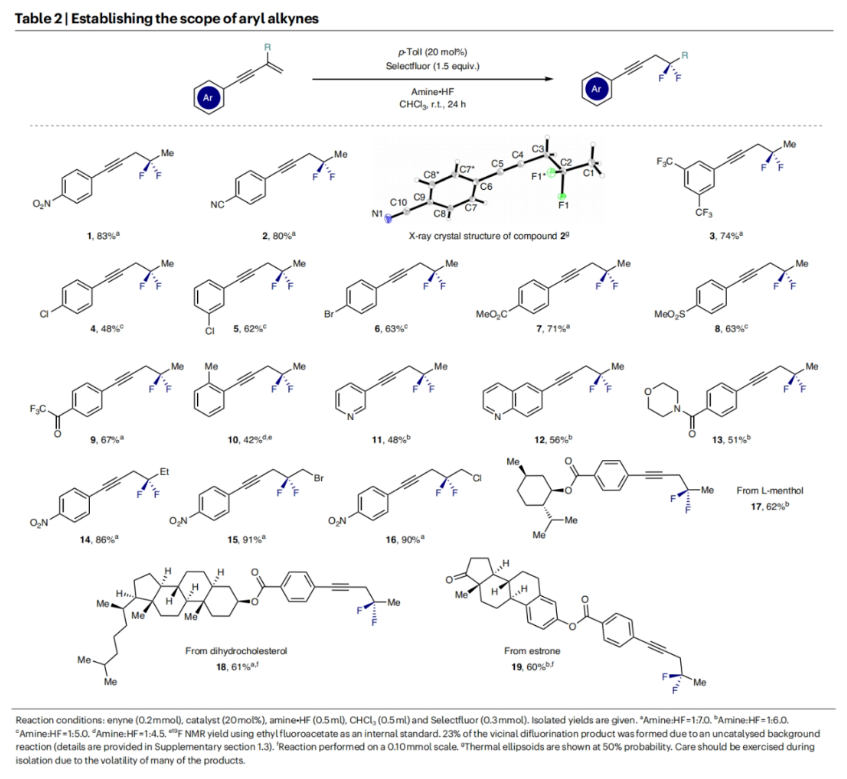
接下來,作者探索了烷基取代和硅基取代炔烴的兼容性(Table 3)。實(shí)驗(yàn)結(jié)果表明,烯炔底物中不同類型的烷基取代均可兼容,以41-71%的產(chǎn)率得到相應(yīng)的高炔丙基二氟產(chǎn)物20-32。值得注意的是,此轉(zhuǎn)化對(duì)治療痛風(fēng)的藥物Febuxostat衍生的烯炔底物同樣具有良好的普適性,以55%的產(chǎn)率得到產(chǎn)物32。此外,硅基取代的炔烴同樣可以兼容,以67%的產(chǎn)率得到產(chǎn)物33,其后續(xù)可以通過脫去炔上的硅保護(hù)基得到相應(yīng)的端炔產(chǎn)物。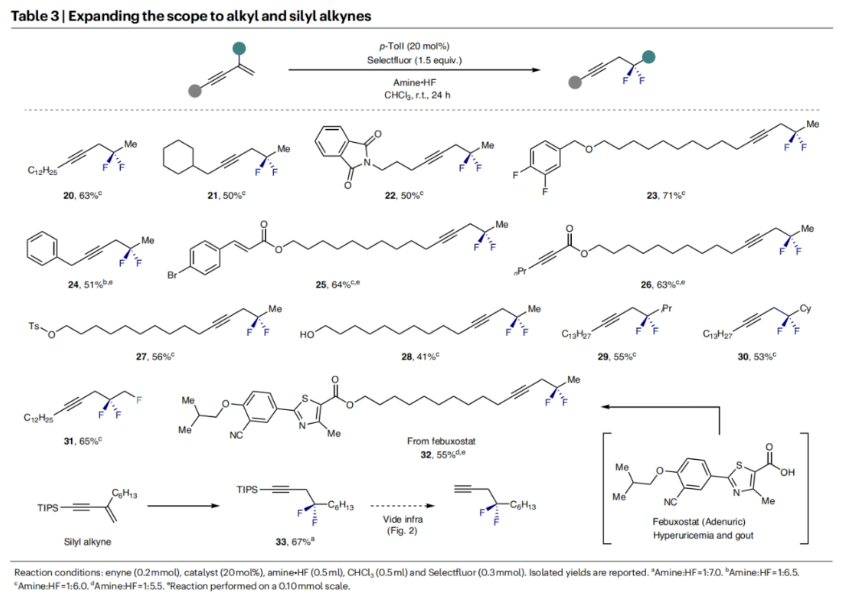
為了證明此轉(zhuǎn)化的實(shí)用性,作者首先進(jìn)行了規(guī)模化實(shí)驗(yàn)(Fig. 2a)。當(dāng)分別使用S4和S20作為起始原料,在4.0 mmol規(guī)模下反應(yīng)可以分別以49%(51%)和50%(62%)的產(chǎn)率得到相應(yīng)的產(chǎn)物4和20。隨后,作者對(duì)合成的出的產(chǎn)物進(jìn)行了一系列衍生化(Fig. 2b),包括:1)炔烴產(chǎn)物20可以被全部還原或部分還原,以80%和63%的產(chǎn)率得到相應(yīng)的烷烴產(chǎn)物34和烯烴產(chǎn)物35(Z:E = 87:13);2)產(chǎn)物4可以通過Ru-催化炔烴的氧化以及與鄰苯二胺的縮合以58%的產(chǎn)率得到喹喔啉產(chǎn)物36;3)產(chǎn)物33可以通過與TBAF(tetrabutylammonium fluoride)反應(yīng)脫硅基,以85%的產(chǎn)率得到端炔產(chǎn)物37,而37則可以通過銅催化的click反應(yīng)以98%的產(chǎn)率實(shí)現(xiàn)三唑產(chǎn)物38的合成;4)產(chǎn)物33經(jīng)歷原位脫硅基保護(hù)以及與Sonogashira偶聯(lián)反應(yīng)串聯(lián)以64%的產(chǎn)率得到富電子芳炔產(chǎn)物39;5)產(chǎn)物6可以經(jīng)歷Suzuki–Miyaura偶聯(lián),以93%的產(chǎn)率得到產(chǎn)物40。接下來,作者利用烯炔41作為起始原料,通過所發(fā)展的區(qū)域選擇性1,1-二氟化反應(yīng)(42,51%)、化學(xué)選擇性還原以及皂化反應(yīng)(44, 98%)以三步50%的產(chǎn)率得到CF2-修飾的棕櫚酸(palmitic acid)(Fig. 2c)。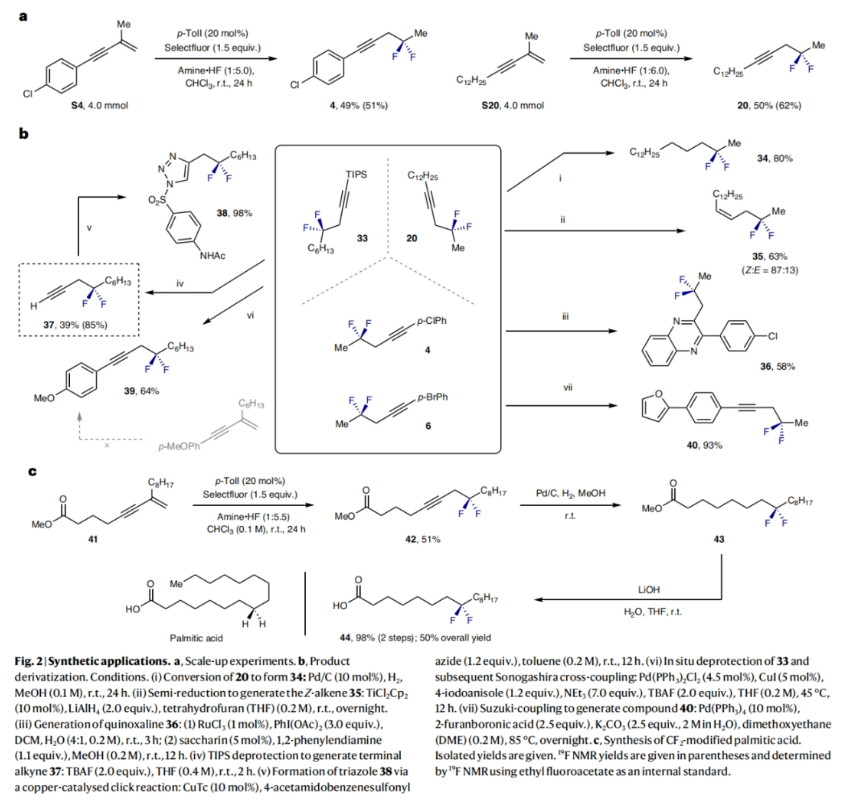
緊接著,為了對(duì)此反應(yīng)有更深入的了解,作者進(jìn)行了一系列控制實(shí)驗(yàn)(Fig. 3)。首先,在移除烯炔底物中的烷基取代基時(shí),反應(yīng)仍可進(jìn)行,分別以60%和55%的產(chǎn)率得到高炔丙基二氟產(chǎn)物46和48。值得注意的是,分子內(nèi)的二氟甲基可以作為伯醇的生物電子等排體,因此可以利用此類產(chǎn)物的供氫特性對(duì)分子進(jìn)行設(shè)計(jì)(Fig. 3a)。接下來,作者將取代基轉(zhuǎn)換為對(duì)三氟甲基苯基來探索反應(yīng)的區(qū)域選擇性。當(dāng)使用烯炔49反應(yīng)時(shí),可以以40%的產(chǎn)率專一的得到產(chǎn)物50,這與1,2-移位競(jìng)爭(zhēng)苯橋正離子重排相一致(Fig. 3b)。最后,作者通過氘代實(shí)驗(yàn)證明了反應(yīng)中經(jīng)歷了1,2-炔基遷移過程(Fig. 3c)。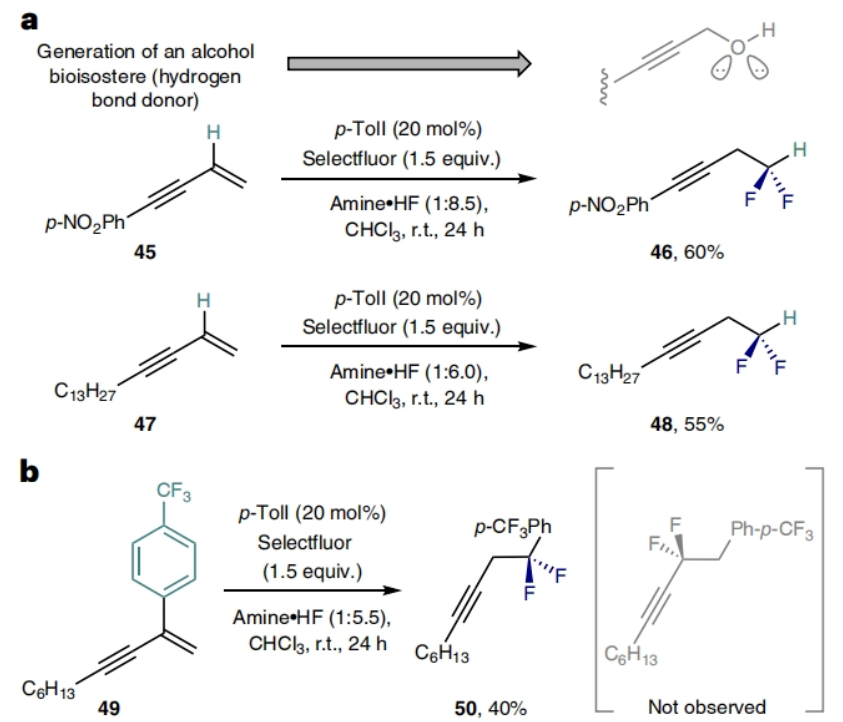
Ryan Gilmour課題組利用烯炔作為起始原料,通過I(I)/I(III)催化實(shí)現(xiàn)了一系列高炔丙基二氟化物的合成。該轉(zhuǎn)化展現(xiàn)了良好的底物適用性和官能團(tuán)兼容性。通過產(chǎn)物的進(jìn)一步衍生化,可以實(shí)現(xiàn)包括CF2-修飾的棕櫚酸在內(nèi)的一系列衍生物的合成。此反應(yīng)的發(fā)展有望在新藥研發(fā)中得到廣泛的應(yīng)用。 文獻(xiàn)詳情:
Zi-Xuan Wang, Keith Livingstone, Carla Hümpel, Constantin G. Daniliuc, Christian Mück-Lichtenfeld, Ryan Gilmour*. Regioselective, catalytic 1,1-difluorination of enynes. Nat. Chem. 2023, https://doi.org/10.1038/s41557-023-01344-5.