

隨著分子生物學技術的發展和人類基因組計劃的完成,發現了大量可供研究的新型分子靶點,但并不是所有的靶點都與疾病發展進程相關,在新藥研發的過程中靶點的選擇與驗證至關重要,也是新藥創新的前提和保障。雖然對于疾病發生的生物學機制研究發展迅速,但是新藥靶點的發現仍然是一項高成本且費時費力的過程。
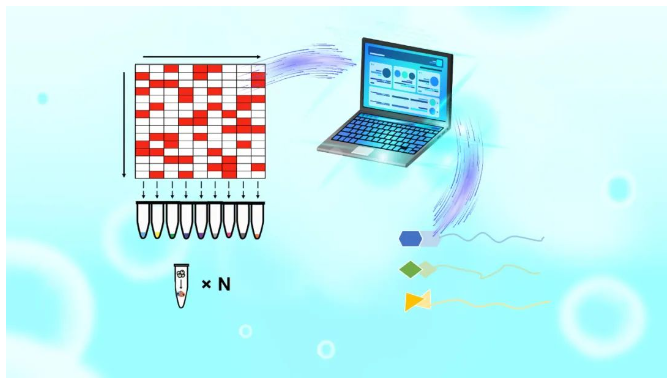
針對上述問題,陳順興領導的團隊開發了一種高通量混合策略,稱為矩陣增強池策略(MAPS)。這一策略包括優化混合物中多種藥物的排列,并以數學方法處理混合物以同時描述每種藥物的靶標(圖1)。該技術包括三個主要步驟: 1)優化藥物的排列以確保組間高度正交性,每個組中的化合物數量相似或相等,每個化合物至少在三個組中存在; 2)基于排列矩陣創建測試藥物的多個混合系統,并使用iTSA單溫點加熱獲得蛋白質熱穩定性轉換結果; 3)分析質譜法結果以確定藥物靶標。
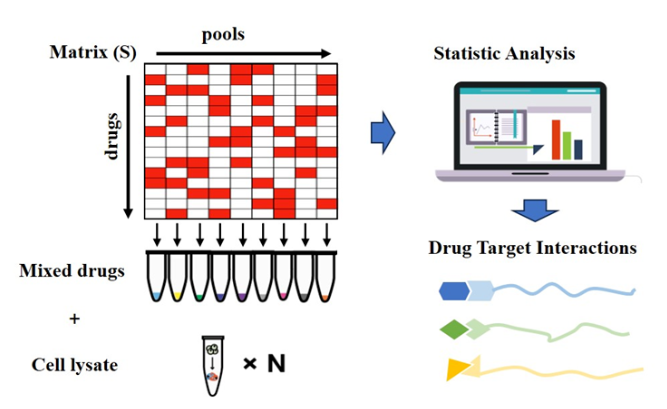
圖1 MAPS流程示意圖
研究人員通過15種藥物的熱蛋白質組分析(TPP)測試驗證了這一策略。該策略使得實驗通量增加了60倍并降低了90%的成本,這對于大規模篩選藥物靶點提供了良好的方法途徑。通過在K562、MCF7、HEK293T、HCT116、HepG2五種細胞系進行同樣一組MAPS實驗,其中包括5種作用機制模糊的潛在脫靶藥物。MAPS-iTSA分析揭示了不同細胞系藥物-靶標的相互作用親和力不同(圖2),通過對不同細胞系的數據分析得到了這些藥物的許多新的潛在脫靶點。
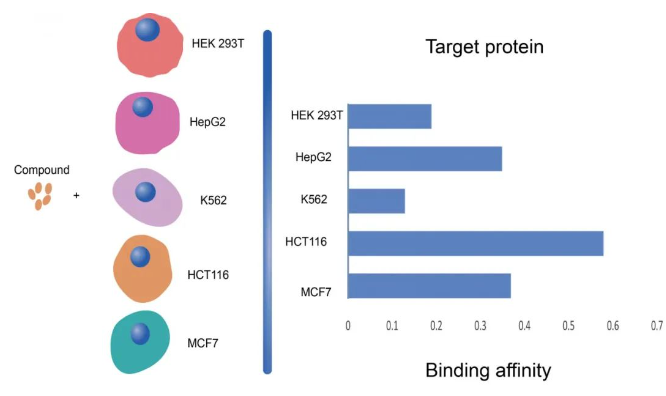
圖2 不同細胞系藥物-靶標的相互作用親和力不同
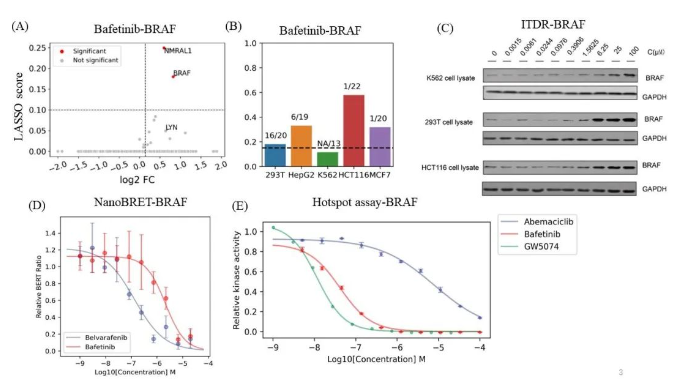
圖3 脫靶解釋和驗證
A.巴非替尼藥物的靶點火山圖。B.不同細胞系中Bafetinib-BRAF的親和力。C. 不同細胞系中Bafetinib-BRAF的劑量依賴性免疫印跡圖。d. NanoBERT細胞內脫靶Bafetinib-BRAF劑量反應曲線。e. Bafetinib-BRAF體外脫靶驗證的激酶活性劑量反應曲線。
研究人員分析表明,針對BCR-ABL和LYN治療淋巴細胞白血病的實驗性藥物巴非替尼(Bafetinib)可以結合BRAF。并且在不同的細胞系中Bafetinib-BRAF的親和力不同,通過ITDRFCETSA(等劑量依賴曲線)驗證得到與質譜數據相匹配的結果。經過NanoBRET(細胞內激酶檢測)及Kinase hotspot assay(放射性同位素標記ATP法)驗證了BRAF可能是巴非替尼的潛在靶點(圖3)。除此之外研究人員也同樣驗證了CSNK2A2是阿西貝利的潛在靶點。該策略這對于分析細胞類型的藥物-靶標親和力及大規模篩選藥物靶點提供了良好的方法途徑。
綜上所述,由南方科技大學的陳順興團隊領導的研究在高通量藥物靶標篩選技術方面取得了重要進展,特別是在研究細胞特異性藥物靶標相互作用方面。他們創新的矩陣增強匯集策略(MAPS)為確定藥物靶點提供了一種有價值的方法,并在新藥開發中具有潛在的應用。
南方科技大學化學系博士后紀宏超(現為中國農業科學院深圳農業基因組研究所副研究員)和南方科技大學2019級博士生陸雪為論文共同第一作者,陳順興為第一通訊作者,南科大為論文第一單位。合作單位還包括美國加州大學、牛津大學納菲爾德醫學院。該研究得到了深圳市科技創新委員會基金項目和國家自然科學基金委員會的支持。
論文鏈接:https://doi.org/10.1016/j.chembiol.2023.08.002
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn