

(圖片來源:Adv. Funct. Mater)
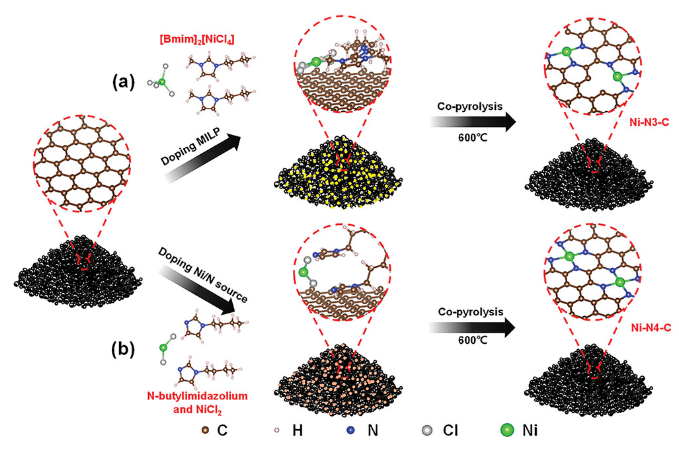
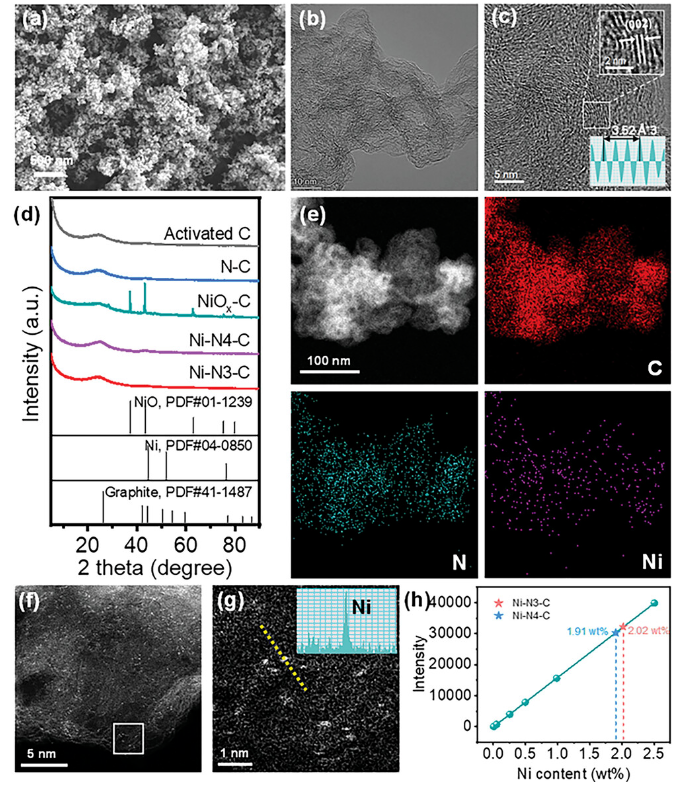
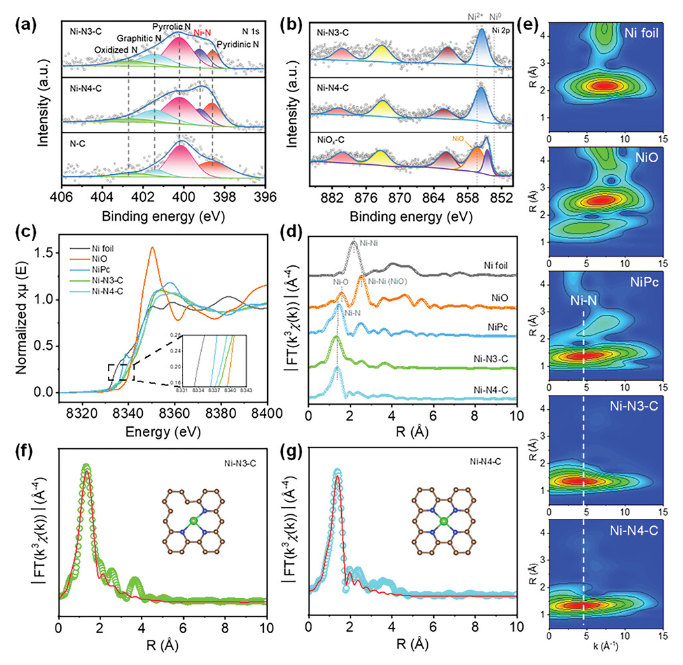
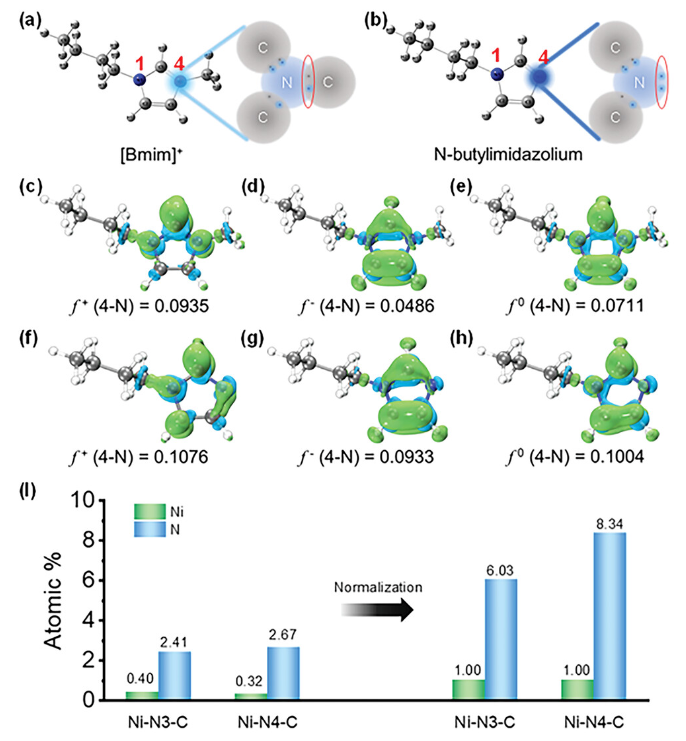
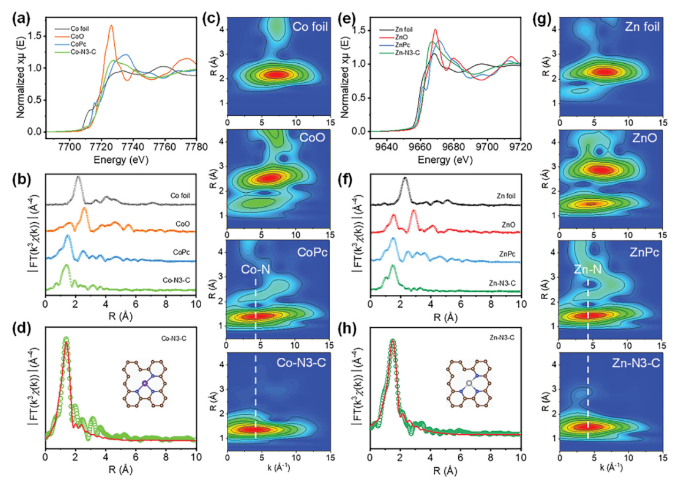
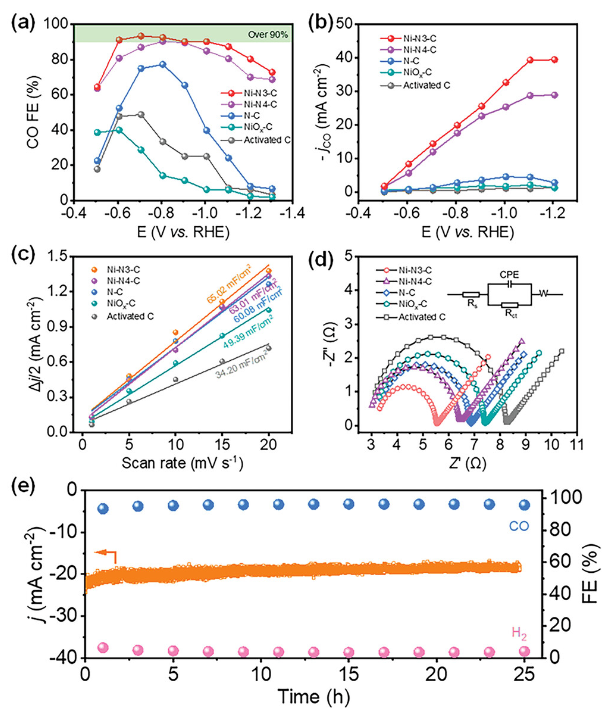
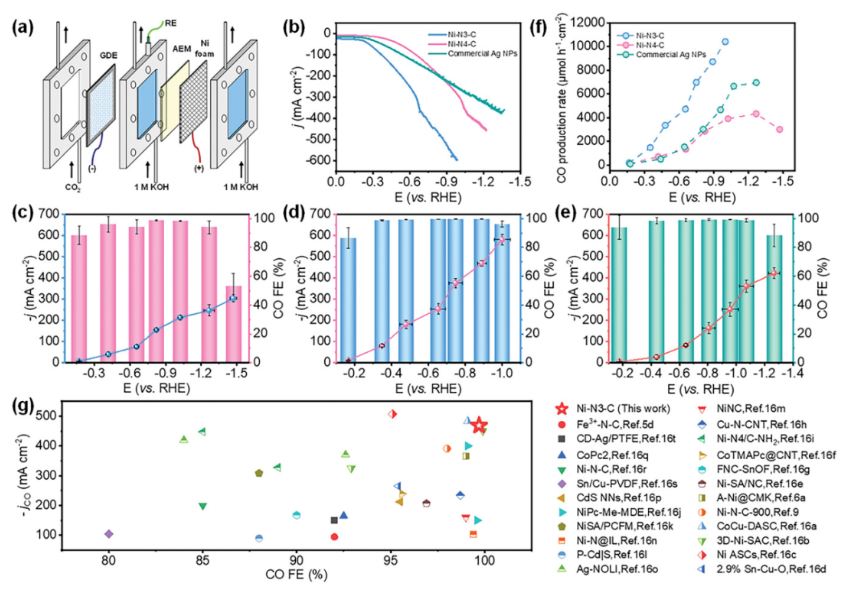
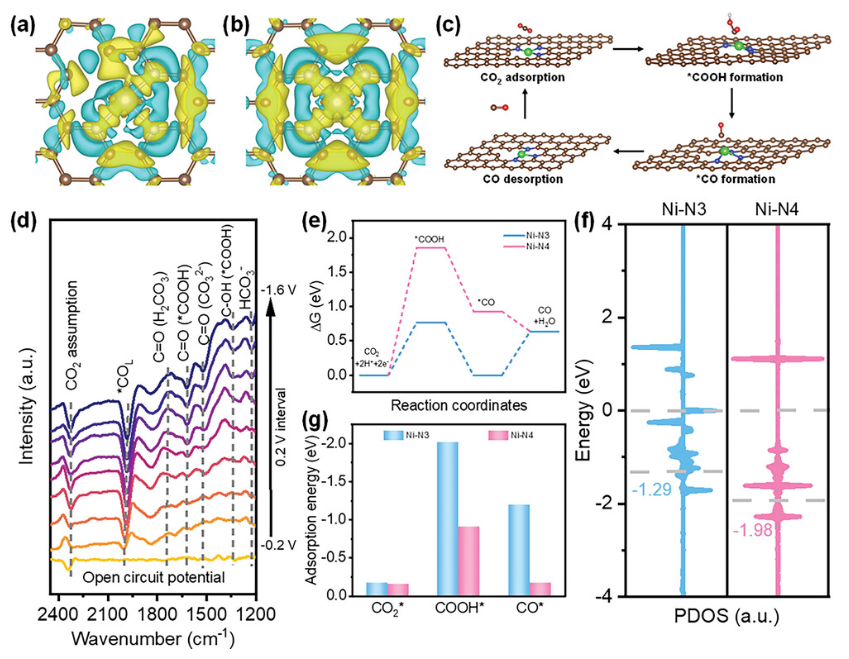
正文 如圖1所示,作者制備了兩種Ni SACs,其中[Bmim]2[NiCl4]的MILPs和N-丁基咪唑和NiCl2·6H2O的非MILPs分別與導電炭黑(CB)充分摻雜并進一步共熱解得到Ni-N3 SACs (記為Ni-N3-C)和Ni-N4 SACs (記為Ni-N4-C)。 圖1. 不同配位環境(Ni-NX)的SACs的合成工藝 Ni-N3-C和Ni-N4-C的掃描電子顯微鏡圖像均顯示出珊瑚狀的多孔結構(圖2a),這有利于CO2分子的傳質促進CO2的電還原。透射電子顯微鏡(TEM)圖像(圖2b,c)表明,Ni-N3-C和Ni-N4-C的形貌類似于活性C或N-C,沒有明顯的納米顆粒。同時,圖2d中的X-射線衍射結果表明,NiOX-C的X-射線衍射譜中的主要峰可以被指標化為NiO相,而在其他樣品中只有24.6°和43.4°的峰被檢測到,并歸因于石墨碳的(002)和(100)面。沒有其他衍射峰進一步表明沒有金屬相或團簇。圖2e的能量色散X-射線能譜(EDS)圖譜表明,Ni和N成功地引入到碳基質中,并均勻分布在Ni-N3-C和Ni-N4-C中。作者用像差校正的高角度環形暗場掃描電子顯微鏡對Ni-N3-C和Ni-N4-C進行的原子尺度觀察表明(圖2f),Ni物種在Ni-N3-C中是原子分散的,沒有納米團簇(圖2g)。電感耦合等離子體原子發射光譜(圖2h)分析表明,Ni-N3-C和Ni-N4-C中的Ni含量分別為2.02wt%和1.91wt%。 圖片來源:Adv. Funct. Mater 圖3a中Ni-N3-C、Ni-N4-C和N- C的高分辨率N 1s光譜表明,Ni原子在Ni-N3-C和Ni-N4-C中主要與N原子結合。同時,Ni-N3-C和Ni-N4-C的高分辨Ni 2p譜說明了Ni-N3-C和Ni-N4-C中Ni原子的價態在0 ~ +2之間(圖3b)。圖3c中X-射線吸收光譜(XAS)進一步證實了Ni-N3-C和Ni-N4-C中Ni原子的價態在0 ~ +2之間。如圖3d所示,Ni箔中Ni─Ni鍵在2.17 ?處明顯存在,NiO中Ni─O鍵在1.60 ?處和Ni─Ni鍵在2.55 ?處明顯存在,而Ni-N3-C和Ni-N4-C中Ni─Ni鍵幾乎消失。Ni-N3-C和Ni-N4-C的主峰均位于1.41 ?附近,與Ni─N散射路徑的主峰相對應。小波變換結果(圖3e)證明了Ni SACs的成功制備,因為Ni原子只與N原子成鍵。根據定量EXAFS擬合結果(圖3f、g)發現,非離子液體原料制備的Ni-N4-C中Ni─N配位數約為3.8±0.1,表明孤立的Ni原子與近4倍的N原子配位。而用[Bmim]2[NiCl4]的MILPs制備的Ni-N3-C中的Ni─N配位數僅為3.2±0.2,說明Ni-N3-C中主要由Ni和N原子形成Ni-N3中心。上述結果表明,用MILPs制備的Ni SACs可以降低Ni與N原子之間的配位數,生成以Ni-N3為中心的SACs。 作者對比圖4a,b中的優化結構,[Bmim]+和N-丁基咪唑的陽離子中的4位N原子存在明顯的電子結構差異。在圖4c-h中,[Bmim]+中的電離4位N原子的Fukui函數值比N-丁基咪唑中的降低,表明[Bmim]+中4位N原子的性質更穩定。此外,這兩種SACs中元素的原子含量也進一步證實了上述結論。如圖4i所示,根據Ni原子含量對Ni-N3-C和Ni-N4-C中N原子的原子含量進行歸一化后,Ni-N3-C中的N原子含量(6.03%)僅占Ni-N4-C中的72.30%(8.34%)。結果表明,MILPs策略對1位N原子的親電性幾乎沒有影響,它主要是通過電離[Bmim]+中的4位N原子而不是N-丁基咪唑中的N原子來調節L殼層的電子結構,導致其熱解過程中的親電性和配位活性下降約50%,從而導致N原子含量較低,從而定向合成了以Ni-N3為中心的低配位SACs。 圖5中的XAS精細結構表征證實,Co-N3-C和Zn-N3-C中分別僅存在Co─N或Zn─N鍵,而不存在金屬鍵,這表明SACs的成功合成。在Co-N3-C或Zn-N3-C SACs中,孤立的金屬原子Co或Zn均與三重N原子配位,這意味著MILPs策略對于M-N3中心定向合成SACs具有良好的普適性。總之,MILPs策略為SACs協調環境的調節開辟了一條前所未有的新途徑。 在相同條件下,在H型電池中評估了Ni-N3-C、Ni-N4-C和其他樣品(例如 N-C、NiOx-C和活化C)的eCO2-to-CO性能。結果表明,Ni-N3-C和Ni-N4-C均表現出比N-C、NiOx-C和活化C更好的起始電位,而Ni-N3-C的起始電位較低,且在相應的負電位下,電流響應值比Ni-N4-C更高。此外,如圖6a、b所示,活化C的eCO2-to-CO性能僅為48.8% CO FE,在0.69 V下jCO為0.53 mA·cm?2。Ni-N3-C和Ni-N4-C的CO FE和jCO在不同電勢下均優于其他電催化劑,進一步證實了SACs由于其獨特的中心而具有優異的eCO2-to-CO性能。此外,MILPs制備的Ni-N3-C比Ni-N4-C表現出更好的eCO2-to-CO性能。在圖6c中,Ni-N3-C和Ni-N4-C的ECSA分別為65.02和63.01 mF cm?2,大于其他電催化劑。最重要的是,作者進行了連續25小時的CO2電解實驗來評估Ni-N3 SACs的穩定性(圖6e),發現在長期電解過程中CO FEs穩定保持在90%以上,電流密度沒有明顯衰減。上述結果表明,MILPs策略調制的Ni-N3-C對eCO2-to-CO表現出優異的穩定性。 由于H型電池中CO2供應量低且傳質不良,作者采用配備氣體擴散電極(GDE)的流通池來改善上述困境,并研究了不同濃度的Ni SACs的eCO2-to-CO性能(圖7a)。陰極和陽極均使用1 M KOH作為電解質。CO2進料引入單獨的氣室,并通過GDE直接擴散到催化劑/電解質界面使eCO2-to-CO。具體來說,Ni-N3-C在不同電位下的反應電流響應值明顯大于Ni-N4-C以及商業Ag NPs(圖7b),表明Ni-N3-C表現出最好的CO2催化活性。盡管 Ni-N4-C在-1.02 V下實現了98.3% CO FE的出色eCO2-to-CO性能和210.25 mA·cm?2的工業級jCO(圖7c),但Ni-N3-C在?0.89 V下獲得了467.55 mA·cm?2的超高 jCO(圖 7d),甚至超過了商用Ag NPs在-0.96 V下獲得的99.3% CO FE和250.18 mA·cm?2的最佳eCO2-to-CO性能(圖7e)。此外,即使在-1.00 V的更負電位下,Ni-N3-C可以實現96.2% CO FE和558.41 mA·cm?2的jCO的卓越性能(圖7f),優于Ni-N4-C和商業Ag NP兩倍以上。與文獻中報道的電催化劑的eCO2-to-CO性能相比(圖7g),通過MILPs策略調制的Ni-N3-C無論是CO選擇性還是部分電流密度,幾乎超過了其他電催化劑,是目前最先進的eCO2-to-CO電催化劑之一。 為了進一步揭示不同Ni─N配位環境對Ni SACs電子結構的影響,作者在VASP軟件包中進行DFT計算。以Ni-N3和Ni-N4為中心的SAC的電荷密度差結果分別如圖8a、b所示。證實了Ni-N3結構中Ni原子周圍的負電荷比Ni-N4位點更利于CO2分子的吸附和轉化。如圖8c的反應路徑,CO2分子首先吸附在Ni單原子中心,獲得電子并偶聯質子后形成*COOH中間體,進一步獲得電子和質子,生成*CO和H2O。最后,通過*CO的解吸產生氣態CO。如圖 8d 所示,原位ATR-SEIRAS結果證實電催化劑表面存在*COOH和*CO中間體,這與eCO2-to-CO的路徑和DFT計算的假設一致。 作者計算了具有不同Ni─N配位環境的Ni SACs上eCO2-to-CO路徑中各中間體的自由能,結果如圖8e所示。發現eCO2-to-CO路徑中的關鍵*COOH 中間體更容易在Ni-N3位點上進行。此外,作者進一步深入研究了其電子結構的差異(圖8f)。Ni-N3中心的Ni 3d電子態部分密度(PDOS)的計算d帶中心為-1.29 eV,比Ni-N4位點的-1.98 eV更正,有利于提高中間體在Ni單原子位點的吸附能力。Ni 3d PDOS在不同Ni─N配位環境下的差異可以很好地解釋中間體和低配位Ni-N3中心之間的吸附能高于Ni-N4位點 (圖8g)。結果表明,Ni-N3位點的配位環境可以更強地吸附*COOH關鍵中間體,加速eCO2-to-CO,從而提高催化活性和反應速率,這也與較高電流密度的結果很好地吻合。 總結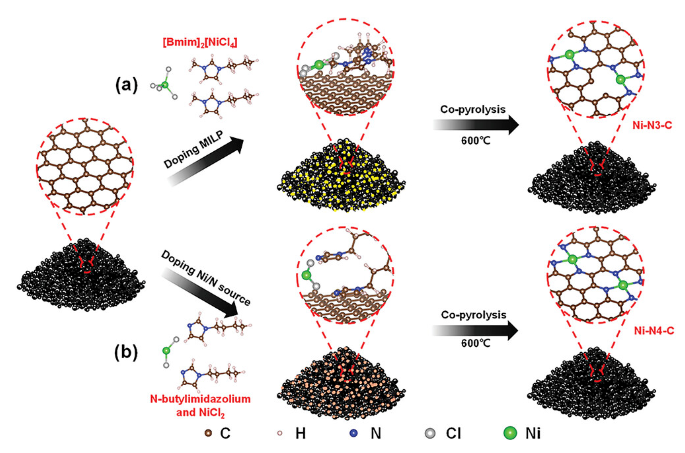
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn