

(圖片來源:Nat. Chem.)
正文
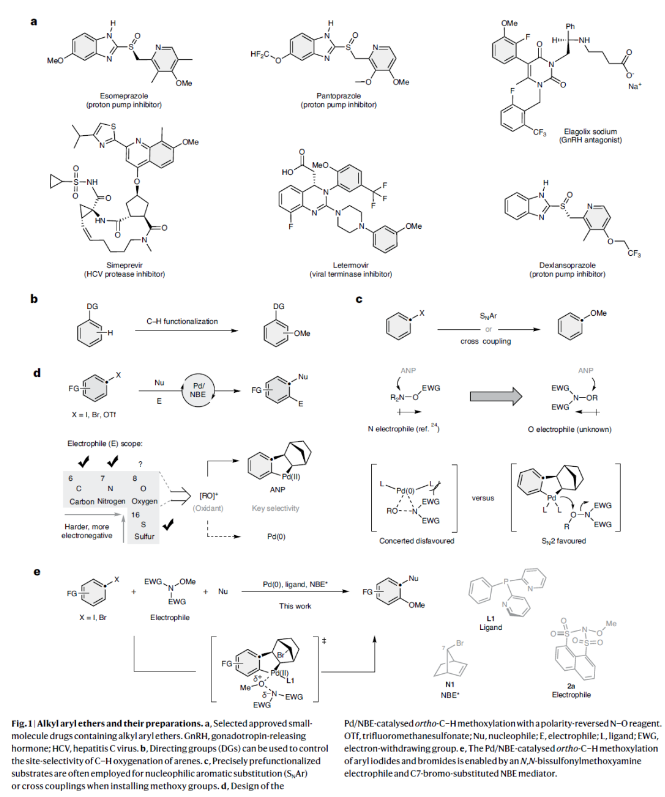
氧取代的芳烴廣泛存在于生物活性分子中(Fig. 1a),其還可以通過化學轉化實現其它官能團化的芳烴。然而,選擇性地直接將含氧基團安裝到芳香族化合物上仍具有一定的難度,特別是在同時實現芳烴的其它官能團化時則具有一定的挑戰性。目前,芳烴的C-H氧化策略通常需要導向基團或精確的預官能團化底物來控制位點選擇性(Fig. 1b)。此外,在大多數現有C-H氧化方法中,由于需要強氧化劑的參與可能會影響官能團的耐受性。雖然目前可以使用親核芳香取代或交叉偶聯等策略來實現芳烴的甲氧基化,但被官能團化的位置通常會受到離去基團或活化基團在芳烴底物中的位置所限制。因此,這通常需要使用精確的預官能團化底物來參與反應,但有時獲得它們并不容易(Fig. 1c)。
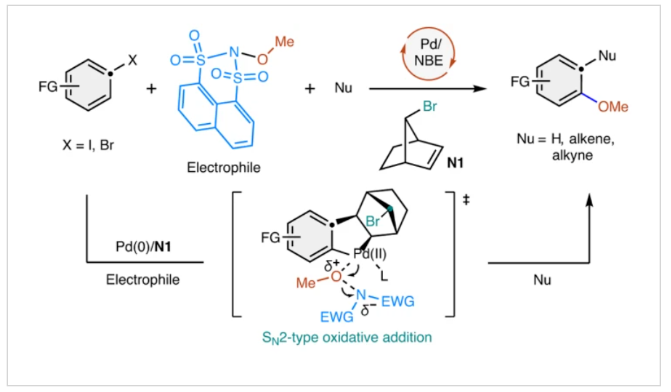
鈀/降冰片烯協同催化,又叫Catellani反應,其可以通過與親電試劑和親核試劑同時發生反應來實現特定位點芳烴的原位/鄰位雙官能團化。然而,已發展的反應中親電試劑通常僅局限于碳、氮和硫等“軟”元素。而實現“硬”親電試劑,如氧衍生物的偶聯則具有很大的挑戰性(Fig. 1d)。這主要是由于氧原子具有較大的電負性,且氧衍生物親電試劑通常具有較強的氧化性,其可以很容易的通過單電子轉移氧化Pd(0),并終止催化循環。最近,美國芝加哥大學董廣彬課題組與美國匹茲堡大學劉鵬課題組聯合發展了鈀/降冰片烯協同催化策略,首次實現了芳基鹵化物的鄰位C-H甲氧基化,快速構建了一系列芳基醚類化合物。其中,穩定的、極性反轉的N-O試劑以及C7-溴取代的降冰片烯的使用是實現此轉化的關鍵(Fig. 1e)。
(圖片來源:Nat. Chem.)
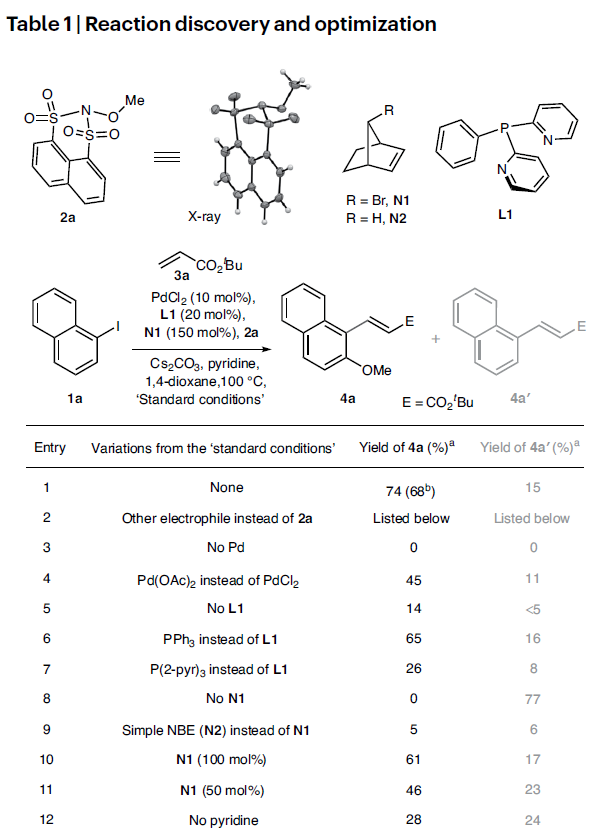
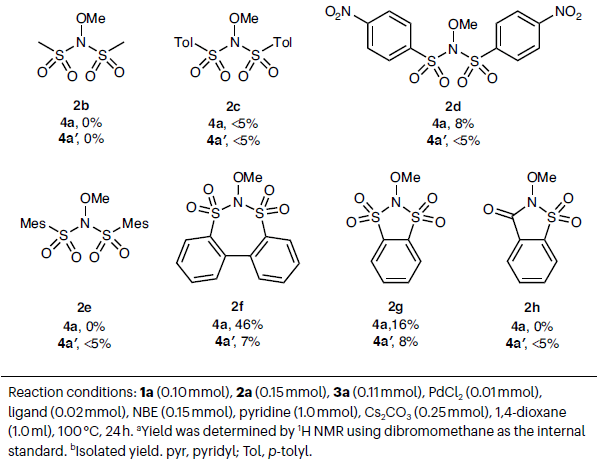
首先,作者選擇1-碘萘1a和丙烯酸叔丁酯3a作為模板底物進行反應探索(Table 1)。通過一系列條件篩選,作者發現當使用2a作為N-O親電試劑,PdCl2 (10 mol%), L1 (20 mol%), N1 (1.5 equiv.), Cs2CO3 (2.5 equiv.), 在1,4-二氧六環中100 °C反應24小時可以以74%的核磁產率和68%的分離產率得到鄰位C-H甲氧基化產物4a。
(圖片來源:Nat. Chem.)
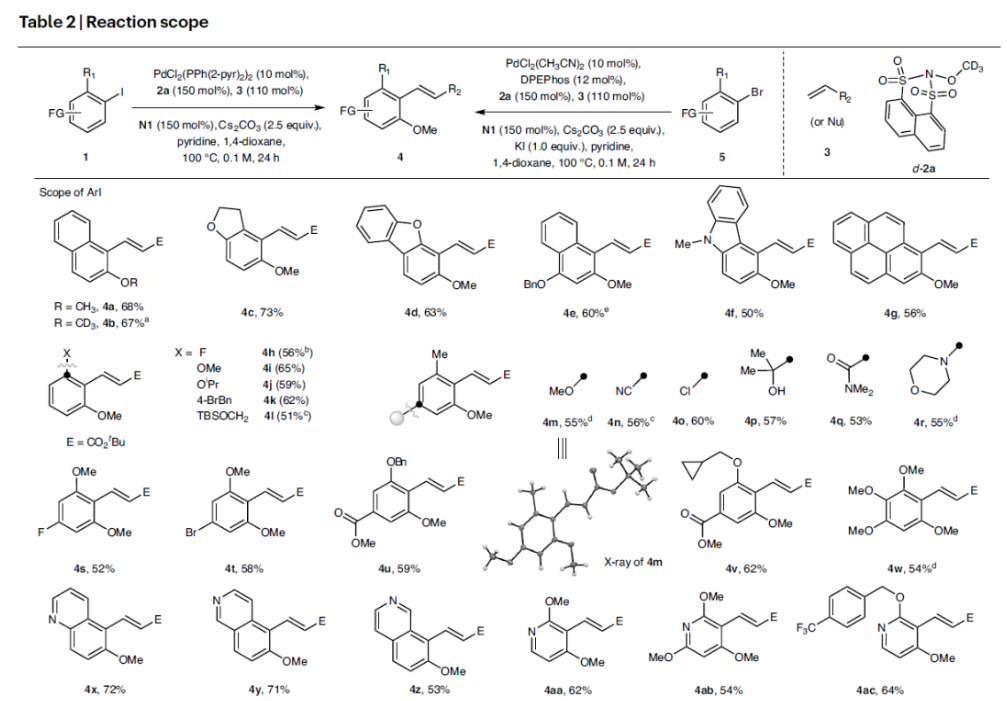
在得到了最佳反應條件后,作者對此轉化的底物范圍進行了考察(Table 2)。實驗結果表明不同取代的芳基碘化物均具有良好的兼容性,以53-73%的產率得到相應的鄰位C-H甲氧基化產物4a-4z, 4aa-4ac。值得注意的是,此轉化對一系列生物活性分子衍生的芳基碘化物,如D-galactose、quetiapine、napropamid和napropamid等同樣具有良好的兼容性,以37-63%的產率得到相應的產物4ad-4ag。除此之外,不同取代的烯基親核試劑,如丙烯酸酯、丙烯腈以及苯乙烯等同樣可以兼容,以47-71%的產率得到4ah-4ak。值得注意的是,除了利用烯烴作為親核試劑終止反應之外,其它的終止試劑,如2-冰片(2-Borneol)和三異丙基硅乙炔也可作為親核試劑參與反應,分別以57%和51%的產率得到相應的原位氫化產物4al和原位炔基化產物4am。接下來,當作者使用更廉價易得的芳基溴化物為底物時,通過對反應條件的進一步優化以及加入KI為添加劑則可以以中等至良好的產率(50-68%)得到相應的產物4an-4av。
(圖片來源:Nat. Chem.)
為了深入理解此轉化的反應機理,作者進行了DFT計算(Fig. 2)。計算結果表明,N-O親電試劑與富電子Pd(II)親核試劑之間經歷了獨特SN2-類型氧化加成過程。

(圖片來源:Nat. Chem.)
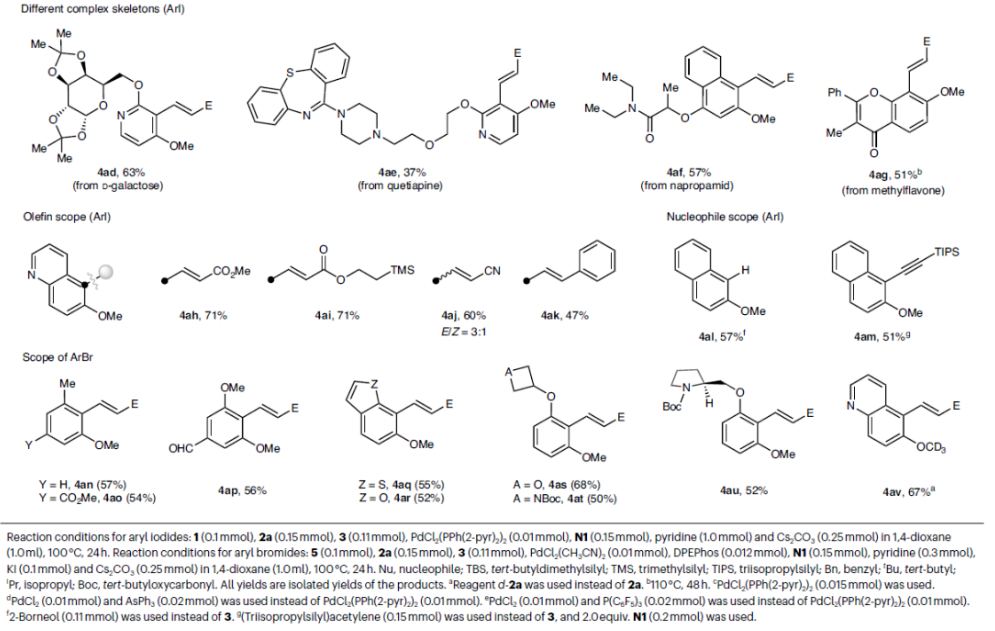
為了展示此方法的應用潛力,作者探索了其在構建重要結構骨架中的應用(Fig. 3)。2,3-二氫苯并呋喃9是獲得5-HT2C受體激動劑10的重要中間體。傳統的合成方法需要使用2,5-二羥基苯甲酸甲酯11,通過7步才能實現9的合成。而利用作者所發展出的鄰位氧化/原位Heck反應方法,則可以直接使用4-碘-2,3-二氫苯并呋喃1c和商業可得的起始原料,僅需1步即可以65%的產率實現9的合成。
再比如,酯13在治療癲癇方面表現出良好的抗驚厥活性。而在已報道的合成路線中,關鍵的羧酸中間體12則是由3,4,5 -三甲氧基苯甲醛14通過6步合成得到的。利用此方法,以芳基碘化物1w為起始原料,僅通過兩步(56%、98%)即可得到關鍵的羧酸中間體12,大大提升了合成效率。
(圖片來源:Nat. Chem.)
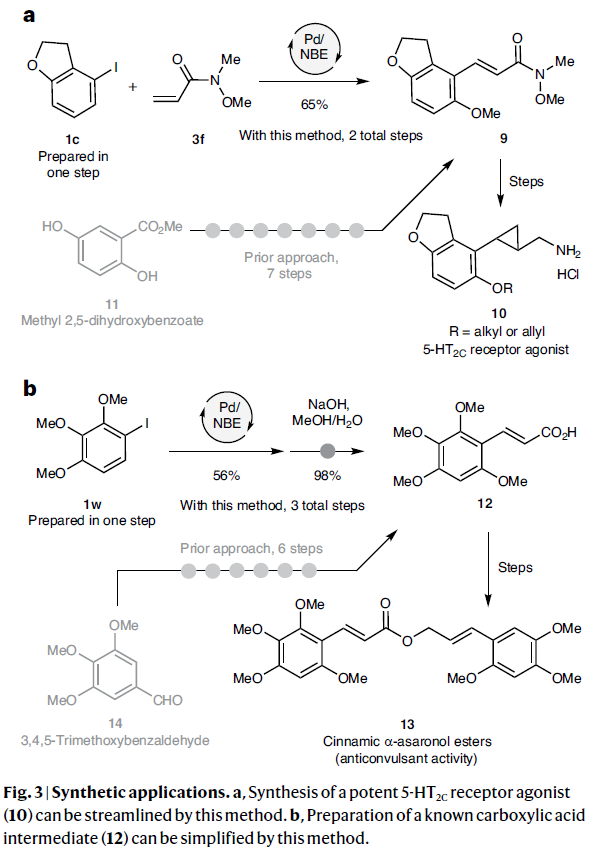
Merck公司最近的分析表明,在已批準的小分子藥物中,苯類化合物的取代模式較為單一,主要原因是缺乏獲得不同取代模式的有效途徑。特別是對于1,3,5-, 1,2,3,4-, 1,2,3,4,5- 和1,2,3,4,5,6-取代的苯環是四類最難獲得的結構(Fig. 4a)。考慮到甲氧基在分子內具有多重作用,作者認為上述取代模式均可以利用簡單易得鄰位取代的芳基鹵化物,通過接力C-H官能團化策略來實現(Fig. 4b)。作者首先利用15作為模板底物進行反應嘗試(Fig. 4c)。利用作者發展的方法,利用15可以以50%的產率得到1,2,3-三取代苯16(2.0 mmol規模);而16可以通過臭氧化(72%)和親電碘化(94%),以良好的對位選擇性得到1,2,3,4-四取代苯18;隨后,18通過鄰位烷基化/原位芳基化可以67%的產率到得到五取代苯19;接下來,19利用金催化的溴化以及進一步的Sonogashira偶聯即可得到全取代苯21。此外,利用18通過鄰位胺化/原位芳基化還可以以63%的產率到得到五取代苯22;22中的甲氧基可以通過兩步轉化為具有更高活性的三氟甲磺酸酯24(81%,90%),并通過隨后的Suzuki偶聯得到五取代烯基苯產物25(87%)。最后,作者利用2-碘甲苯26的鄰位氧化/原位氫化以52%的產率得到三氘甲氧基化產物27;其可以通過親電碘化和鄰位氧化/原位氫化的Catellani反應串聯得到1,3,5-三取代苯29。
(圖片來源:Nat. Chem.)
總結
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn