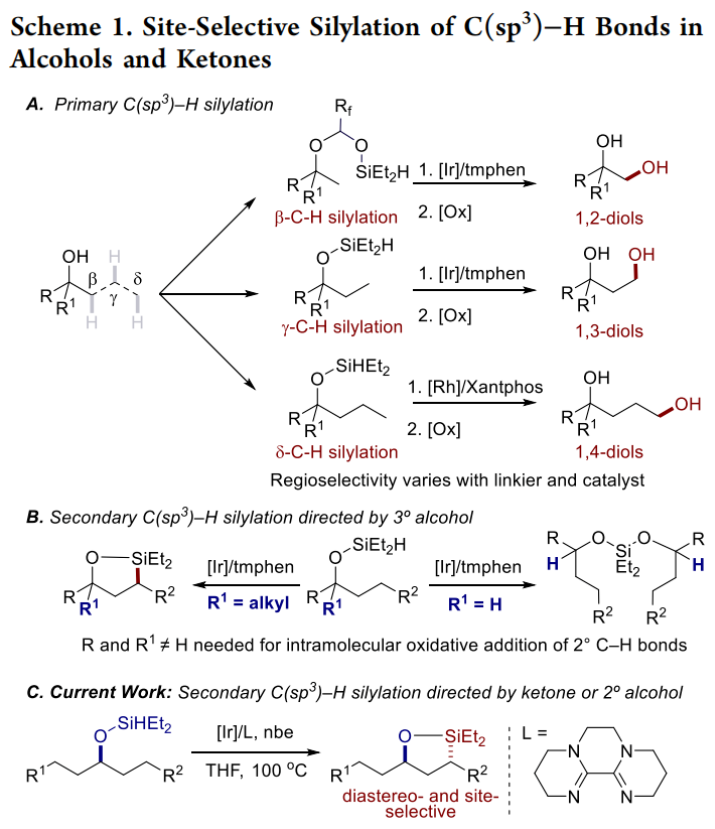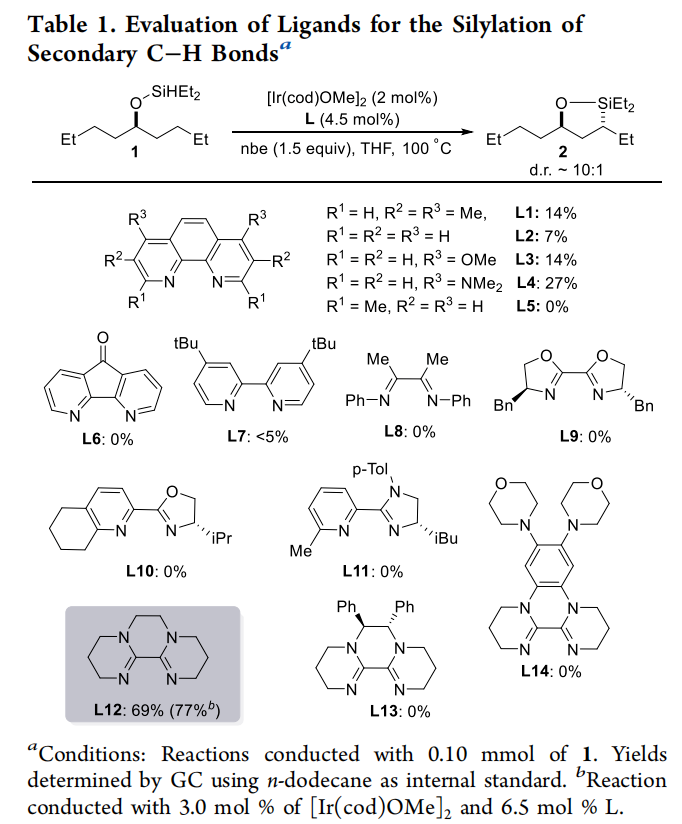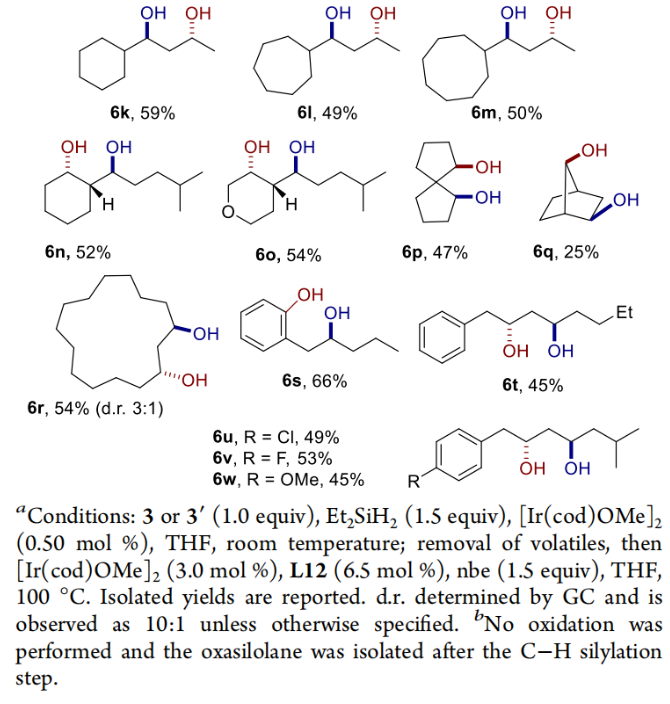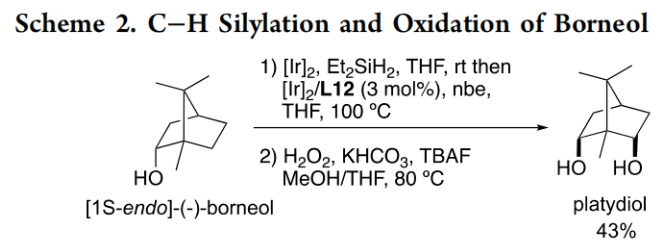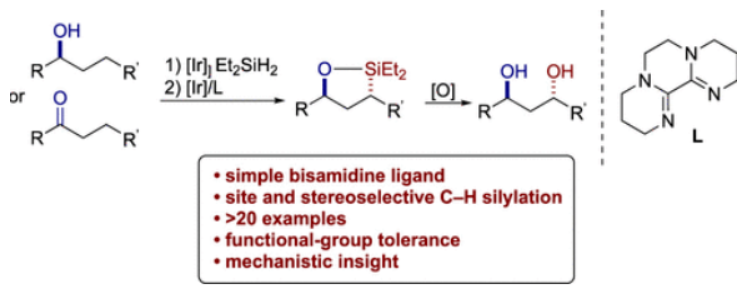
過渡金屬催化的C-H鍵選擇性官能團化為有機分子的合成及衍生化提供了新的策略。在這些官能團化過程中,C-H鍵硅基化是非常有價值的,因為有機硅烷產物很容易分離并進行各種衍生。烷基C-H鍵的催化硅基化可以發生在分子間或分子內。雖然已有文獻報道通過對醇的高區域選擇性β、γ和δ位的末端C-H鍵硅基化反應來生成環硅烷,而后通過氧化形成1,2-二醇、1,3-二醇和1,4-二醇(Scheme 1A),但是分子內二級C(sp3)-H硅基化則還未有報道。然而,二級C-H鍵的硅基化比一級C-H鍵的硅基化更具挑戰性,主要是由于C-H鍵的氧化加成比一級C-H鍵的氧化加成要慢。雖然John F. Hartwig課題組在2014年報道了二級C-H鍵的分子內硅基化反應(J. Am. Chem. Soc., 2014, 136, 6586),但反應底物的選擇則具有一定的局限性(Scheme 1B)。因此,發展更先進的催化體系來實現二級醇和酮的二級C-H鍵的硅基化具有重要意義。最近,美國加州大學伯克利分校John F. Hartwig課題組發展了銥/雙脒配體催化體系,選擇性的實現了二級醇或酮的氧原子γ-位二級C-H的硅基化,并通過后續的氧化,構建了反式1,3-二醇(Scheme 1C)。下載化學加APP到你手機,更加方便,更多收獲。首先,作者以硅醚1作為模板底物進行反應探索(Table 1)。通過一系列配體篩選,作者發現當使用[Ir(cod)OMe]2 (3.0 mol%), 雙脒配體L12 (6.5 mol%), nbe (norbornene, 降冰片烯,1.5 equiv), 在THF中100 oC反應,可以以77%的產率得到γ-位C-H硅基化產物2。接下來,作者利用二級醇或酮作為底物,首先通過[Ir(cod)OMe]2催化的脫氫硅基化或氫硅化得到相應的硅醚,隨后經歷作者發展的γ-位C-H硅基化以及后續的Tamao-Fleming氧化實現了一系列1,3-二醇的合成(Table 2)。實驗結果表明,一系列對稱的二級醇、非對稱的二級醇(在小位阻的C-H鍵一側)均可順利參與反應,以45-67%的產率得到相應的1,3-二醇6a-6g。環二級C-H鍵也可順利實現γ-C-H硅基化,以36-92%的產率得到產物6h-6j。此外,此體系對一系列環狀化合物具有良好的普適性,包括中到大環、螺環、橋環等,以25-59%的產率得到1,3-二醇產物6k-6r。值得注意的是,對于3t’,可以選擇性的在二級C(sp3)-H發生硅基化。之所以沒有在C(sp2)-H位點發生硅基化可能由于會形成八元氧硅環產物。當作者使用萜烯類化合物[1S-endo]-(?)-borneol反應時,可以以43%的產率得到platydiol,且氧原子的α-位并沒有發生差向異構化(Scheme 2)。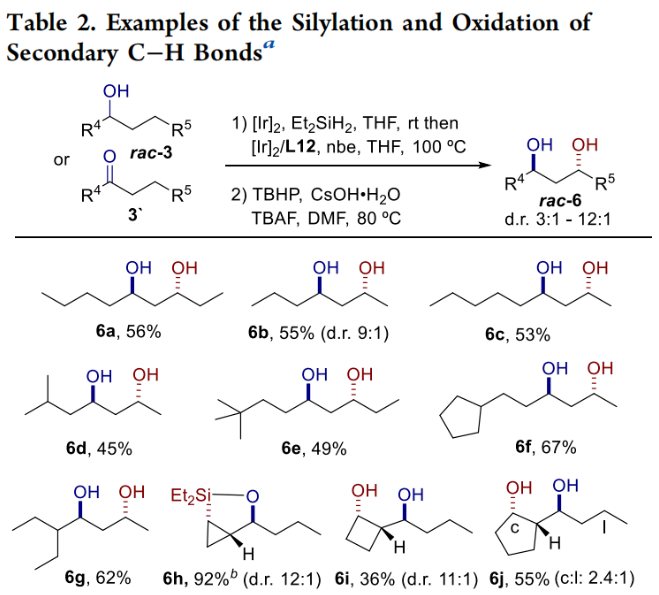
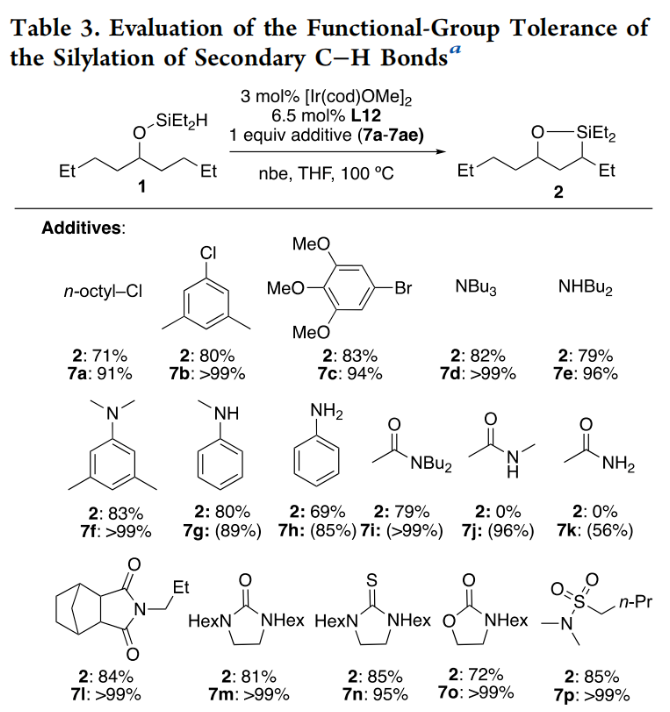
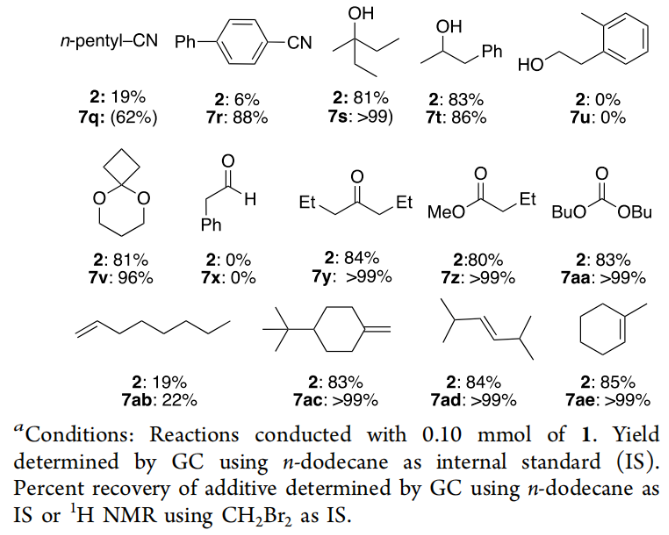
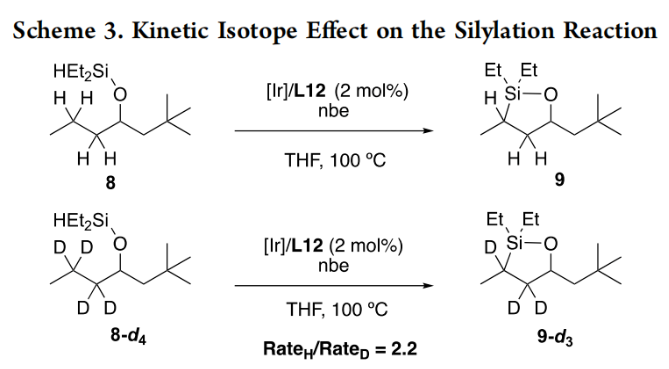
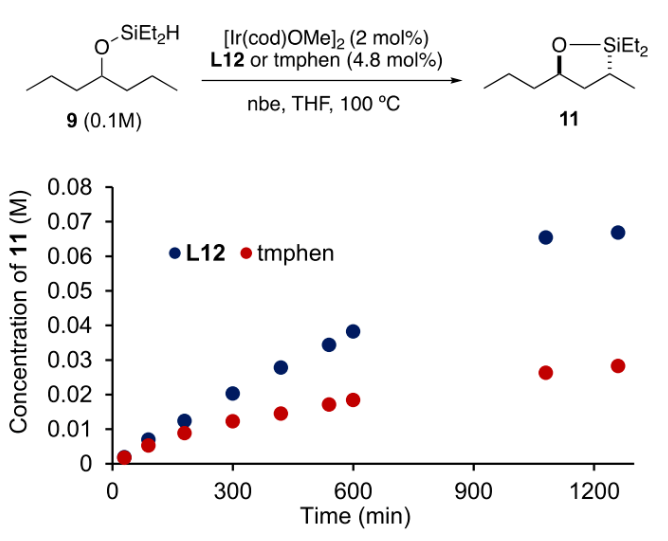
隨后,作者對此體系的官能團兼容性進行了進一步考察(Table 3)。當沒有添加劑時,1在標準條件下可以以85%的產率得到2。當體系中存在23類官能團時,包括烷基和芳基鹵化物、叔和仲烷基胺、芳基胺、叔酰胺、鄰苯二胺、脲、硫脲、氨基甲酸酯、磺胺、叔和仲醇、縮醛、酮、酯、碳酸鹽、1,1-和1,2-二取代烯烴、三取代烯烴等,均對產物2的產率沒有太大的影響。而其中七類官能團對此轉化有一定的影響,包括二級和一級酰胺(7j, 7k)、烷基和芳基腈(7q, 7r)、伯醇和醛(7u, 7x)、單取代烯烴(7ab)。為了理解反應機理,作者進行了一系列控制實驗。首先KIE實驗表明C-H鍵的斷裂為此轉化的決速步驟(KIE = 2.2)(Scheme 3)。隨后,作者以9為原料,分別以tmphen和L12為配體測量了其C-H硅基化的反應時間進程。實驗結果表明銥催化劑與L12配體結合成的銥絡合物的壽命有所延長,而并不是反應速率的提高(Figure 1)。最后,作者利用競爭實驗得出配體L12更易于與銥催化劑形成銥絡合物(Scheme 4)。由于L12對Ir(III)金屬中心的結合親和力大于tmphen,由此導致由L12生成的催化劑比tmphen生成的催化劑壽命更長。John F. Hartwig課題組發展了銥/雙脒絡合物催化體系,通過選擇性γ-位二級C-H的硅基化以及后續的氧化,實現了一系列反式1,3-二醇的合成。反應具有良好的底物適用性和官能團兼容性。機理研究表明C-H活化為此轉化的決速步驟,且強給電子的雙脒配體可以延長催化劑的壽命。文獻詳情:
Jake W. Wilson, Bo Su, Makoto Yoritate, Jake X. Shi, John F. Hartwig*. Iridium-Catalyzed, Site-Selective Silylation of Secondary C(sp3)-H Bonds in Secondary Alcohols and Ketones. J. Am. Chem. Soc., 2023, https://doi.org/10.1021/jacs.3c03127.