

正文
有機磷化合物由于其獨特的生物和化學特性,在有機化學、藥物化學和材料科學等領域中有著重要而廣泛的應用,如何高立體選擇性地構建手性有機磷化合物是有機化學領域的重要研究方向之一。過渡金屬催化重氮化合物分解生成金屬卡賓繼而發生不對稱X-H鍵插入反應是立體選擇性構建C-X鍵的有效途徑。雖然金屬卡賓參與的不對稱X-H(X=C, N, O, S, Si, B)插入反應已獲得較好的發展,但P-H插入反應在經過三十多年發展之后仍未有效解決其不對稱催化的難題,直接影響了該C-P鍵高效構建方法的應用。不對稱催化P-H插入反應挑戰在于:(1)膦氫化合物易毒化手性金屬催化劑,從而影響重氮分解生成金屬卡賓或手性配體的立體選擇性控制能力;(2)不對稱P-H插入反應的質子轉移過程不易控制;(3)活性卡賓中間體易于發生自聚等競爭反應。下載化學加APP到你手機,更加方便,更多收獲。
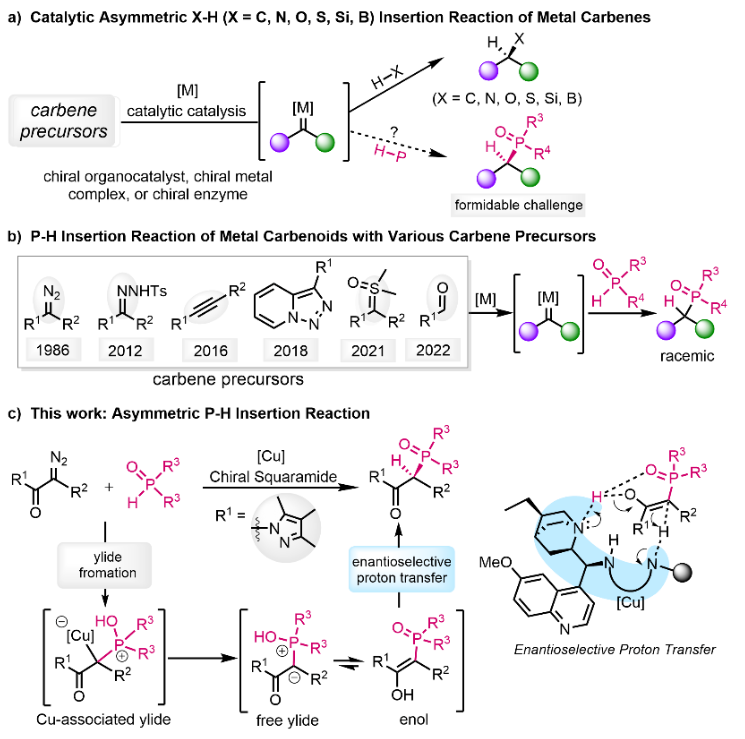
圖1 金屬卡賓的插入反應
作者首先使用重氮吡唑酰胺A1和二苯基膦氧B1作為底物模型對反應條件進行篩選(圖2),并在反應條件篩選中發現:(1)金屬銅化合物和手性有機小分子催化劑缺一不可;(2)手性有機小分子催化劑需同時具備質子供體和質子受體的雙功能性質才能很好地實現反應的立體選擇性控制;(3)手性有機小分子催化劑的骨架結構為金雞納堿時反應立體選擇性效果最好。經過大量的條件篩選后確定了最優反應條件:溴化亞銅(CuBr)和手性奎寧方酰胺衍生物Q7作為共催化劑,硫酸鋇作為添加劑,二氯甲烷(DCM)作為溶劑,反應溫度為0 ℃,同時使用硼氫化鈉作為還原劑,一鍋法合成手性b-羥基膦氧化合物。
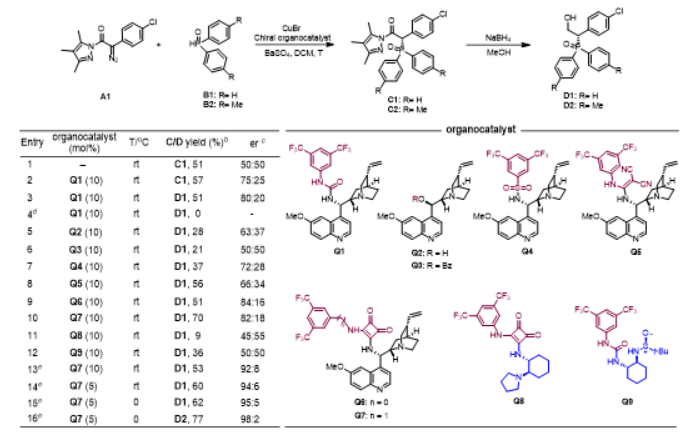
圖2 條件篩選
在最優反應條件下,作者對底物普適性進行了考查(圖3)。首先,苯環上帶有不同吸電子和供電子取代基的重氮吡唑酰胺底物均有很好的適用性,稠環重氮吡唑酰胺底物也能以較好的收率和高對映體選擇性生成相應手性b-羥基膦氧化合物(圖3A)。隨后,對不同的膦氫化合物底物進行拓展,含有供電子和吸電子取代基的芳環和萘環均能順利地發生不對稱P-H插入反應,生成相應的手性b-羥基膦氧化合物(圖3B),膦氫化合物的電子效應和位阻效應對該反應有較大影響。作者還進一步驗證了該反應的可擴展性和實用性,反應放大至1 mmol規模時,仍可以以73%的產率和95:5 er的對映體選擇性合成目標產物。同時,作者對產物進行了衍生實驗,手性b-羥基膦氧化合物可以順利進行硼烷化、溴化和酯化等多種轉化,為快速獲得結構多樣的手性膦氧化合物提供了可能途徑。
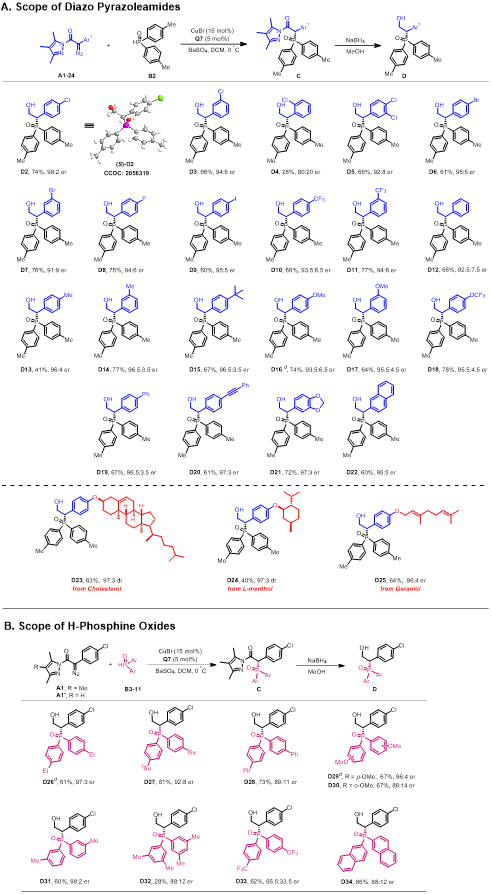
圖3 底物拓展
為了進一步探索反應機理,研究人員開展了氘代實驗、控制實驗等機理驗證實驗。此外,廣西大學謝鵬副教授對該反應進行了密度泛函理論(DFT)計算研究。如圖4所示,膦氫化合物B1的互變異構體B1’與銅卡賓中間體IM1發生反應生成銅絡合的葉立德IM2,再經羰基扭轉、質子轉移和銅解離等過程生成烯醇中間體IM5。作者還對銅催化劑與奎寧方酰胺Q7在不同位點絡合形成的催化物種,及其與IM5發生Ha質子轉移生成中間體IM6的能壘進行比較,發現當銅催化劑與奎寧方酰胺Q7的雙羰基配位形成的[Cu·Q7]*配合物時的反應能壘更低,只有4.1 kcal/mol。最后,在不對稱質子轉移生成產物C1的過程中,分別計算了Ha、Hb和Hc質子轉移途徑的反應能壘,結果顯示,Hc發生質子轉移過程的能壘最小。作者還比較了決定反應對映體選擇性的過渡態TS7(S)和TS7(R)的反應能壘,發現反應經過TS7(S)的能壘比TS7(R)低1.4 kcal/mol,解釋了產物(S)絕對構型產生的原因。
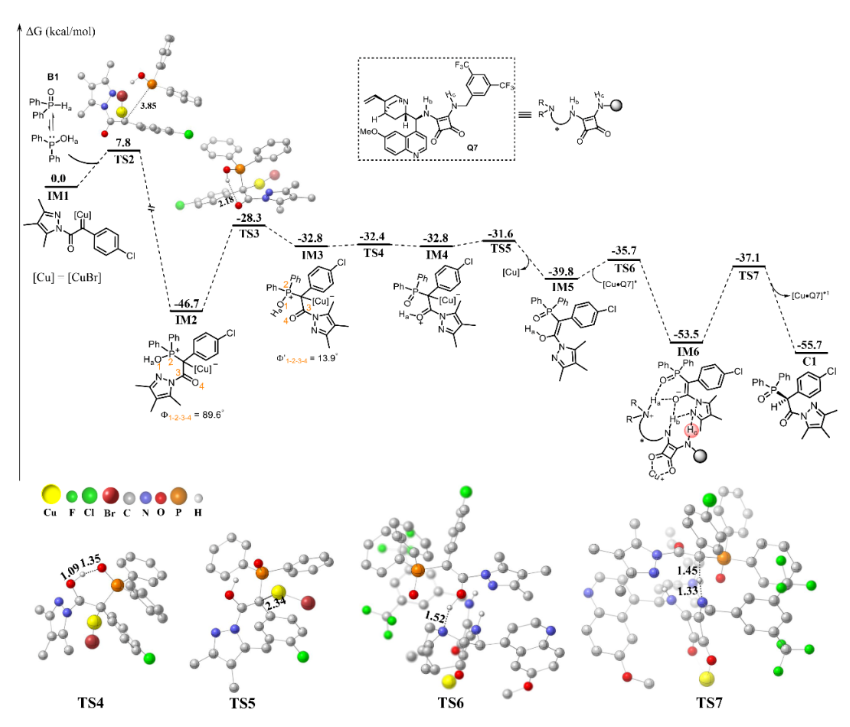
圖4 反應機理的計算研究
總結
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn