

研究團隊使用專家知識改善的人工智能逆向合成方法針對6種潛在的抗新冠藥物(圖1)的合成路線進行了設計,以便找到低成本大規模生產的簡單路線。
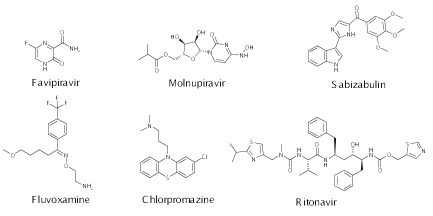
圖1潛在的抗新冠藥物
設計出的新合成路線中,法匹拉韋(Favipiravir)的步驟僅為3步,而它已有的合成路線為5步;Molnupiravir的新路線的步驟為2步,已有路線為2步;Sabizabulin的新路線的步驟為4步,已有路線為5步;Fluvoxamine的新路線的步驟為2步,已有路線為3步;Chlorpromazine的新路線的步驟為1步,已有路線為1步;Ritonavir的新路線的步驟為2,已有路線為3步。除了Molnupiravir和Chlorpromazine的已有路線已經很少以外,其他復雜藥物分子的新合成路線的步驟均減少了1-2步。為驗證新合成路線的合理性,以法匹拉韋為例進行了實驗合成驗證,經過實驗證實了設計的新合成路線有效,且成本相比已有路線便宜了近44倍。
綜上,研究團隊對人工智能輔助逆向合成方法引入專家知識,改善了包含稀有反應的合成路線的預測。并用專家知識改善的人工智能逆向合成方法設計了6種潛在抗新冠藥物的合成路線,通過實驗證實了法匹拉韋的合成。相關成果以“Optimized synthesis of anti-COVID-19 drugs aided by retrosynthesis software”為題,發表在RSC Medicinal Chemistry期刊,并被選為封面文章(FrontCover)。山東大學前沿交叉科學青島研究院碩士研究生戚文濤和翟冬助理研究員為該論文的共同第一作者,鄧偉僑教授和蘇州大學李有勇教授為通訊作者,山東大學為第一完成單位。相關研究得到了國家重點研發計劃,國家自然基金委,山東省自然基金等項目的支持。

圖2相關發表論文的RSCMedicinalChemistry封面
原文鏈接:https://doi.org/10.1039/D2MD00444E
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn