- 首頁
- 資訊
?JACS:芳烴的形式脫氫合成芳炔
來源:化學(xué)加原創(chuàng) 2023-02-13
導(dǎo)讀:近日,美國波特蘭州立大學(xué)David R. Stuart課題組報道了一種簡單芳烴的兩步形式脫氫策略,可在相對于傳統(tǒng)反應(yīng)性基團(如鹵化物)較遠的位置生成芳炔衍生物。其中,該方法是通過區(qū)域選擇性地引入和去除“鎓”離去基團實現(xiàn)的。同時,簡單芳烴(20例)和arynophiles(8例)均與體系兼容。此外,通過與目前芳炔前體的合成策略相比,該形式脫氫策略在生成芳炔方面更具出色的官能團兼容性和效率。與其它方法不同,芳炔中間體還為區(qū)域選擇性C-H胺化提供了機會。文章鏈接DOI:10.1021/jacs.2c13007
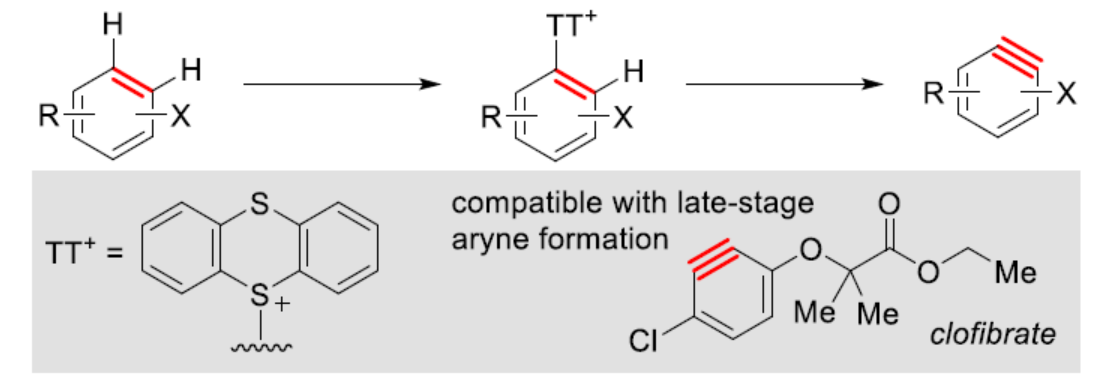
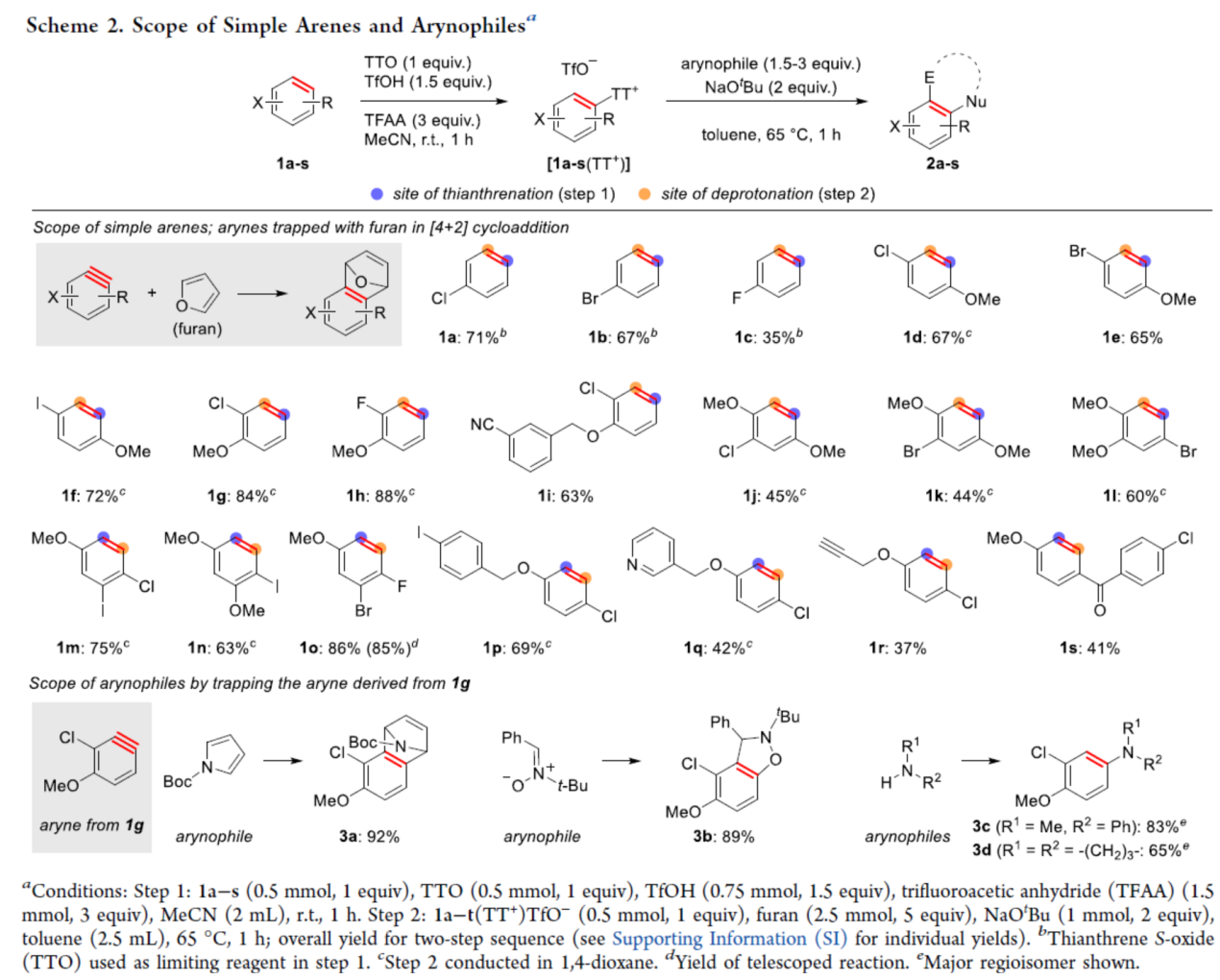
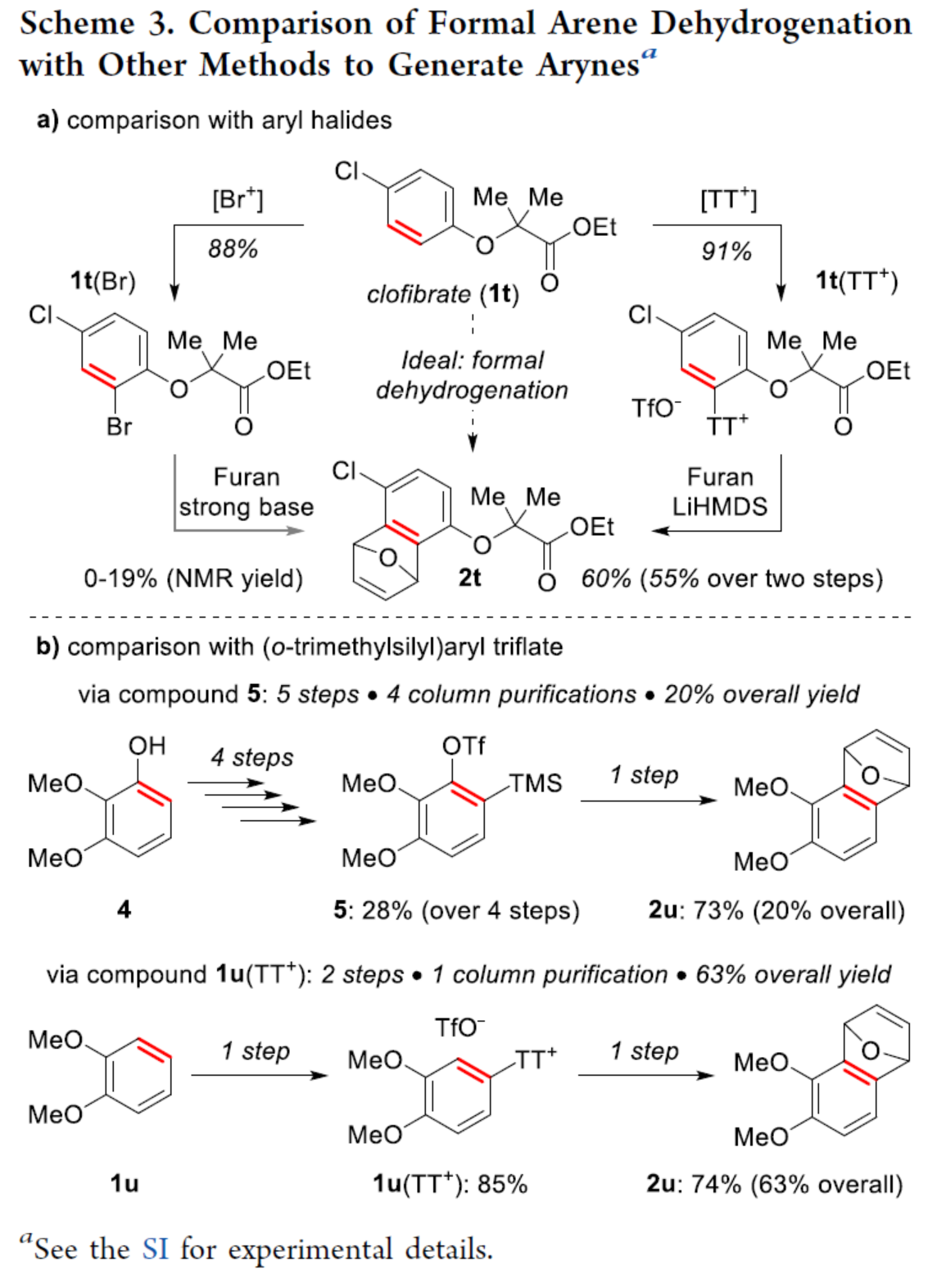
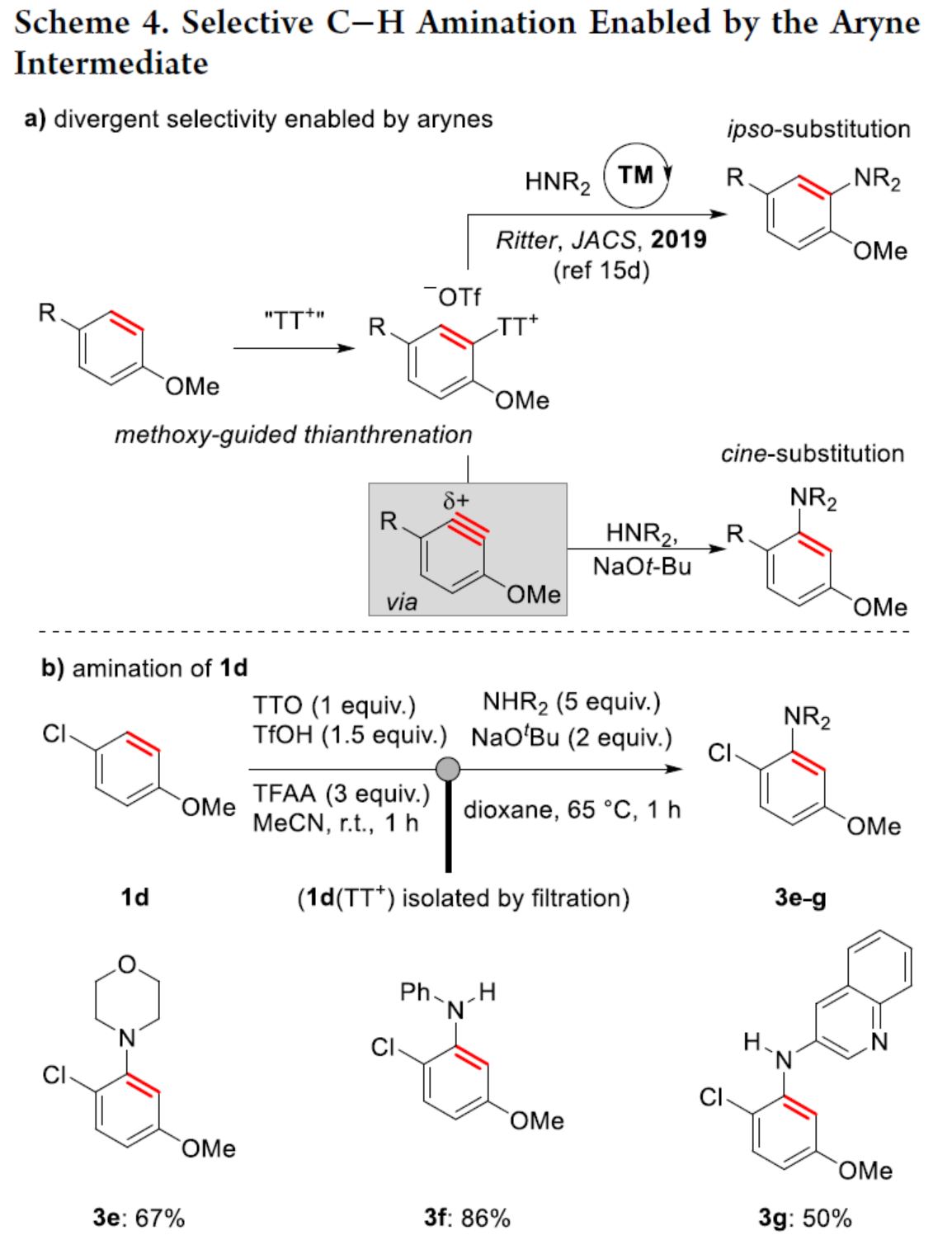
自從一個多世紀(jì)前,芳炔化合物被發(fā)現(xiàn)以來,由于其在合成方面的多功能性,芳炔化合物的合成一直備受關(guān)注。這些高反應(yīng)性中間體通常不易分離和儲存,因此需要合成前體來充分利用其反應(yīng)性。芳炔化學(xué)的許多顯著進展涉及開發(fā)新的前體或開發(fā)合成芳炔的新方法。目前,化學(xué)家們發(fā)現(xiàn)了兩種簡單性的芳炔前體(Scheme 1a)。其中,芳基鹵化物是最簡單的芳炔前體,但此類反應(yīng)常需強堿來進行芳環(huán)的去質(zhì)子化并消除鹵化物離去基團,導(dǎo)致數(shù)千種商用芳基鹵化物的優(yōu)勢被削弱(Scheme 1a,left)。鈉和鋰酰胺、烷基鋰和叔丁醇鉀以及18-冠-6是這種方法的已知堿,但它們與酸性和親電官能團不相容,導(dǎo)致了底物范圍有限。同時,在多鹵代芳烴中,也存在去質(zhì)子化和鹵化物離去的低選擇性問題。為了解決芳基鹵化物的區(qū)域選擇性和化學(xué)選擇性問題,化學(xué)家們發(fā)現(xiàn)了一種(鄰三甲基硅基)芳基三氟甲磺酸酯試劑(Scheme 1a,right)。然而,此類試劑不易直接購買,并且它們的合成通常需要從苯酚經(jīng)三至四步反應(yīng)。同時,(鄰三甲基硅基)芳基三氟甲磺酸酯試劑需要使用烷基鋰試劑來引入三甲基硅基,從而限制了這些芳炔前體中的酸性和親電性的官能團。因此,簡單芳烴的直接形式脫氫仍是合成芳炔的理想合成前體。理想情況下,簡單芳烴的脫氫將以選擇性的方式進行,其中合成有用的鹵化物被完全保留,并且親電和酸性官能團也是相容的(Scheme 1b)。因此,各種簡單的芳烴砌塊可以作為芳炔的前體,從而擴大這些中間體的合成潛力。近日,美國波特蘭州立大學(xué)David R. Stuart課題組報道了一種簡單芳烴的兩步形式脫氫策略,合成了一系列芳炔衍生物,具有出色的官能團兼容性與區(qū)域選擇性(Scheme 1c)。其中,位點選擇性芳炔的形成是通過區(qū)域選擇性地引入和去除“鎓”離去基團(噻蒽鎓,TT+)來實現(xiàn)的。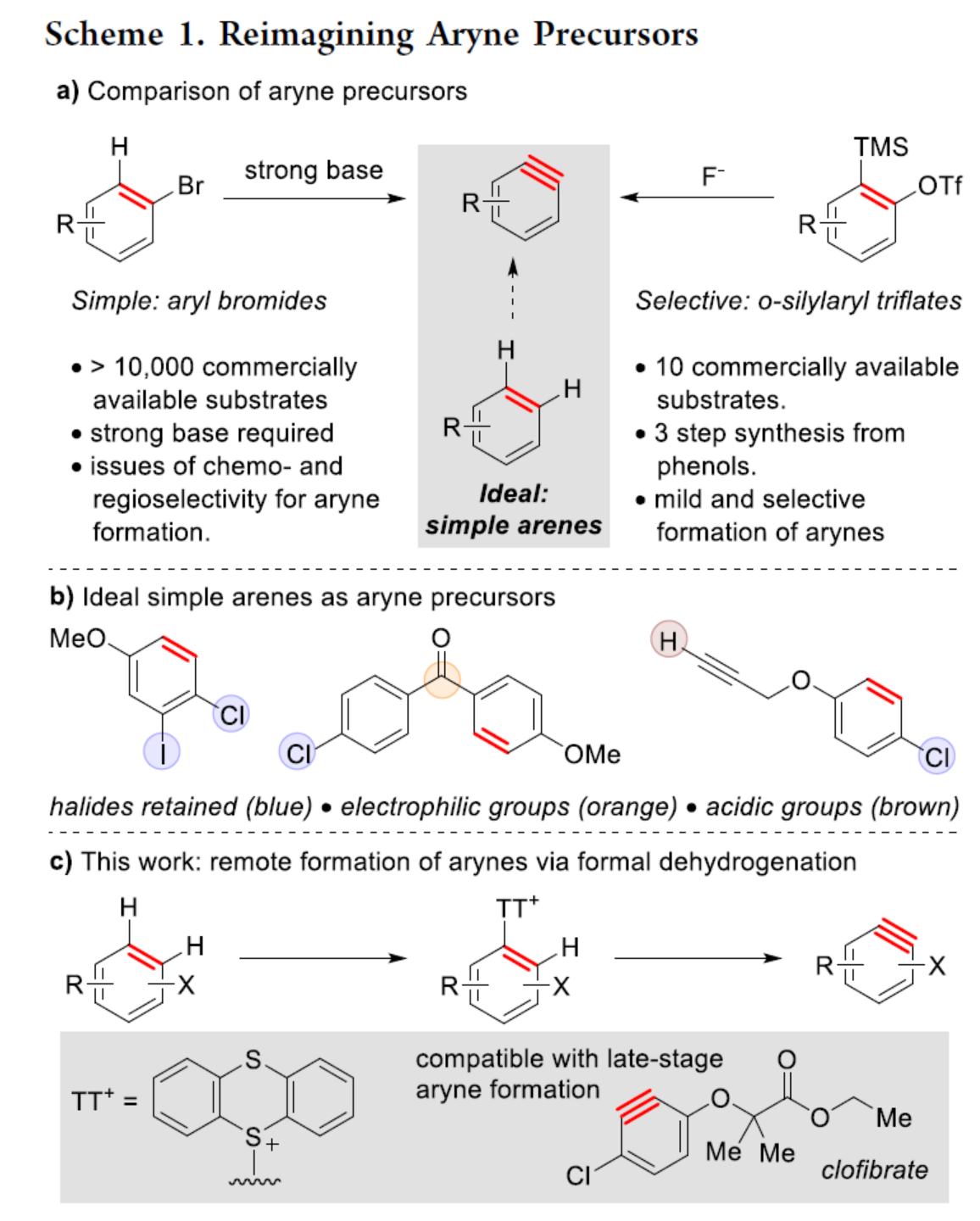 首先,作者以氯苯1a與呋喃作為模型底物,進行了相關(guān)三組分偶聯(lián)反應(yīng)條件的篩選(Table 1)。當(dāng)氯苯1a在TTO/TfOH/TFAA條件下室溫反應(yīng)1 h,可生成含有TT+離去基團的中間體1a(TT+)。隨后,當(dāng)以NaOt-Bu(2 eq.)作為堿,1a(TT+)可與呋喃在甲苯溶劑中65 oC反應(yīng)1 h,可以81%的收率得環(huán)加成產(chǎn)物2a。在獲得上述最佳反應(yīng)條件后,作者對底物范圍進行了擴展(Scheme 2)。首先,一系列簡單的芳烴,均可順利進行反應(yīng),獲得相應(yīng)的產(chǎn)物2a-2s,收率為35-88%。值得注意的是,該反應(yīng)具有出色的官能團兼容性,如炔基、鹵素等均與體系兼容。其次,該策略還可以環(huán)加成(吡咯和硝酮)和親核加成(苯胺和氮雜烷)的方式進行,獲得相應(yīng)的產(chǎn)物3a-3d,收率為65-92%。為了進一步證明反應(yīng)的兼容性以及效率,作者對該形式芳烴脫氫策略與其它方法生成芳炔的策略進行了對比(Scheme 3)。首先,以氯貝特(clofibrate,1t)作為底物,分別生成了中間體1t(Br)(收率為88%)和1t(TT+)(收率為91%)。其中,1t(Br)的溴化時間長達72 h,且需柱色譜進行分離純化。然而,1t(Br)在強堿性條件下未能有效的與呋喃進行反應(yīng)。相比之下,1t(TT+)可在LiHMDS條件下順利進行環(huán)加成反應(yīng),可以60%的收率得到產(chǎn)物2t,兩步總收率為55%(Scheme 3a)。其次,以市售苯酚4為底物,通過四步反應(yīng)以及三次柱純化過程,可分別引入-OTf與-TMS,并以28%的總收率得到中間體5。5可與呋喃進行環(huán)加成反應(yīng),可以73%的收率得到產(chǎn)物2u。因此,以4為底物合成產(chǎn)物2u共需五步反應(yīng),四次柱純化過程,總收率為20%(Scheme 3b)。相比之下,以1u作為底物,可以85%的收率得到芳炔前體1u(TT+),僅需通過簡單的過濾分離即可。在NaOt-Bu條件下,1u(TT+)可與呋喃進行環(huán)加成反應(yīng),可以74%的收率得到產(chǎn)物2u。因此,通過該策略僅需兩步反應(yīng)(先生成1u(TT+),再與呋喃進行環(huán)加成反應(yīng))以及一次色譜純化,即可在數(shù)小時內(nèi)從簡單芳烴1u得到產(chǎn)物2u,總收率為63%。此外,作者還對芳炔中間體選擇性C-H胺化反應(yīng)進行了研究(Scheme 4)。首先,利用芳炔中間體與NHR2反應(yīng),可獲得cine-取代的胺化產(chǎn)物,并作為Ritter課題組(J. Am. Chem. Soc. 2019, 141, 13346.)合成ipso-取代的胺化產(chǎn)物的補充(Scheme 4a)。其次,通過1d生成的芳炔前體1d(TT+),可分別與嗎啉、苯胺和3-氨基喹啉進行胺化反應(yīng),獲得相應(yīng)的產(chǎn)物3e-3g,收率為50-86%(Scheme 4b)。
首先,作者以氯苯1a與呋喃作為模型底物,進行了相關(guān)三組分偶聯(lián)反應(yīng)條件的篩選(Table 1)。當(dāng)氯苯1a在TTO/TfOH/TFAA條件下室溫反應(yīng)1 h,可生成含有TT+離去基團的中間體1a(TT+)。隨后,當(dāng)以NaOt-Bu(2 eq.)作為堿,1a(TT+)可與呋喃在甲苯溶劑中65 oC反應(yīng)1 h,可以81%的收率得環(huán)加成產(chǎn)物2a。在獲得上述最佳反應(yīng)條件后,作者對底物范圍進行了擴展(Scheme 2)。首先,一系列簡單的芳烴,均可順利進行反應(yīng),獲得相應(yīng)的產(chǎn)物2a-2s,收率為35-88%。值得注意的是,該反應(yīng)具有出色的官能團兼容性,如炔基、鹵素等均與體系兼容。其次,該策略還可以環(huán)加成(吡咯和硝酮)和親核加成(苯胺和氮雜烷)的方式進行,獲得相應(yīng)的產(chǎn)物3a-3d,收率為65-92%。為了進一步證明反應(yīng)的兼容性以及效率,作者對該形式芳烴脫氫策略與其它方法生成芳炔的策略進行了對比(Scheme 3)。首先,以氯貝特(clofibrate,1t)作為底物,分別生成了中間體1t(Br)(收率為88%)和1t(TT+)(收率為91%)。其中,1t(Br)的溴化時間長達72 h,且需柱色譜進行分離純化。然而,1t(Br)在強堿性條件下未能有效的與呋喃進行反應(yīng)。相比之下,1t(TT+)可在LiHMDS條件下順利進行環(huán)加成反應(yīng),可以60%的收率得到產(chǎn)物2t,兩步總收率為55%(Scheme 3a)。其次,以市售苯酚4為底物,通過四步反應(yīng)以及三次柱純化過程,可分別引入-OTf與-TMS,并以28%的總收率得到中間體5。5可與呋喃進行環(huán)加成反應(yīng),可以73%的收率得到產(chǎn)物2u。因此,以4為底物合成產(chǎn)物2u共需五步反應(yīng),四次柱純化過程,總收率為20%(Scheme 3b)。相比之下,以1u作為底物,可以85%的收率得到芳炔前體1u(TT+),僅需通過簡單的過濾分離即可。在NaOt-Bu條件下,1u(TT+)可與呋喃進行環(huán)加成反應(yīng),可以74%的收率得到產(chǎn)物2u。因此,通過該策略僅需兩步反應(yīng)(先生成1u(TT+),再與呋喃進行環(huán)加成反應(yīng))以及一次色譜純化,即可在數(shù)小時內(nèi)從簡單芳烴1u得到產(chǎn)物2u,總收率為63%。此外,作者還對芳炔中間體選擇性C-H胺化反應(yīng)進行了研究(Scheme 4)。首先,利用芳炔中間體與NHR2反應(yīng),可獲得cine-取代的胺化產(chǎn)物,并作為Ritter課題組(J. Am. Chem. Soc. 2019, 141, 13346.)合成ipso-取代的胺化產(chǎn)物的補充(Scheme 4a)。其次,通過1d生成的芳炔前體1d(TT+),可分別與嗎啉、苯胺和3-氨基喹啉進行胺化反應(yīng),獲得相應(yīng)的產(chǎn)物3e-3g,收率為50-86%(Scheme 4b)。
美國波特蘭州立大學(xué)David R. Stuart課題組報道了一種簡單芳烴的形式脫氫生成芳炔前體的策略。該策略使用噻蒽鎓(thianthrenium)基團作為雙電子氧化劑,從而使反應(yīng)能夠在相對溫和的條件下進行。與目前已知的方法相比,該策略具有出色的官能團耐受性,并提供了一種高效和選擇性的合成芳炔的方法。此外,芳炔中間體還可參與多種不同的轉(zhuǎn)化,進一步證明了反應(yīng)的實用性。
文獻詳情:
Riley A. Roberts, Bryan E. Metze, Aleksandra Nilova, David R. Stuart*. Synthesis of Arynes via Formal Dehydrogenation of Arenes. J. Am. Chem. Soc. 2023, https://doi.org/10.1021/jacs.2c13007
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn