



(圖片來(lái)源:J. Am. Chem. Soc.)
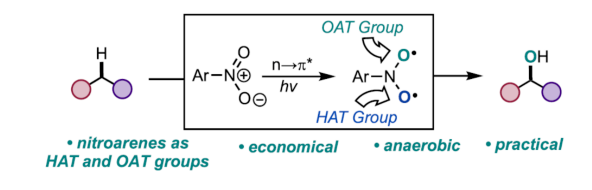
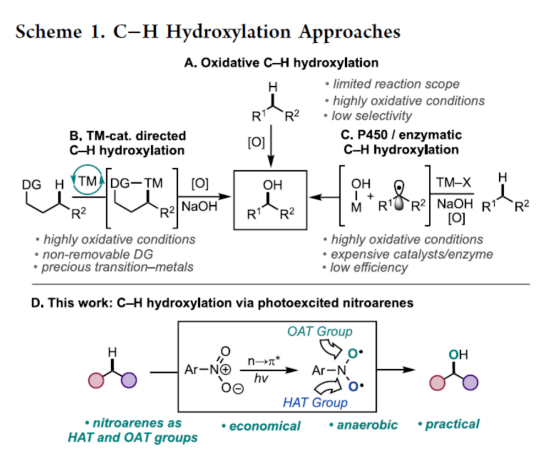
脂肪族C-H鍵直接轉(zhuǎn)化為羥基,是有機(jī)化學(xué)中的一個(gè)具有價(jià)值的研究課題。然而,由于C(sp3)-H鍵的位點(diǎn)選擇性活化難度大以及一些氧化敏感性官能團(tuán)的兼容性問(wèn)題,此類反應(yīng)具有一定的挑戰(zhàn)。目前,化學(xué)家們已開(kāi)發(fā)出幾種創(chuàng)新型的策略,可在脂肪族骨架上引入氧原子(Scheme 1)。然而,由于C-H鍵的直接氧化條件苛刻,從而限制了底物的范圍。此外,使用這種方法很難實(shí)現(xiàn)位點(diǎn)選擇性的C-H氧化功能化和對(duì)醇優(yōu)于其它過(guò)氧化副產(chǎn)物的偏好(Scheme 1A)。為了解決位點(diǎn)選擇性的問(wèn)題,化學(xué)家們?cè)谶^(guò)渡金屬催化的C-H羥基化反應(yīng)使用了導(dǎo)向基團(tuán),但存在導(dǎo)向基團(tuán)的引入與去除的繁瑣過(guò)程以及貴金屬催化劑的使用(Scheme 1B)。最近,仿生Mn/Fe-催化或酶催化C-H羥基化反應(yīng)是貴金屬方法的一種有效的替代策略,但也存在反應(yīng)效率低、過(guò)度氧化、配體與酶的成本高等問(wèn)題(Scheme 1C)。同時(shí),上述三種方法都需要使用額外的氧化劑,從而限制了反應(yīng)的底物范圍。近日,美國(guó)紐約大學(xué)Marvin Parasram課題組報(bào)道了一種光激發(fā)硝基芳烴介導(dǎo)脂肪族化合物的無(wú)氧C-H羥基化反應(yīng)(Scheme 1D)。值得注意的是,光激發(fā)硝基芳烴的雙自由基性質(zhì)使C-H活化和氧原子轉(zhuǎn)移步驟都成為可能,從而消除了對(duì)額外氧化劑的需要,并為C(sp3)-H羥基化提供了一種溫和、通用且經(jīng)濟(jì)高效的方法。
最近,化學(xué)家們研究發(fā)現(xiàn),硝基芳烴的可見(jiàn)光激發(fā)可生成三重態(tài)的雙自由基中間體,可使烯烴發(fā)生斷裂生成羰基化合物。機(jī)理研究表明,上述的三重態(tài)雙自由基中間體能夠與硝基芳烴的鄰?fù)榛ㄟ^(guò)分子內(nèi)氫原子轉(zhuǎn)移(HAT)活化C-H鍵。同時(shí),在苛刻的紫外線照射下,硝基芳烴的氧原子轉(zhuǎn)移(OAT)可以實(shí)現(xiàn)C-H氧化。此外,光激發(fā)的β-芳基取代的硝基芳烴可引發(fā)分子內(nèi)OAT,生成三級(jí)二芳基醇。雖然上述的兩種方法都具有顯著的新穎性,但其仍存在底物范圍有窄以及過(guò)度氧化的問(wèn)題。基于光生硝基芳烴作為C-H鍵活化劑和氧原子源的能力,作者設(shè)想,在可見(jiàn)光照射下能否實(shí)現(xiàn)脂肪族前體的選擇性、分子間無(wú)氧C-H鍵的羥基化反應(yīng)。
(圖片來(lái)源:J. Am. Chem. Soc.)
首先,通過(guò)對(duì)反應(yīng)條件的優(yōu)化后發(fā)現(xiàn),2-氯-4-硝基吡啶和3,5-雙(三氟甲基)硝基苯分別對(duì)芐基和非活化C-H鍵的羥基化是高效的;(2)使用六氟異丙醇(HFIP)作為添加劑,對(duì)于抑制羥基化產(chǎn)物的過(guò)度氧化至關(guān)重要,可能是通過(guò)氫鍵的相互作用;(3)對(duì)照研究表明,光和其它反應(yīng)組分是轉(zhuǎn)化所必需的。
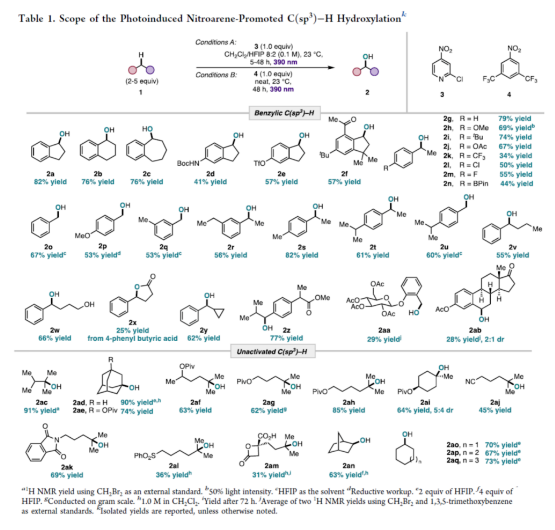
隨后,作者對(duì)底物范圍進(jìn)行了擴(kuò)展(Table 1)。在Conditions A條件下,具有不同環(huán)尺寸的環(huán)狀芐基化合物,均可順利進(jìn)行反應(yīng),獲得相應(yīng)的產(chǎn)物2a-2c,收率為76-82%。茚的芳基上含有-NHBoc和-OTf時(shí),也是合適的底物,獲得相應(yīng)的產(chǎn)物2d-2e,收率為41-57%。Celestolide是香精和香料中的一種有價(jià)值的分子,也可以57%的收率得到產(chǎn)物2f。其次,一系列具有不同電性取代的乙苯,均可順利進(jìn)行反應(yīng),獲得相應(yīng)的產(chǎn)物2g-2n和2r-2t,收率為34-82%。當(dāng)甲苯底物的芳基上含有烷氧基、甲基、異丙基時(shí),也與體系兼容,獲得相應(yīng)的產(chǎn)物2o-2q和2u,收率為34-79%。值得注意的是,基于2s-2t的反應(yīng)結(jié)果表明,芐基C(sp3)-H氧化反應(yīng)的選擇性為二級(jí)>一級(jí)>三級(jí)。具有不同鏈長(zhǎng)和官能團(tuán)的其它二級(jí)芐基底物,也能夠順利反應(yīng),獲得相應(yīng)的產(chǎn)物2v-2y,收率為25-66%。同時(shí),該策略還可用于一些藥物分子的后期修飾,如2z和2aa-2ab,收率為28-77%。
在Conditions B條件下,非活化底物中較弱的3°C-H鍵,可順利進(jìn)行羥基化反應(yīng),獲得相應(yīng)的產(chǎn)物2ac-2ad,收率為90-91%。含有遠(yuǎn)端新戊酸酯基的底物,也可選擇性的在3°C-H鍵進(jìn)行羥基化,獲得相應(yīng)的產(chǎn)物2ae-2ai,收率為62-85%。含有各種敏感性的極性基團(tuán),如腈、鄰苯二甲酰亞胺和磺酰基,也與體系兼容,獲得相應(yīng)的產(chǎn)物2aj-2al,收率為36-69%。同時(shí),該策略還可用于生物活性分子的后期衍生化,如2am。此外,一系列具有挑戰(zhàn)性的二級(jí)C-H鍵也可順利進(jìn)行C-H羥基化反應(yīng),獲得相應(yīng)的產(chǎn)物2an-2aq,收率為63-73%。
(圖片來(lái)源:J. Am. Chem. Soc.)
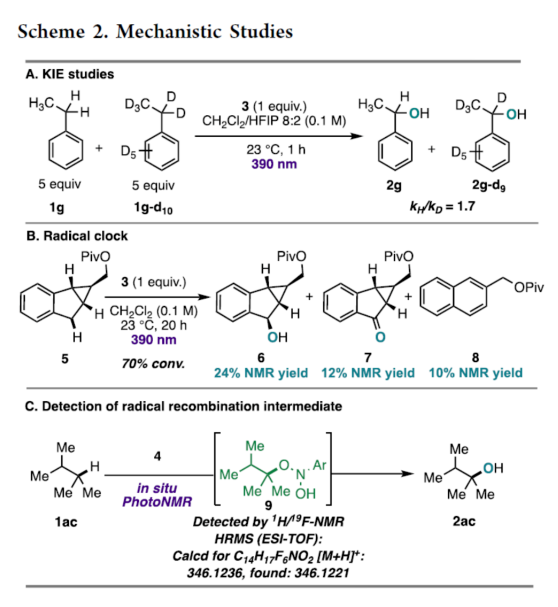
此外,作者還對(duì)反應(yīng)機(jī)理進(jìn)行了進(jìn)一步的研究(Scheme 2)。首先,KIE研究表明,C(sp3)-H鍵與光激發(fā)硝基芳烴的HAT參與了限速步驟(Scheme 2A)。其次,自由基鐘實(shí)驗(yàn)表明,反應(yīng)形成了碳中心的自由基中間體(Scheme 2B)。此外,通過(guò)對(duì)自由基重合中間體的檢測(cè)發(fā)現(xiàn),自由基重組產(chǎn)物(12)的斷裂,可生成所需的C-H羥基化產(chǎn)物(2)和nitrosoarene副產(chǎn)物(Scheme 2C)。
(圖片來(lái)源:J. Am. Chem. Soc.)
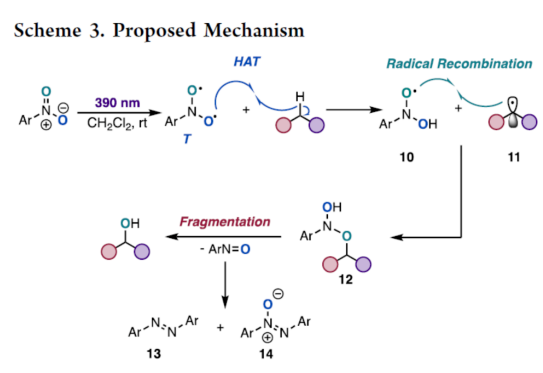
基于上述的研究以及相關(guān)文獻(xiàn)的查閱,作者提出了一種合理的催化循環(huán)過(guò)程(Scheme 3)。首先,硝基芳烴的直接光激發(fā)可生成三重態(tài)雙自由基中間體,可與烷烴中的C(sp3)-H鍵發(fā)生HAT,生成烷基自由基11和以氧中心的二羥基苯胺自由基10。10和11通過(guò)自由基重合后,生成中間體12。最后,12斷裂后,可生成氧原子轉(zhuǎn)移產(chǎn)物和亞硝基副產(chǎn)物,后者在反應(yīng)條件下迅速縮合形成副產(chǎn)物13和14。
(圖片來(lái)源:J. Am. Chem. Soc.)
總結(jié)
美國(guó)紐約大學(xué)Marvin Parasram課題組報(bào)道了一種光激發(fā)硝基芳烴介導(dǎo)脂肪族化合物的無(wú)氧C-H羥基化反應(yīng)。基于光激發(fā)硝基芳烴的雙重官能團(tuán)化的反應(yīng)性,形成的三重態(tài)雙自由基激發(fā)態(tài)可以活化C(sp3)-H鍵和促進(jìn)氧原子轉(zhuǎn)移。值得注意的是,該策略不需要使用額外的氧化劑或過(guò)渡金屬催化劑,具有低成本與高原子經(jīng)濟(jì)性。此外,由于體系的無(wú)氧性質(zhì),一些具有氧化敏感性官能團(tuán)的脂肪族底物,也在未發(fā)生過(guò)度氧化的狀態(tài)下順利進(jìn)行。
文獻(xiàn)詳情:
Joshua M. Paolillo, Alana D. Duke, Emma S. Gogarnoiu, Dan E. Wise, Marvin Parasram*. Anaerobic Hydroxylation of C(sp3)?H Bonds Enabled by the Synergistic Nature of Photoexcited Nitroarenes. J. Am. Chem. Soc. 2023
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn