

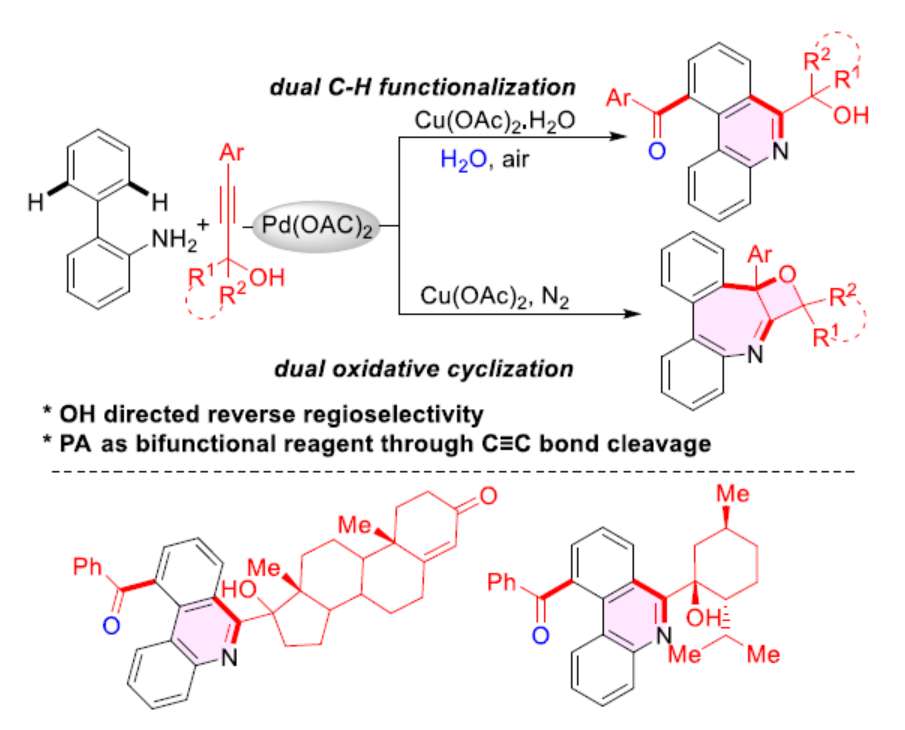
(圖片來源:Angew. Chem. Int. Ed.)
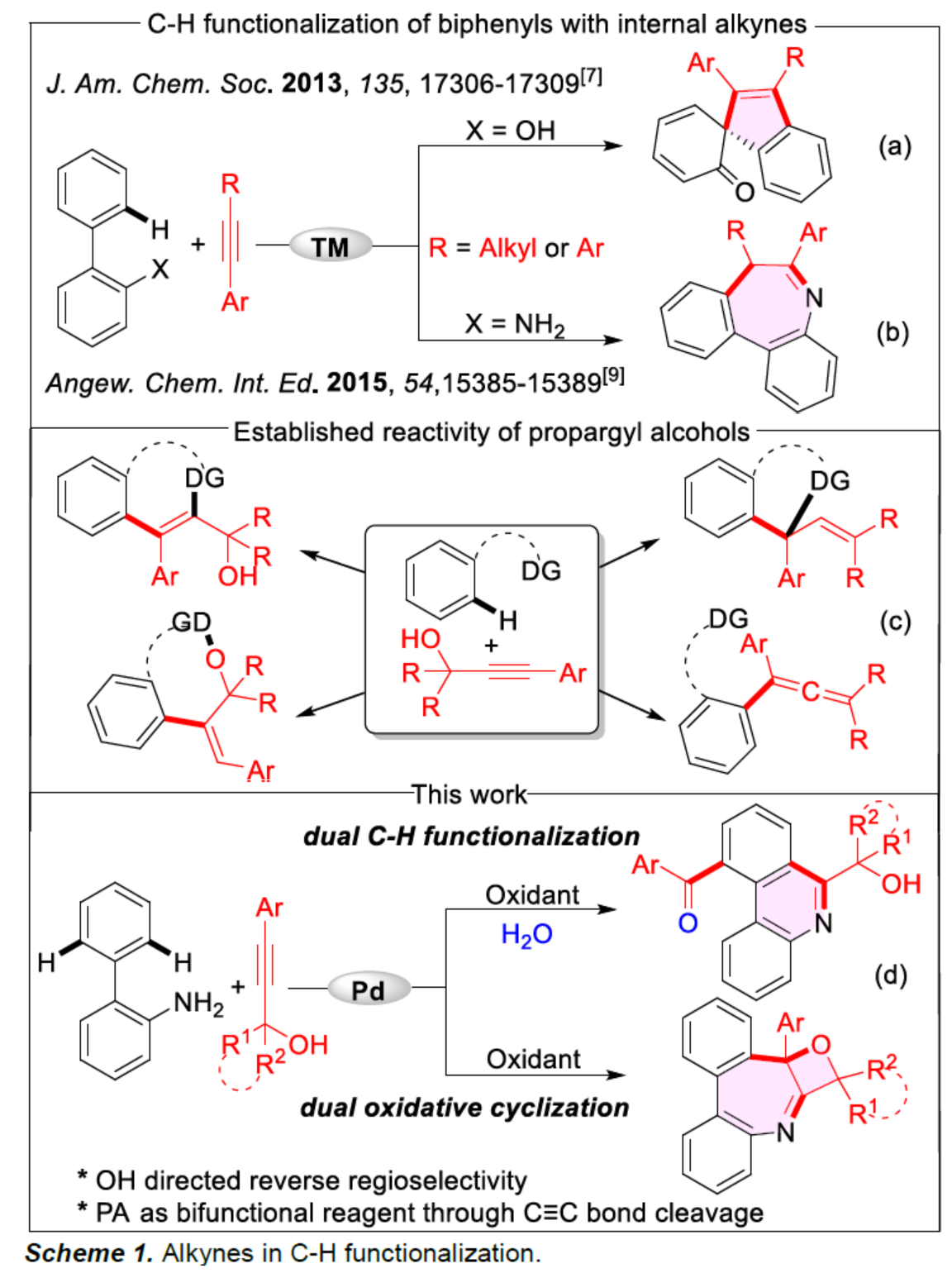
近年來,炔烴的C-H官能團化反應已成為構建環狀骨架的一種有效的途徑。2013年,欒新軍課題組(J. Am. Chem. Soc. 2013, 135, 17306.)報道了一種炔烴與鄰芳基苯酚的環化反應,合成了相應的螺環化產物(Scheme 1a)。沿著這條路線,使用游離胺(-NH2)作為DG一直是一個緊迫的挑戰,并且仍然是當代的焦點領域。2013年,Miura課題組(Org. Lett. 2013, 15, 3990.)報道了聯苯胺的C-H烯基化反應,涉及Ru-催化游離-NH2導向的C-H鍵活化的過程。2015年,欒新軍課題組(Angew. Chem. Int. Ed. 2015, 54, 15385.)報道了一種鈀催化聯苯胺的氧化環化反應(Scheme 1b)。最近,Reddy課題組集中于炔丙醇(PAs)的C-H官能團化反應的研究,這是因為羥基與過渡金屬催化劑的配位可使反應具有優異的區域和化學選擇性(Scheme 1c)。通常,PAs作為兩個碳單位的合成子可進行形式[4+2]環化反應,而在一些脫水偶聯反應中,它們也可作為一個碳單位的合成子。此外,化學家們還報道了幾例利用羥基的氧實現了相應的[3+3]環化反應。近日,印度化學技術研究所Maddi Sridhar Reddy課題組報道了一種Pd-催化雙重C-H官能團化反應,涉及PAs中C≡C氧化斷裂的過程(Scheme 1d)。值得注意的是,這是PAs首次用作非對稱雙重C-H官能團化反應中雙官能團化試劑。此外,通過進一步條件的優化,還可實現聯苯胺的雙重氧化環化反應,合成了一系列稠合的氧雜環丁烷衍生物。
(圖片來源:Angew. Chem. Int. Ed.)
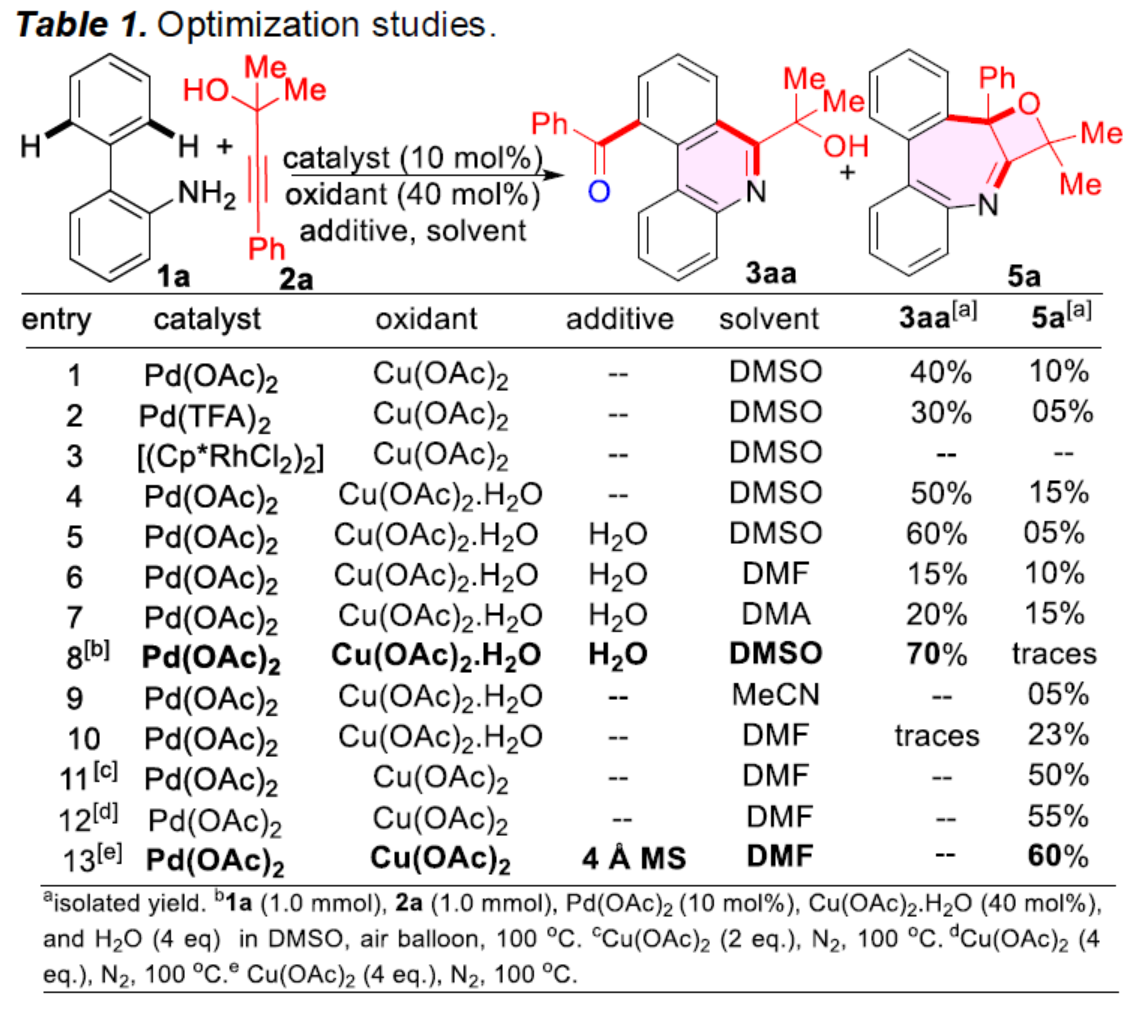
首先,作者以聯苯胺1a與炔丙醇2a作為模型底物,進行了相關反應條件的篩選(Table 1)。當以Pd(OAc)2作為催化劑,Cu(OAc)2·H2O作為氧化劑,H2O作為添加劑,在DMSO溶劑中100 oC反應,可以70%的收率得到雙重C-H官能團化產物3aa。此外,當以Pd(OAc)2作為催化劑,Cu(OAc)2作為氧化劑,4 ?分子篩作為添加劑,在DMF溶劑中100 oC反應,可以60%的收率得到雙重氧化環化產物5a。
(圖片來源:Angew. Chem. Int. Ed.)
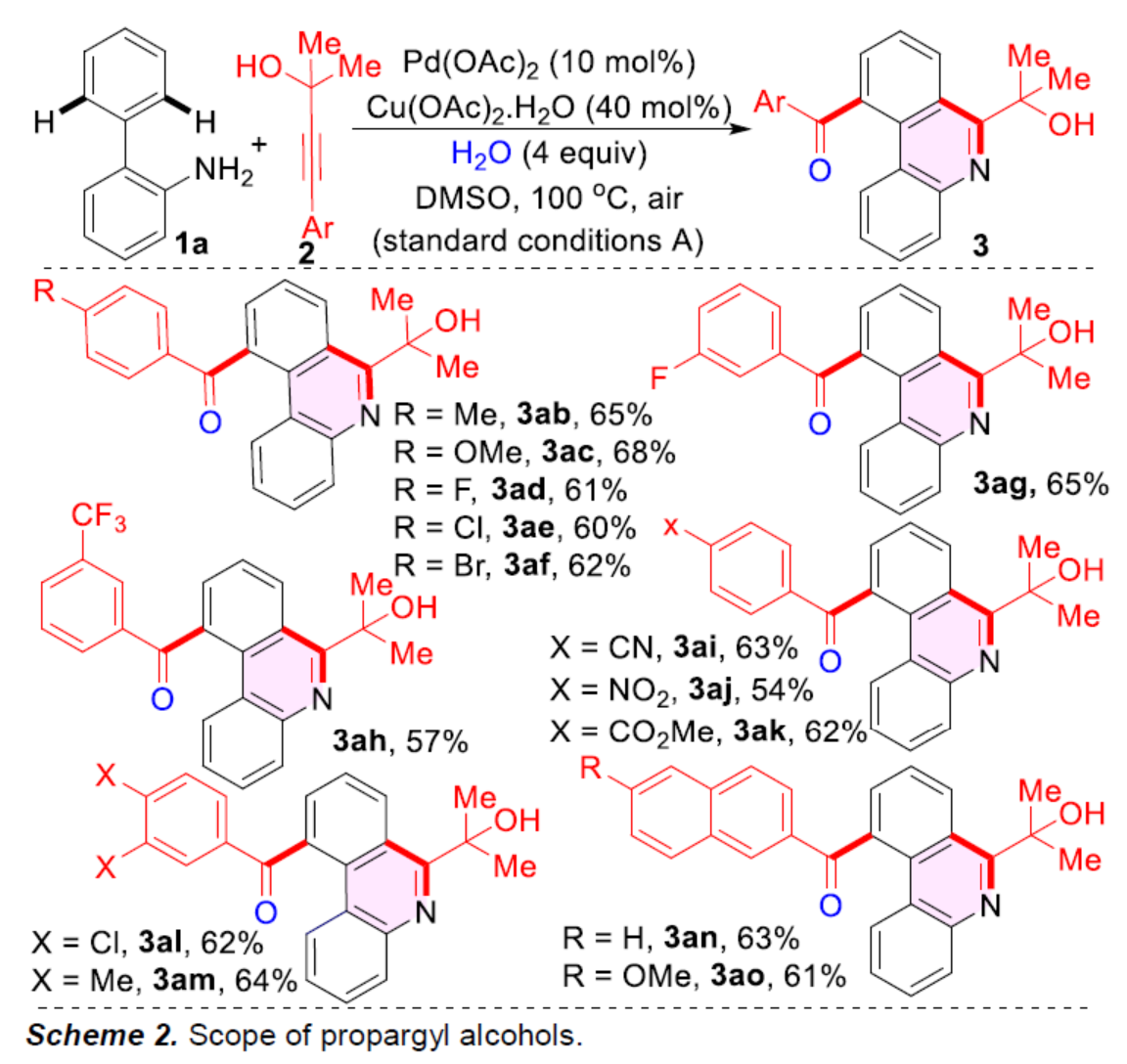
在獲得上述最佳反應條件后,作者對炔丙醇2的底物范圍進行了擴展(Scheme 2)。研究表明,當炔丙醇底物2的末端含有一系列不同電性取代的芳基與萘基時,均可順利進行反應,獲得相應的產物3ab-3ao,收率為54-68%。
(圖片來源:Angew. Chem. Int. Ed.)
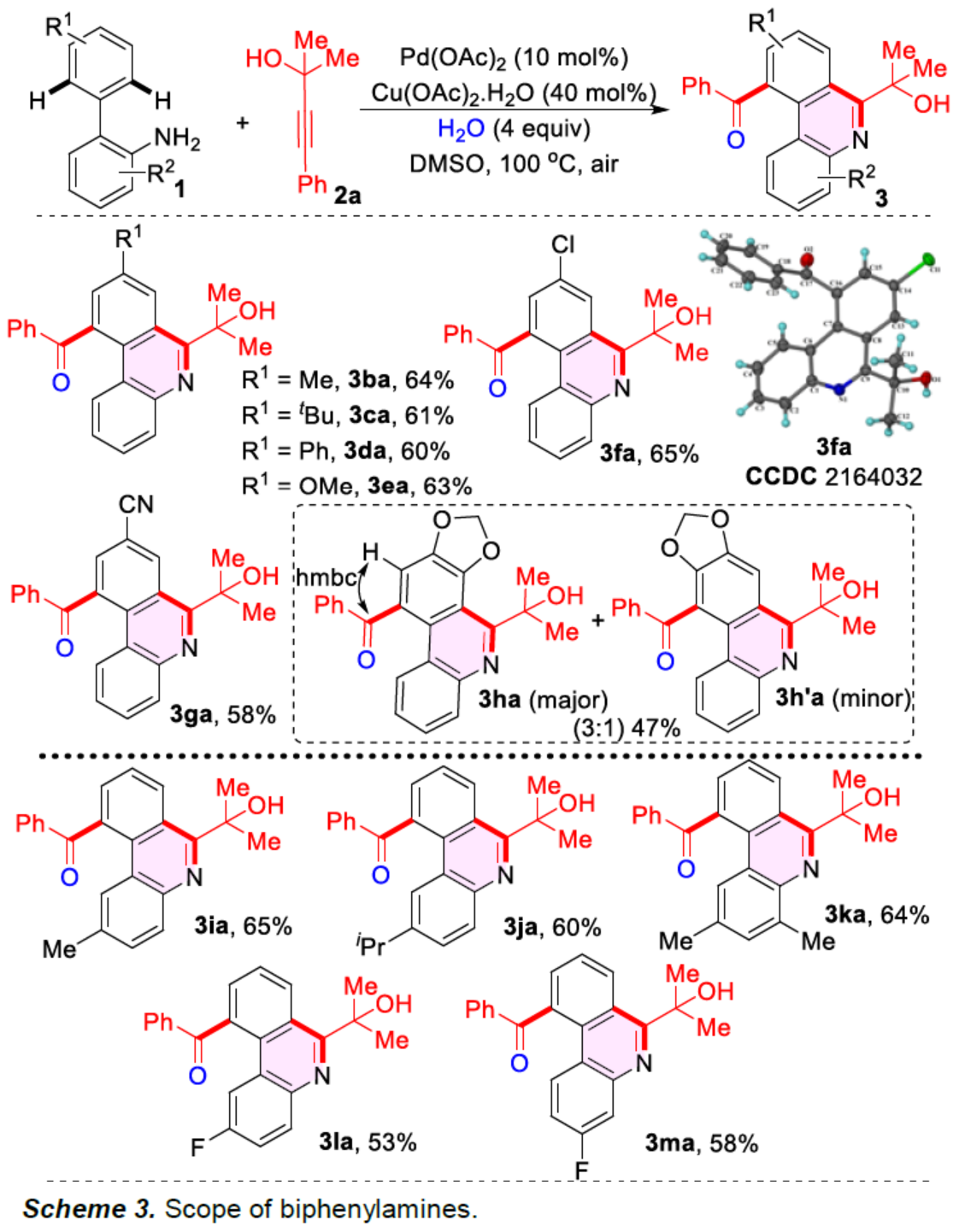
緊接著,作者對聯苯胺1的底物范圍進行了擴展(Scheme 3)。研究表明,當底物1中的R1為-Me、-tBu、-Ph、-OMe、-Cl、-CN時,均可順利反應,獲得相應的產物3ba-3ga,收率為58-65%。由于空間位阻的原因,含有亞甲二氧基取代的底物1h,獲得區域異構體的混合物3ha和3h'a(比例為3:1),收率為47%。當底物1中的R2為-Me、-iPr、-F時,也與體系兼容,獲得相應的產物3ia-3ma,收率為53-65%。
(圖片來源:Angew. Chem. Int. Ed.)
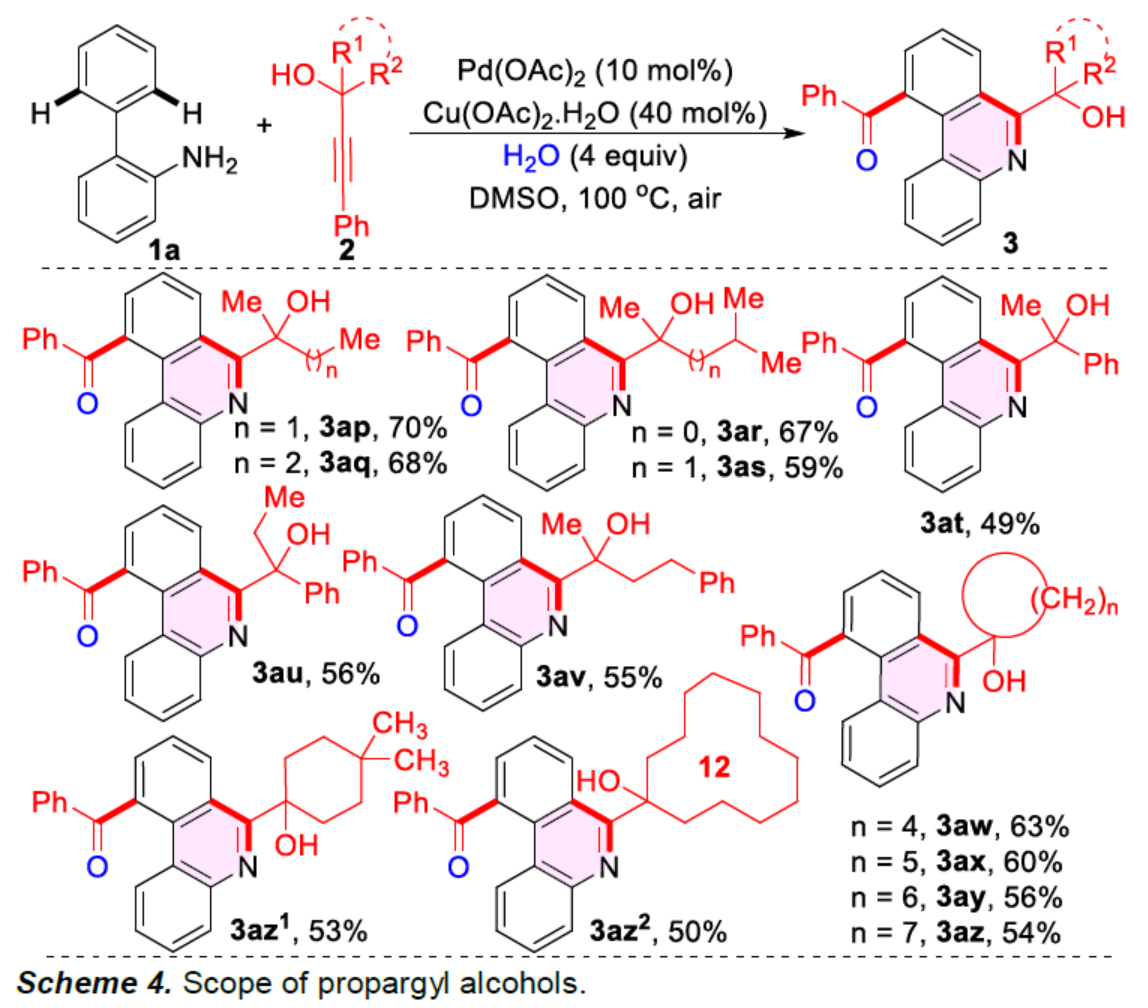
隨后,作者繼續對炔丙醇2的底物范圍進行了擴展(Scheme 4)。研究表明,當底物2中得R1與R2為不同的烷基與芳基取代時,均可順利進行反應,獲得相應的產物3ap-3av,收率為49-70%。當底物2中得R1與R2為相連的環狀烷基鏈時,也與體系兼容,獲得相應的產物3aw-3az2,收率為50-63%。
(圖片來源:Angew. Chem. Int. Ed.)
同時,該策略還可用于一些結構復雜天然產物的后期衍生化,獲得相應的產物4a-4d,收率為47-60%(Scheme 5)。

(圖片來源:Angew. Chem. Int. Ed.)
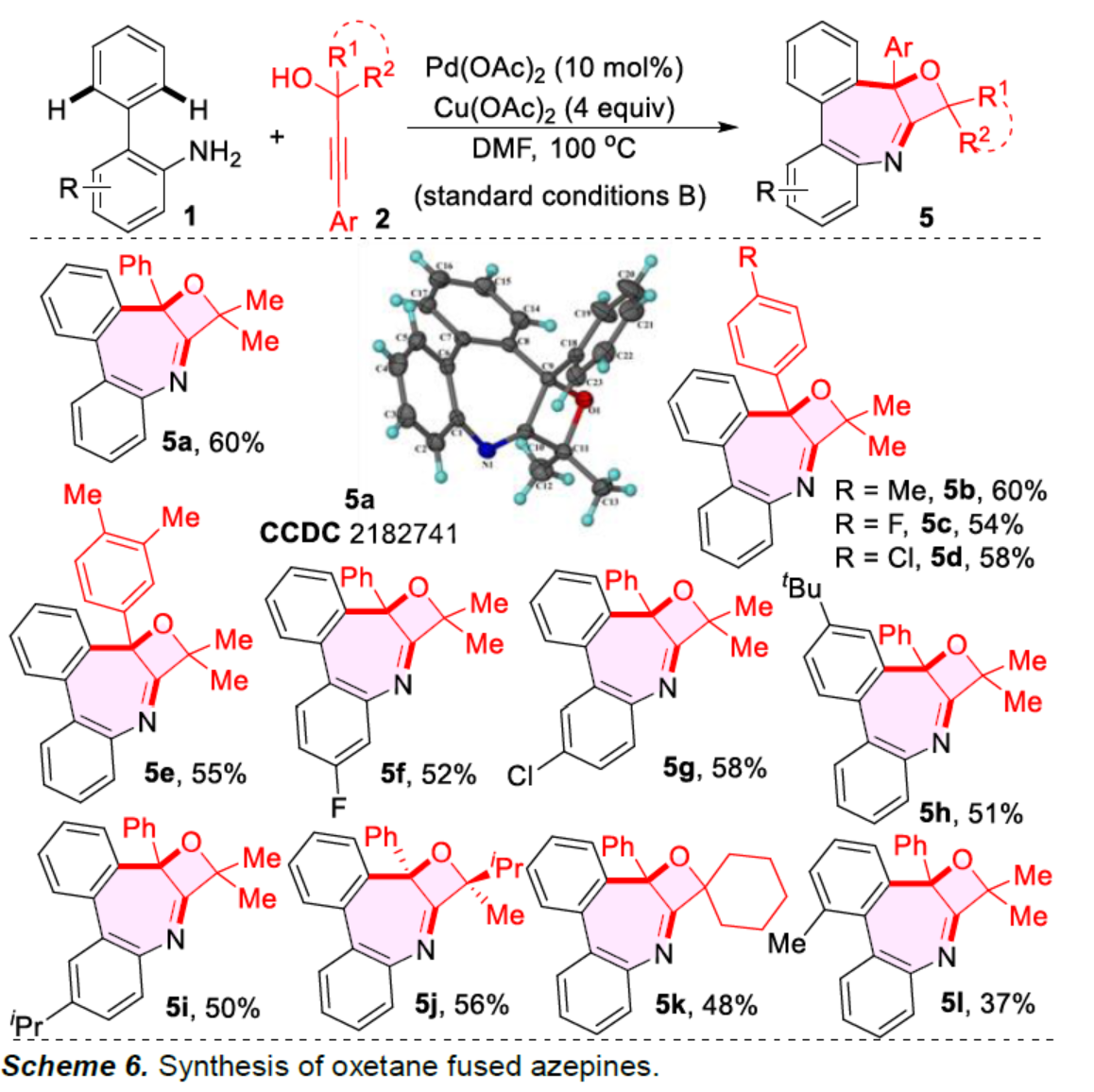
此外,在標準條件下(standard conditions B),一系列不同取代的聯苯胺1與炔丙醇2,均可順利發生雙重氧化環化反應,獲得相應的稠合氧雜環丁烷衍生物5a-5l,收率為37-60%(Scheme 6)。
(圖片來源:Angew. Chem. Int. Ed.)
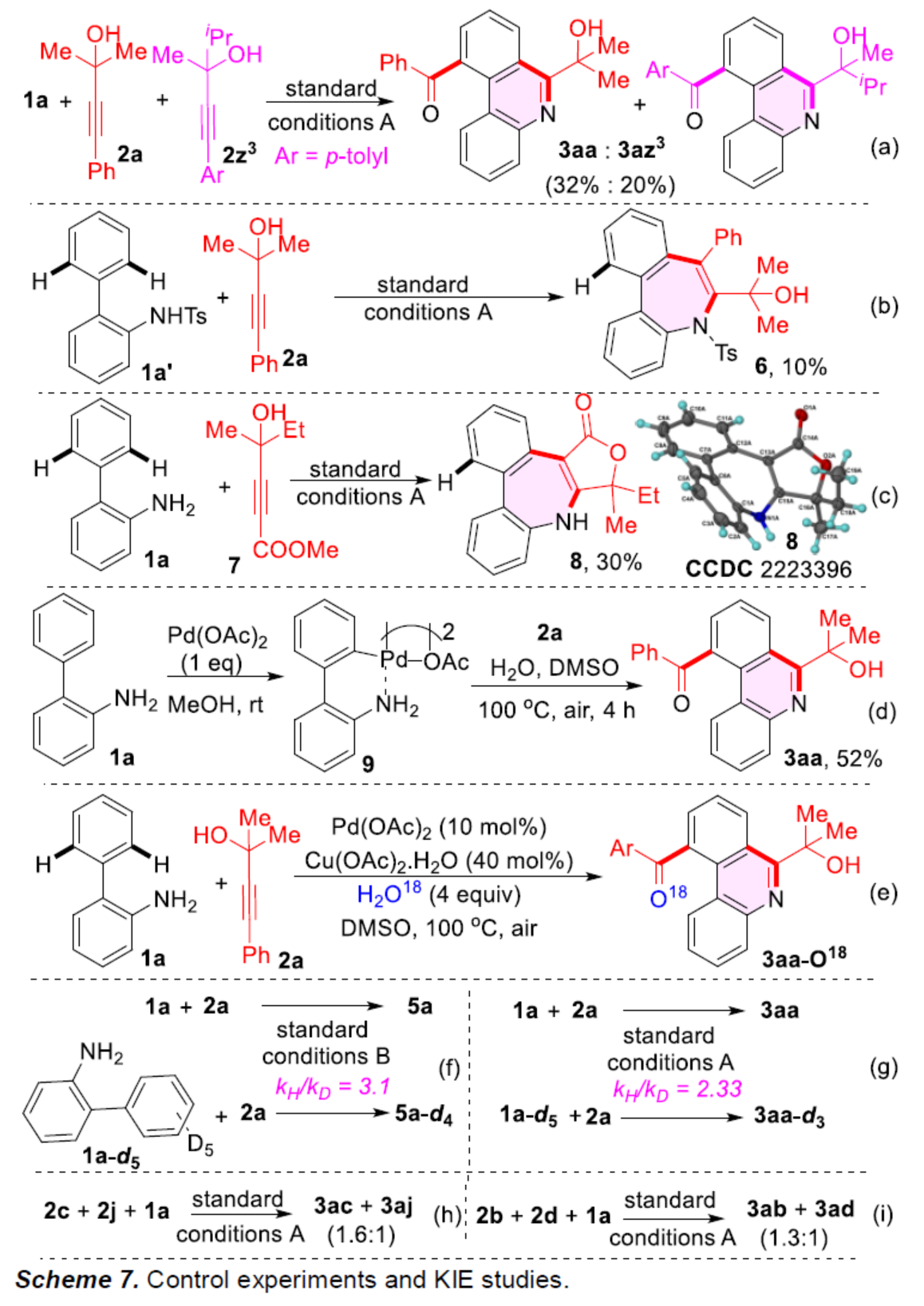
為了進一步了解反應的機理,作者進行了相關的實驗研究(Scheme 7)。首先,1a、2a和2z3之間的實驗,僅生成3aa和3az3,未獲得交叉產物,從而表明鍵的斷裂發生在切斷部分,在整個反應過程中與基本分子保持完整(Scheme 7a)。不含游離羥基的炔烴,未能生成所需產物,從而表明羥基螯合在區域選擇性環化以及中間體向所需產物的分布中的重要性。當使用受保護的聯苯胺1a’與2a反應時,反應僅獲得環化產物6,從而表明游離胺對于轉化是必需的(Scheme 7b)。羥基炔酸酯7與1a反應,可獲得環化內酯化產物8,8未能與水進一步反應,從而表明了游離羥基的作用(Scheme 7c)。其次,通過乙酸鈀與1a的化學計量實驗表明,反應是通過胺輔助鈀的C-H插入而開始的(Scheme 7d)。通過氘代實驗表明,產物中的氧來源于水中的氧(Scheme 7e)。通過KIE實驗表明,初始C-H鍵的斷裂可能參與了決速步驟(Scheme 7f-7g)。此外,通過競爭性實驗表明,富電子炔烴更容易進行所需的配位和碳金屬化(Scheme 7h-7i)。
(圖片來源:Angew. Chem. Int. Ed.)
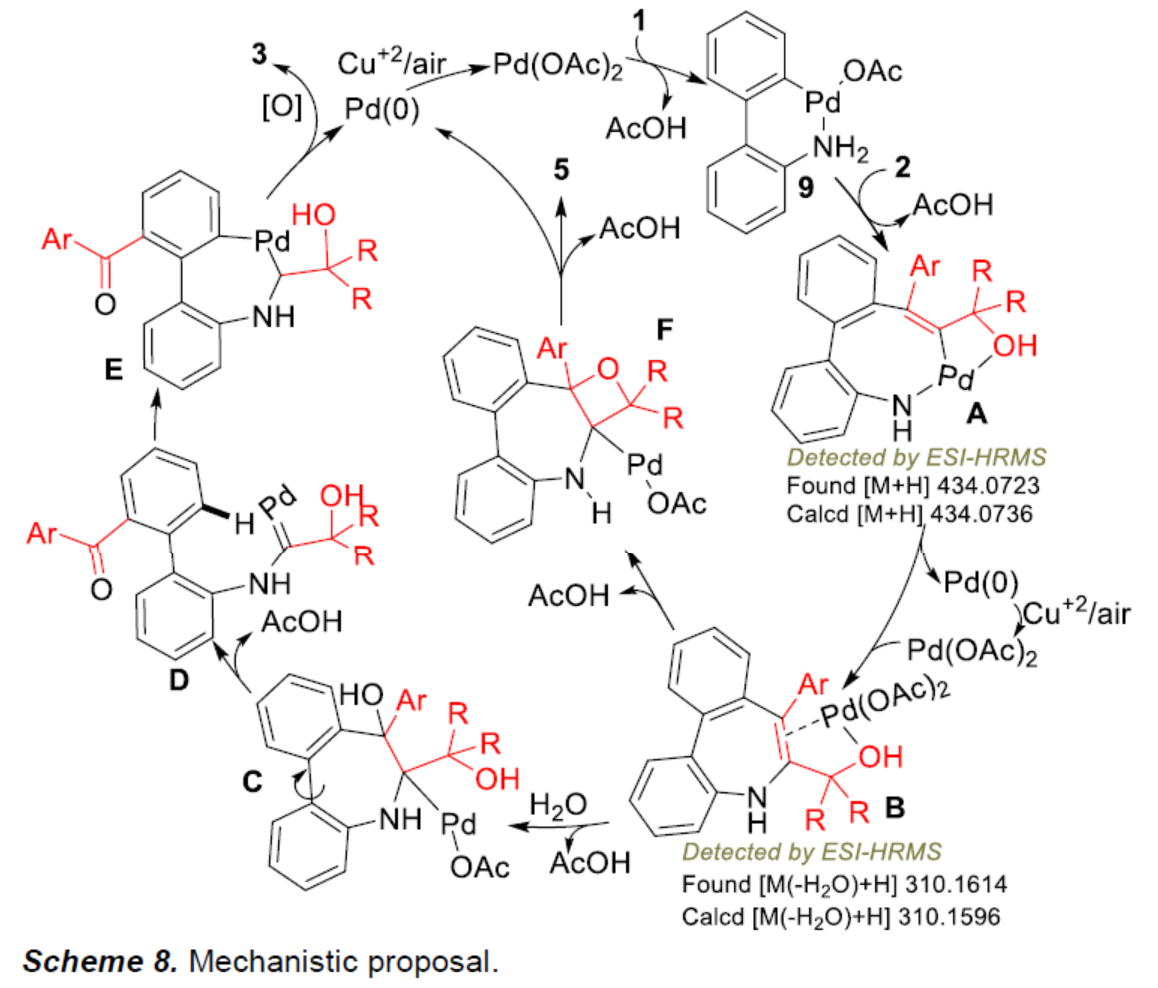
基于上述的研究以及相關文獻的查閱,作者提出了一種合理的催化循環過程(Scheme 8)。首先,1與Pd(OAc)2經胺輔助的C-H鍵的活化,可生成鈀環中間體9。在金屬和羥基之間的配位幫助下,炔烴可進行區域選擇性插入,生成中間體A。中間體A經還原性消除后,可生成中間體B。其次,在配位的幫助下,活化烯烴B可選擇性地進行親核進攻H2O,生成中間體C。中間體C經C-C鍵斷裂,可生成關鍵的金屬卡賓D,其立即插入另一個C-H鍵后生成中間體E。中間體E經還原消除以及氧化后,可獲得目標產物3。此外,在體系無水的情況下,炔丙基羥基進攻活化的烯烴生成氧雜環丁烷環(B至F),其中鈀通過β-H氫消除后,獲得目標產物5。
(圖片來源:Angew. Chem. Int. Ed.)
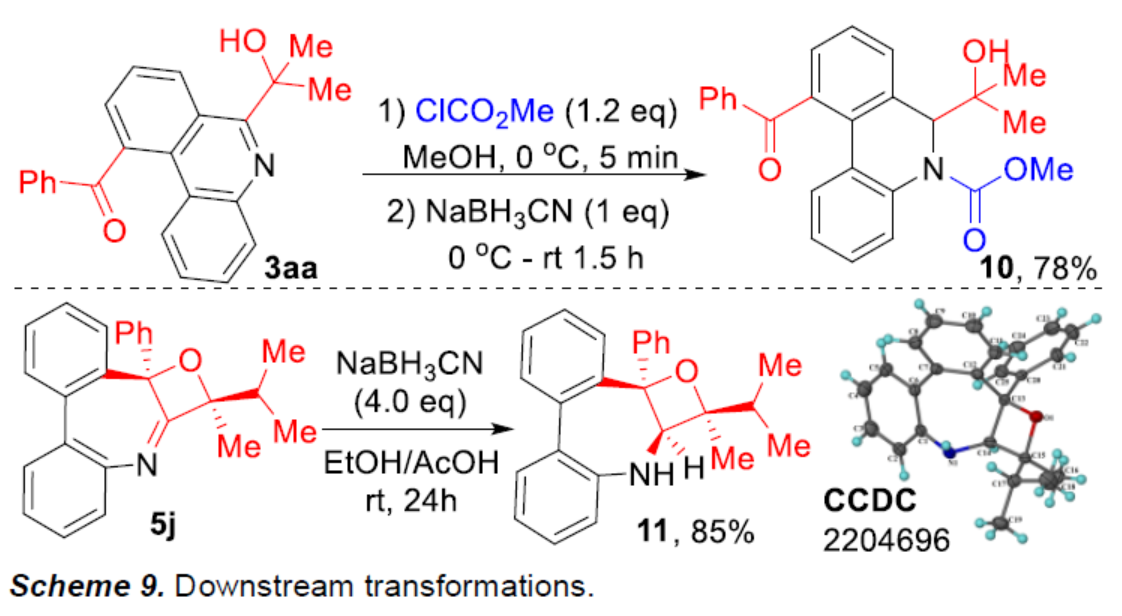
最后,作者進行一些下游轉化,進一步表明了反應的實用性(Scheme 9)。3aa經還原后,可以78%的收率得到5,6-二氫菲啶10。5j經還原后,可以85%的收率得到具有三個連續手性中心的氧雜環丁烷產物11,為單一的非對映體。
(圖片來源:Angew. Chem. Int. Ed.)
總結
印度化學技術研究所Maddi Sridhar Reddy課題組首次報道了一種使用炔丙醇(PAs)作為雙官能團化試劑,實現了聯苯胺的非對稱雙重C-H官能團化反應。同時,通過反應條件的調節,還可實現聯苯胺的雙重氧化環化反應。其次,該反應具有底物范圍廣泛、反應條件溫和等特點,并可用于天然產物的后期衍生化。此外,通過相關的控制實驗表明,反應涉及鈀卡賓中間體的形成。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn