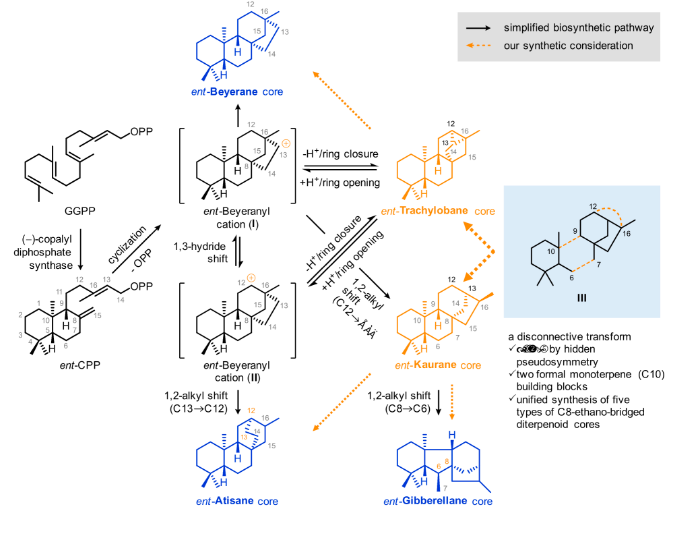
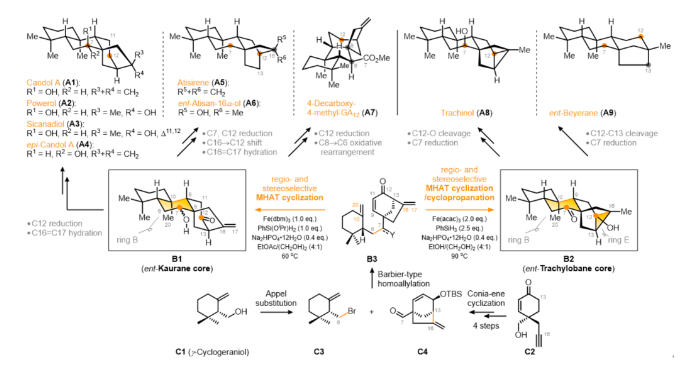
作為四環二萜天然產物的重要成員,C8-成橋環的二萜 (C8-Ethano-Bridged Diterpenoids) 廣泛分布于唇形科 (Lamiaceae) 香茶菜屬 (Isodon) 植物中。迄今為止,已有超過1500個C8成橋環的二萜化合物被分離鑒定,且其具有復雜多變的骨架結構和顯著多樣的生物活性,因此該類天然產物一直是天然產物化學家、有機合成化學家和藥物化學家的重要研究對象。自1962年Ireland首次報道了外消旋貝殼杉烯 (dl-Kaurene) 全合成工作以來,國內外諸多課題組先后報道了多類四環二萜天然產物的合成研究工作。C8-成橋環的二萜化合物主要包括“映-貝殼杉烷、映-阿替生烷、映-貝葉烷、映-綽奇烷、映-赤霉烷、扁枝杉烷和木藜蘆烷”等七種類型。如圖1所示,在已報道的C8-成橋環的二萜生源合成過程中,香葉基香葉基焦磷酸 GGPP (Geranylgeranyl Pyrophosphate) 在 ent-CPP 合成酶 (ent-CPP Synthase) 催化下形成ent-CPP (ent-Copalyl Diphosphate),隨后經過貝殼杉烷合成酶 (ent-Kaurene Synthases) 催化和分子內環化形成映-貝葉烷正離子,再分別經過1,3-氫遷移、1,2-烷基遷移、環化和縮環轉化,生成映-貝葉烷、映-阿替生烷、映-貝殼杉烷、映-綽奇烷和映-赤霉烷多環骨架。受此生源過程的啟發,作者設想通過共同的高級中間體,實現五種類型C8-成橋環的二萜化合物的多樣性全合成。圖1. 已知C8-成橋環的二萜生源途徑與作者的合成設想(圖片來源:J. Am. Chem. Soc.)如圖2所示,基于上述的合成考慮和分子自身的潛在對稱性,作者以手性天然單萜γ-環香葉醇C1 (γ-Cyclogeraniol) 和文獻已知的手性γ-季碳環己烯酮C2為起始原料,分別通過Appel取代和Conia-ene環化為關鍵反應的多步化學轉化,完成了高烯丙基溴化物C3和[3.2.1]橋環合成砌塊C4的的制備。利用Barbier-type高烯丙基化反應,實現了C6-C7的直接構建,完成了三環中間體B3的合成。需要指出的是,C7和C12氧化態的引入,為后續天然產物骨架的快速轉化提供了可能。在此基礎上,以關鍵的Fe(III)-促進的氫原子轉移“自由基環化反應”以及“自由基環化/環丙化反應”,分別實現了映-貝殼杉烷骨架中B環與映-綽奇烷骨架中B/E環的構建。經過氧化態調整和骨架轉化,最終以8至11步完成了五種類型、9個C8-成橋環的二萜全合成研究,其中6個天然產物 (Candol A、Powerol、Sicanadiol、epi-Candol A、ent-Atisan-16α-ol和Trachinol) 屬于首次合成報道。圖2. C8-成橋環的二萜多樣性合成 (圖片來源:J. Am. Chem. Soc.)
樊春安課題組基于已知的生源轉化途徑分析,以目標分子中的潛在對稱性為驅動,發展了以Fe(III)-促進的區域和立體選擇性的氫原子轉移“自由基環化反應”和“自由基環化/環丙化反應”為關鍵步驟發散性合成策略,簡潔、高效地實現了4個映-貝殼杉烷二萜 (Candol A、Powerol、Sicanadiol和epi-Candol A)、2個映-阿替生烷二萜 (Atisirene和ent-Atisan-16α-ol)、1個映-赤霉烷二萜 (4-Decarboxy-4-methylGA12)、1個映-綽奇烷二萜 (Trachinol) 和1個映-貝葉烷二萜 (ent-Beyerane) 的集群式合成。該研究工作不僅探討了Fe(III)-介導的氫原子轉移環化反應在C8-成橋環的二萜多樣性全合成中的可能性,同時為高氧化態四環二萜類天然產物及其類似物的合成研究奠定了基礎。
文獻詳情:
Xian-He Zhao, Le-Le Meng, Xiao-Tao Liu, Peng-Fei Shu, Cheng Yuan, Xian-Tao An, Tian-Xi Jia, Qi-Qiong Yang, Xiang Zhen, Chun-An Fan*. Asymmetric Divergent Synthesis of ent-Kaurane-, ent-Atisane-, ent-Beyerane-, ent-Trachylobane-, and ent-Gibberellane-type Diterpenoids. J. Am. Chem. Soc. 2022, https://doi.org/10.1021/jacs.2c09985