



有機硅化合物在化學(xué)工業(yè)和材料科學(xué)中具有重要的價值。具有Si-H鍵的有機硅烷在各種轉(zhuǎn)化中作為氫原子或者氫化物給體尤其重要。就像強大的烯烴復(fù)分解反應(yīng)可以從廉價的烯烴獲得高附加值的烯烴一樣,選擇性的硅烷再分配反應(yīng)(即硅氫鍵和硅碳鍵的交換)也可能具備從兩個簡單硅烷制備高級硅烷的潛力。盡管HSiCl3的自身再分配反應(yīng)已經(jīng)是制備SiH4的工業(yè)手段,但是選擇性交叉再分配反應(yīng)仍是一個巨大的挑戰(zhàn)。要獲得高的交叉再分配選擇性,需要克服以下幾個困難(圖1):(1)如何抑制自身再分配反應(yīng);(2)如何抑制硅烷脫氫偶聯(lián)的副反應(yīng);(3)如何避免新形成的硅氫鍵的過度反應(yīng)?以往的工作大多是通過生成硅烷氣體來促進反應(yīng),是一種熵驅(qū)動的策略。最近,武漢大學(xué)高等研究院的沈曉課題組首次報道了鎳催化硅烷和苯并硅雜環(huán)丁烷的交叉再分配反應(yīng)合成雙硅化合物, 利用焓驅(qū)動的策略實現(xiàn)了高選擇性的交叉再分配反應(yīng)。
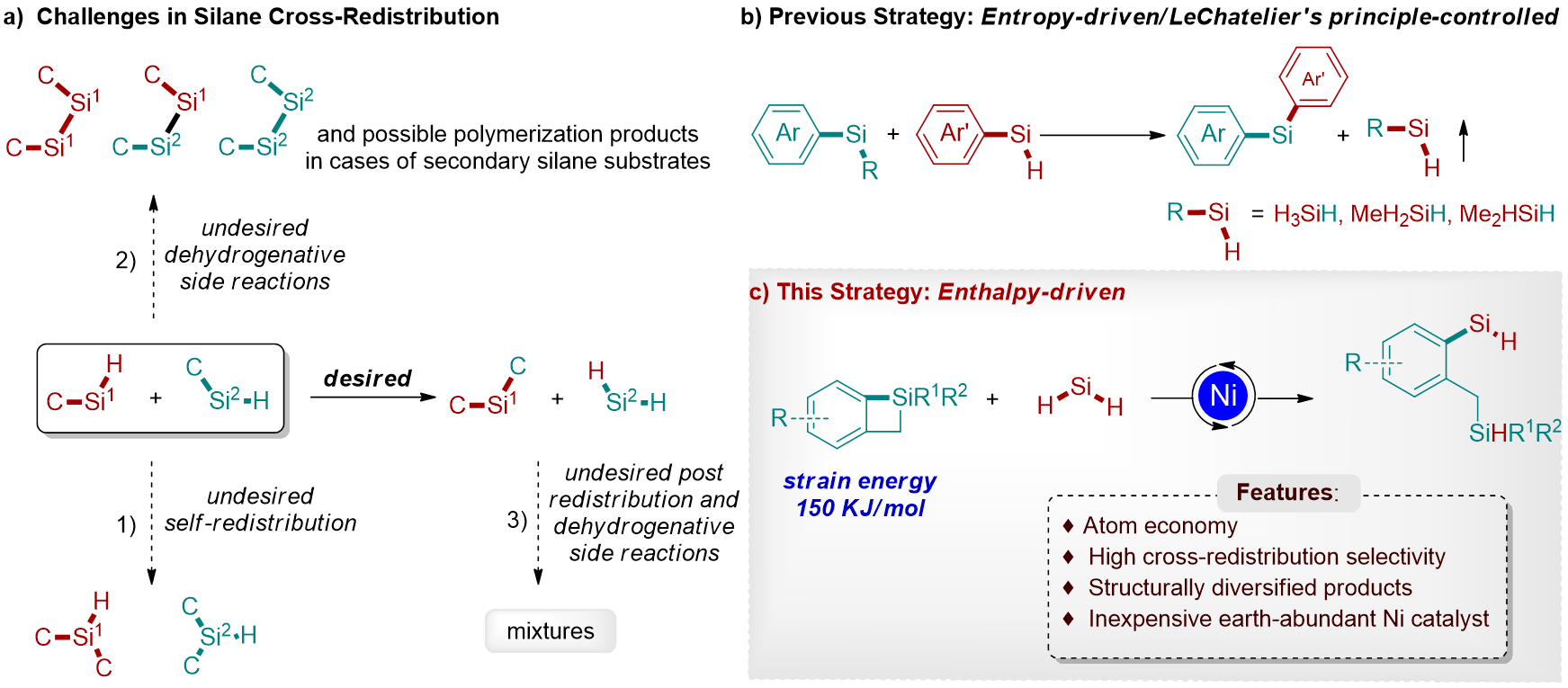
圖1: 硅烷再分配反應(yīng)研究背景和本文的策略
經(jīng)過一系列條件篩選,作者確定了最優(yōu)條件為:當(dāng)Ni(COD)2的摩爾分數(shù)為10 mol%,(p-MeC6H4)3P的摩爾分數(shù)為20 mol%時,反應(yīng)在40 oC下3 h內(nèi)完成,以90%的產(chǎn)率得到所需的交叉再分配產(chǎn)物3a,并在此條件下對底物進行拓展。該反應(yīng)具有廣泛的底物范圍,對于二芳基硅烷、一芳基一烷基硅烷、兩烷基硅烷、三芳基硅烷、三烷基硅烷以及烷基芳基的三取代硅烷均能取得中等到良好的收率。其中包括含有供電子取代基、吸電子取代基和雜原子取代的硅烷底物。值得提出的是,對于工業(yè)上常用的硅氧烷和氯硅烷底物,也能在該條件下順利反應(yīng)得到雙硅化合物。對于天然氨基酸衍生的復(fù)雜硅烷底物也能參與到反應(yīng)中以中等收率得到相應(yīng)的雙硅產(chǎn)物(圖2)。
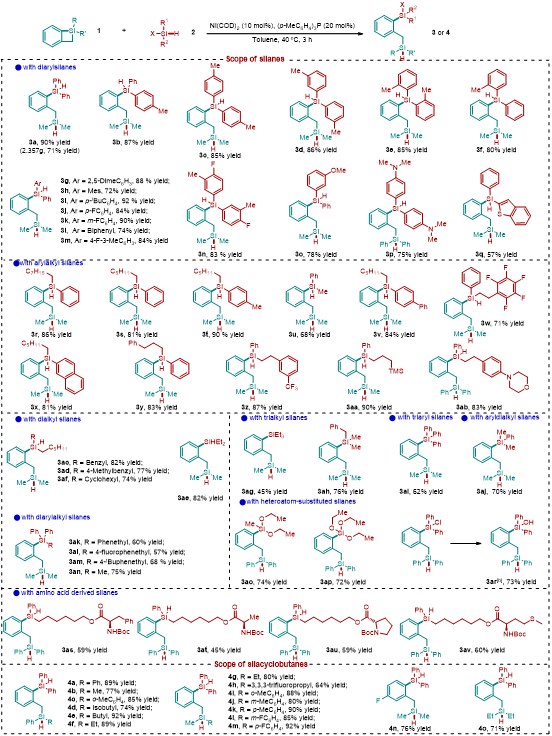
圖2: 底物拓展
隨后作者嘗試對含有硅氫的雙硅化合物進行轉(zhuǎn)化。通過Rh催化的分子內(nèi)脫氫反應(yīng),3a以81%的產(chǎn)率轉(zhuǎn)化為環(huán)雙硅化合物5。除了過渡金屬催化劑外,B(C6F5)3在硅氫化反應(yīng)中也表現(xiàn)出良好的性能。作者以5%的B(C6F5)3為催化劑,實現(xiàn)了丙酮的硅氫化反應(yīng),合成了六元環(huán)硅氧烷6,產(chǎn)率84%。在類似條件下,苯甲腈經(jīng)歷可能的中間體7經(jīng)水解后,以84%的產(chǎn)率得到苯甲胺8。當(dāng)硅上取代基的電性不同時,硅氫的反應(yīng)活性是不同的,作者利用這一特性實現(xiàn)了在同一個分子中有兩個硅氫鍵的選擇性硅氫化,在B(C6F5)3的催化下4b能與苯乙烯反應(yīng),選擇性的在烷基取代的硅氫鍵上發(fā)生硅氫化以78%的收率得到化合物9。剩余的一個硅氫也可以在堿性條件下高效的被轉(zhuǎn)化為硅羥基,以81%的收率得到化合物10。通過C-H硅烷化反應(yīng)合成六元硅雜環(huán)化合物更具挑戰(zhàn)性,因為需要生成高能量的七元環(huán)金屬中間體。作者發(fā)現(xiàn)了一種Rh催化分子內(nèi)碳氫鍵硅基化反應(yīng),以硅烷再分配產(chǎn)物為底物來實現(xiàn)此類分子的構(gòu)建。結(jié)果表明,以[Rh(COD)Cl]2為催化劑,Xantphos為配體,在甲苯中反應(yīng)效果較好,以60%~80%的產(chǎn)率合成了11a到11h的二硅苯并環(huán)己烷(圖3)。這些后續(xù)化學(xué)轉(zhuǎn)化都展示了作者開發(fā)的方法學(xué)的合成應(yīng)用價值。
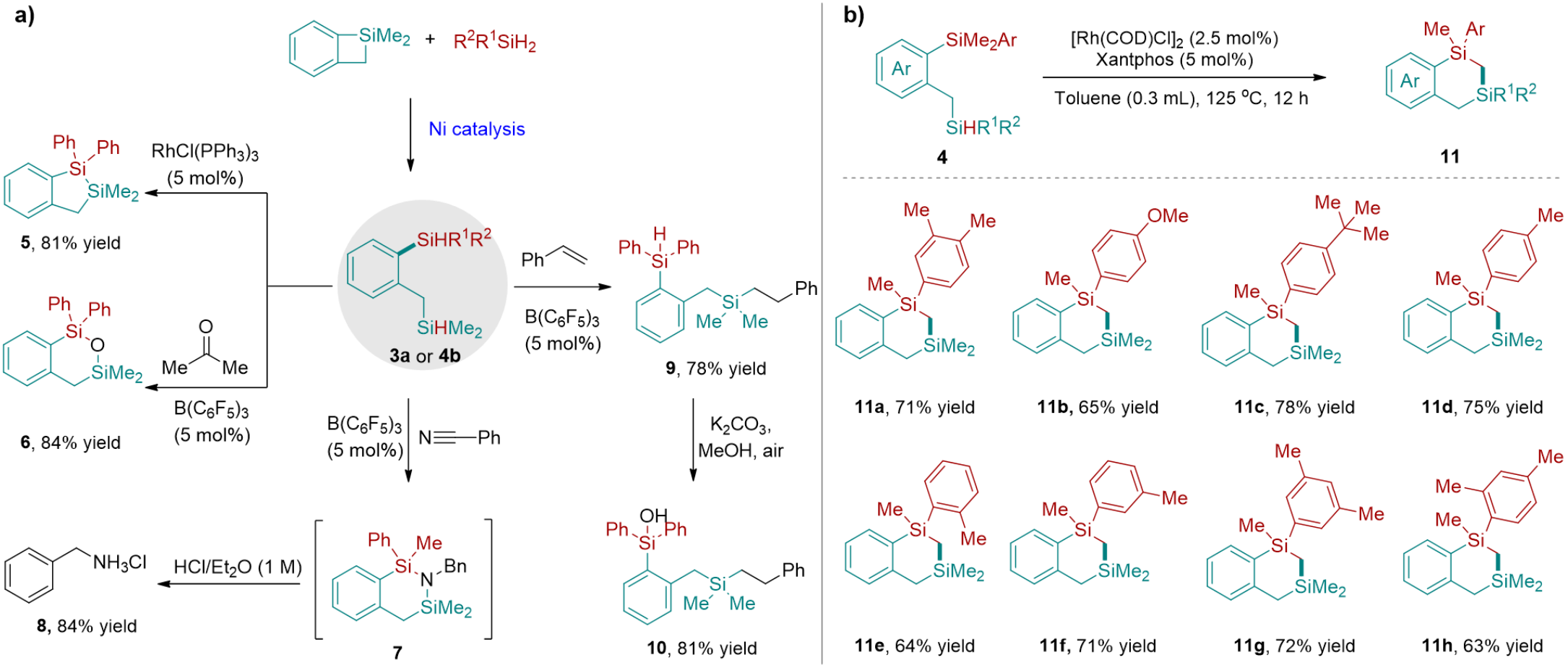
圖3: 雙硅產(chǎn)物的轉(zhuǎn)化與應(yīng)用
為了更加深入的了解硅烷與環(huán)硅化合物的再分配反應(yīng)的機理,作者進行了一系列的機理驗證實驗,并結(jié)合DFT計算,對這個反應(yīng)的機理進行研究。首先,為了探究反應(yīng)是否經(jīng)歷自由基的歷程,作者在標準模板反應(yīng)中加入自由基抑制劑TEMPO,反應(yīng)可以進行,這表明產(chǎn)物的形成不太可能涉及自由基機制(圖4-a)。在模板反應(yīng)中,作者將Ph2SiH2替換為Ph2SiD2,發(fā)現(xiàn)產(chǎn)物中的硅氫均是氘代的硅氫,說明產(chǎn)物中的氫來源于硅烷(圖4-b)。當(dāng)將Ph2SiH2/Ph2SiD2(1:1)混合加入到模板反應(yīng)中時,KIE只有1.08左右,并沒有發(fā)現(xiàn)大的KIE效應(yīng)(圖4-c)。為了更清楚的了解硅氫鍵的斷裂過程,作者還進行了平行實驗進行KIE的探究,得到KIE的數(shù)值為1(圖4-d),說明在這個反應(yīng)中硅氫鍵的斷裂在動力學(xué)上并不顯著,也就是說硅氫鍵的斷裂并沒有參與到?jīng)Q速步中。作者對反應(yīng)組分的動力學(xué)進行了研究(圖4-e)。作者首先研究了Ph2SiH2不同濃度下的初始速率,發(fā)現(xiàn)該速率對Ph2SiH2的濃度呈現(xiàn)零級動力學(xué)效應(yīng),這與KIE結(jié)果一致,表明Ph2SiH2的Si-H鍵的斷裂不參與到?jīng)Q速步中。然后作者接著研究了催化劑和1a不同濃度下的初始速率,發(fā)現(xiàn)反應(yīng)速率與催化劑(Ni(COD)2+2(p-MeC6H4)3P)和1a的濃度呈一級動力學(xué)效應(yīng),表明1a在催化劑作用下C-Si鍵的斷裂可能是反應(yīng)的決速步驟。
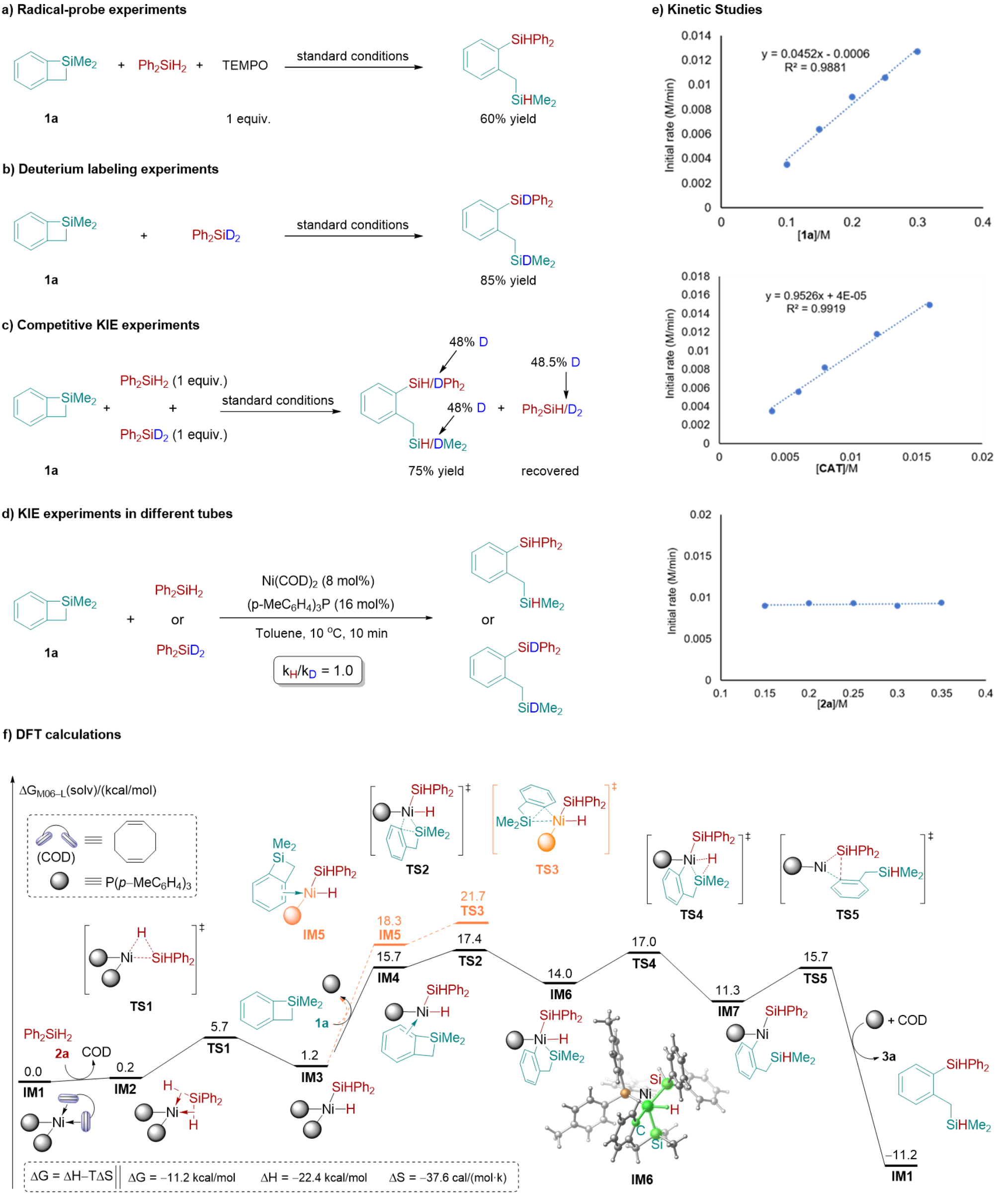
圖4: 機理研究與DFT計算
基于這些實驗結(jié)果和有關(guān)鎳催化反應(yīng)的相關(guān)報道,作者提出了一個可能的鎳催化二苯基硅烷和苯并四元環(huán)硅的交叉再分配反應(yīng)的催化循環(huán)機理。如圖5所示,首先Ni(COD)2和2(p-MeC6H4)3P絡(luò)合配位生成零價鎳物種I與Ph2SiH2發(fā)生配體交換得到中間體II, 然后Ni(0)與二苯基硅烷的硅氫鍵發(fā)生氧化加成生成二價鎳中間體III.隨后苯并環(huán)硅的硅碳鍵與二價鎳中間體III發(fā)生氧化加成得到四價鎳中間體IV。最后,硅氫鍵與硅碳鍵分別發(fā)生還原消除得到目標產(chǎn)物3a并重生了催化劑活性物種I。DFT計算的結(jié)果進一步支持了作者提出催化循環(huán)機理,反應(yīng)整個歷程的吉布斯自由勢能如圖4-f所示。Ni(0)中間體IM1與二苯基硅烷2a發(fā)生配體交換生成中間體IM2所需要的能量僅為0.2 kcal/mol。隨后硅氫鍵的氧化加成經(jīng)過過渡態(tài)TS1生成Ni(II)-中間體IM3所需要的的能量為5.5 kcal/mol。這個計算結(jié)果表明零價鎳可以很容易的被二苯基硅烷氧化為二價鎳。另一種硅烷底物苯并四元環(huán)硅1a可以通過配體交換與Ni(II)中心配位,后續(xù)發(fā)生的配體交換如果發(fā)生在鎳上氫原子的反式會生成中間體IM5,相應(yīng)的通過過渡態(tài)TS3的Si-C鍵氧化加成反應(yīng)需要21.7 kcal/mol的活化自由能。當(dāng)配體交換發(fā)生在鎳上硅原子的反式會形成中間體IM4,相應(yīng)的通過過渡態(tài)TS2的Si-C鍵氧化加成反應(yīng)生成Ni(IV)中間體IM6需要17.4 kcal/mol的活化自由能,比經(jīng)歷TS3所需要的能量低4.3 kcal/mol。隨后的Si-H還原消除通過過渡態(tài)TS4生成Ni(II)中間體IM7,勢壘為2.7 kcal/mol。最后,通過過渡態(tài)TS5的Si-C鍵還原消除得到產(chǎn)物3a并再生Ni(0)物種IM1。該步驟的勢能壘為4.4 kcal/mol,自由能降低為22.5 kcal/mol。計算結(jié)果表明,通過Si-C鍵氧化加成生成的Ni(IV)絡(luò)合物具有最高的活化自由能,可能是決速步。計算的結(jié)果與動力學(xué)結(jié)果是一致的。
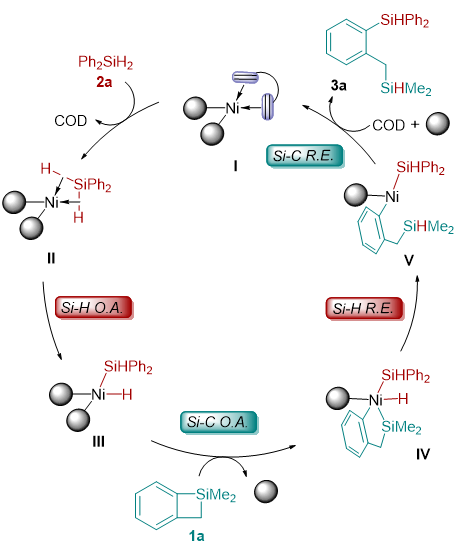
圖5: 機理預(yù)測
在該工作中,沈曉課題組報道了一種硅烷和苯并硅雜環(huán)丁烷在鎳催化下的選擇性交叉再分配反應(yīng)。該反應(yīng)能夠成功的關(guān)鍵是由于在熵驅(qū)動下苯并四元環(huán)硅環(huán)張力的釋放。這與之前的通過生成硅烷氣體的焓驅(qū)動的硅烷再分配反應(yīng)在反應(yīng)模式上是不一樣的。該反應(yīng)具有廣泛的底物范圍。實驗和計算相結(jié)合的機理研究支持反應(yīng)是通過Ni(0)-Ni(II)-Ni(IV)催化循環(huán)進行的。其中環(huán)硅通過環(huán)張力釋放的氧化加成步驟是整個再分配反應(yīng)能夠成功的關(guān)鍵。武漢大學(xué)高等研究院博士生陳紹維為第一作者。計算部分的工作由重慶大學(xué)博士生何曉倩完成。沈曉教授、藍宇教授和加州大學(xué)洛杉磯分校Houk教授為通訊作者。
該研究得到了中國國家自然科學(xué)基金委、中國中央高校基本科研業(yè)務(wù)費、武漢大學(xué)人才啟動經(jīng)費和美國國家自然科學(xué)基金委的支持。
論文鏈接: https://onlinelibrary.wiley.com/doi/10.1002/anie.202213431
沈曉課題組常年招收博士后,研究生,感興趣的同學(xué)請直接聯(lián)系沈曉老師(xiaoshen@whu.edu.cn)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn