

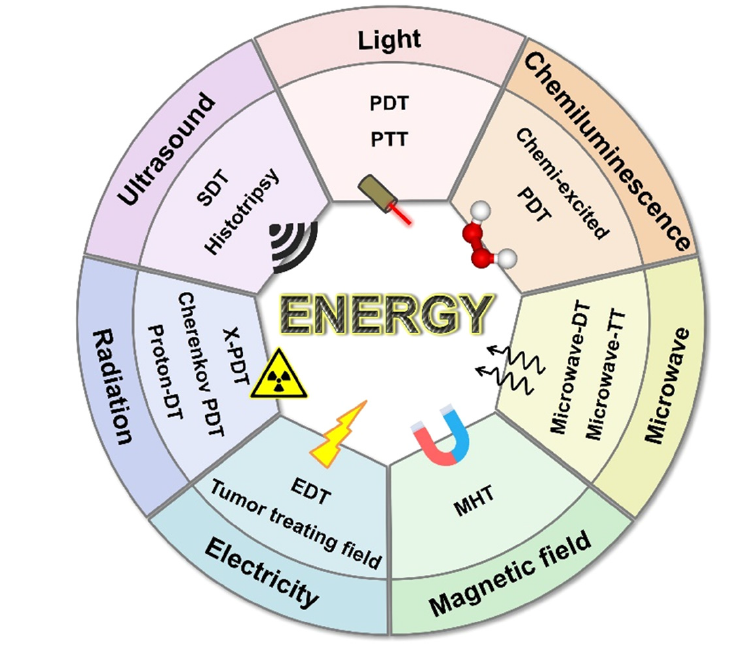
圖1. 用于癌癥治療的不同激發策略(圖片來源:Chem. Soc. Rev.)
1.PTT、PDT作用機制:
PDT是一種臨床確立的腫瘤學干預措施,它依賴于光介導的光敏劑(PS)活化以產生活性氧(ROS)。在光照射下,激發的PS經歷系統間穿越。由于三重態的壽命較長,因此系統間穿越速率高并產生活性氧。對于I型PDT,激發的PS將電子轉移到周圍的分子并產生自由基。相反,II型PDT涉及向三線態氧的能量轉移,受激發的分子氧轉化為單線態氧。PS在靶腫瘤中的蓄積以及充足的分子氧供應是PDT的先決條件。但光對組織的穿透力非常有限(僅有10 mm),對于深層組織處的腫瘤難以造成致命傷害,同時腫瘤微環境乏氧且滲透性低。
PTT是指光熱劑通過非輻射弛豫釋放熱量,從而對癌癥進行熱消融。PTT治療過程產生的副作用較小,全身系統毒性低,不會對正常組織造成損傷,具有很大的臨床應用潛力。有效的PTT可通過阻斷與熱和修復相關的特定基因來提高光熱轉換效率以產生更多熱量和降低癌癥的熱耐受性。但光熱劑在人體內流通情況也并沒有完全搞清楚,也沒有進行長期的實驗觀察,對于其潛在毒性還得繼續摸索。
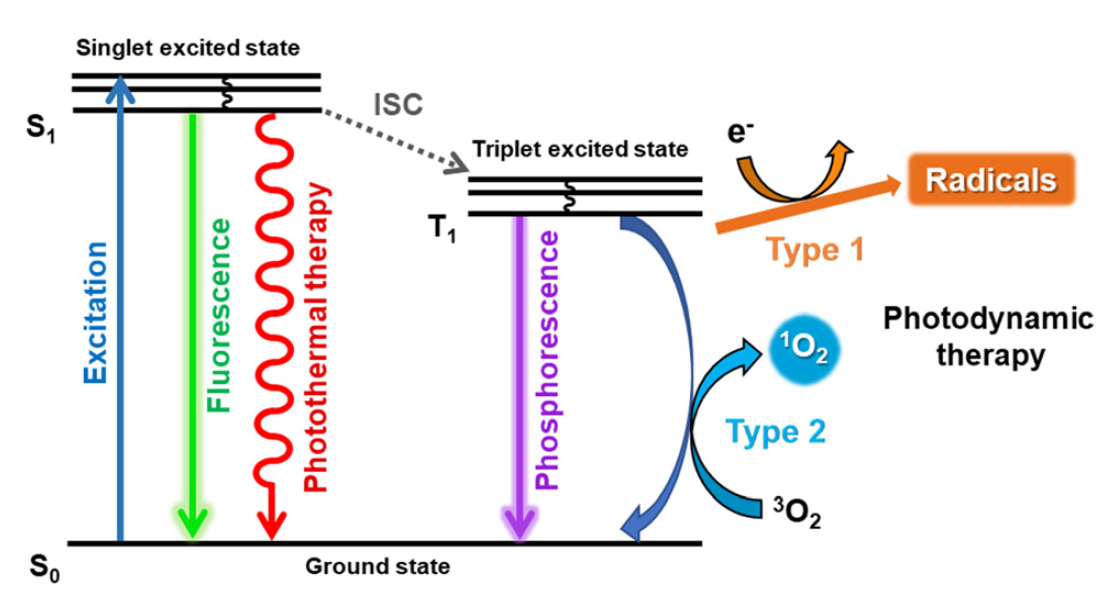
圖2. PDT以及PTT機制示意圖(圖片來源:Chem. Soc. Rev.)
2.SDT及HIFU作用機制:
超聲是一種頻率>20 kHz的機械波,需要彈性介質傳輸能量,由于其非侵入性方式和深層組織穿透能力,已廣泛應用于臨床領域。SDT是基于超聲發展起來的新興無創治療方法,盡管SDT產生活性氧的機制仍有爭議,但目前主要認為超聲與水介質相互作用,引發“空化”作用,空化氣泡的連續坍縮產生聲致發光,同時在周圍的微環境中產生巨大的熱量和壓力,激活聲敏劑,促使其產生活性氧殺傷細胞。然而,大多數聲敏劑的生物安全性和ROS產生率較低,使其療效還不足以取代傳統的抗腫瘤治療方法,因此SDT尚未在臨床上得到廣泛應用。此外,雖然SDT解決了光動力療法低穿透的問題,但仍會導致腫瘤缺氧而阻礙其效率的提高,因此,保障腫瘤部位充足的氧氣供應仍然是一個需要解決的問題。
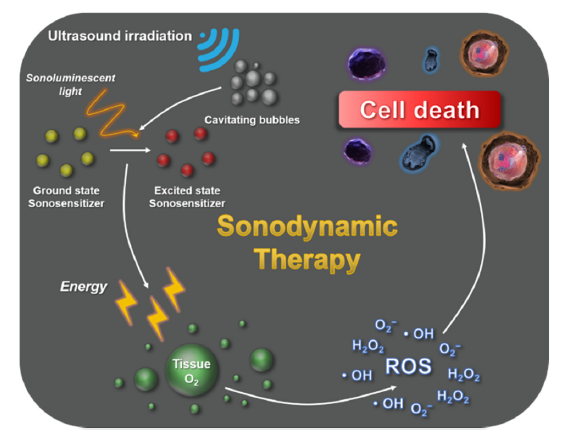
圖3. SDT機制示意圖(圖片來源:Chem. Soc. Rev.)
HIFU原理是利用超聲波能夠無損傷的穿透人體組織,并且在體內聚焦,產生熱效應(主要效應)、空化效應、機械效應等;焦點的溫度可以達到60-100 ℃,從而導致焦點處的組織發生凝固性壞死,而不損傷焦點外的正常結構。近年來,HIFU在免疫治療領域引起了極大的關注,盡管HIFU的免疫機制仍有爭議,但主要認為超聲導致的變性抗原蛋白的消失而引發免疫反應。
3.CL PDT機制
化學發光是一種在室溫下將化學能轉化為光能的化學現象,其反應體系多以草酸酯、過氧化氫(H2O2)以及熒光染料為主要組成部分,自發光波長通常由所采用的熒光染料的性質所決定。草酸酯受H2O2激發產生自發熒光,與熒光成像相比,其具有相對較深的穿透深度和較高的信噪比(S/N)。同時研究發現,其同時可產生化學能,誘導PS激發從而產生ROS。控制腫瘤區域附近CL的激活是取得更好治療效果的關鍵點。如果化學反應在PS到達腫瘤之前開始,產生的ROS會影響正常組織。如果反應速度不足以產生足夠量的ROS,則細胞內抗氧化成分會降低治療效果。相比于直接激發,間接化學發光激發PS的PDT有以下幾個優點:一、通過光轉換納米顆粒,PS可以被高效遞送到腫瘤區域;二、多種激發光源增加了組織穿透能力;三、不管是常氧腫瘤還是乏氧腫瘤均能通過I型PDT來實現高效治療。
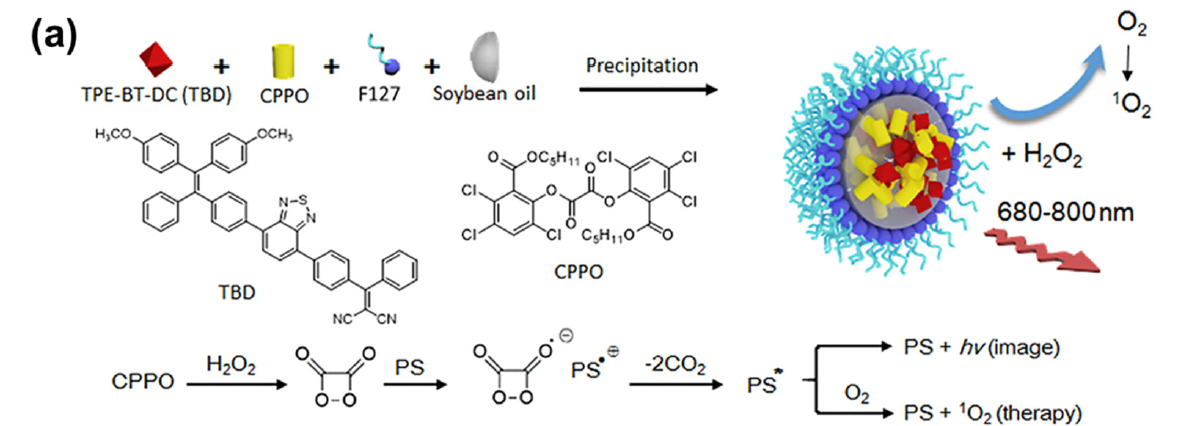
圖4. CL PDT機制示意圖(圖片來源:Chem. Soc. Rev.)
4.X-PDT、CR PDT機制
基于X-射線直接激發PS或以X-射線激發納米閃爍體作為能量傳遞介質間接激發PS的X射線激發的X-PDT成為深層腫瘤治療領域的另一研究熱點。X-射線激發發光納米粒—PS耦合系統可提高ROS的產生率,從而有效提升了腫瘤的治療效果。目前,用于X-PDT的納米材料主要有基于稀土金屬閃爍發光納米粒和基于金屬硫/氧化物(金屬)半導體發光納米粒。
CR PDT是一種不需要外界光激發的新型光動力療法。通過放射性核素產生的切倫科夫輻射激活附近的PS,使其產生ROS以破壞靶細胞或組織,它克服了傳統PDT存在的組織滲透受限、依賴外部光等缺點,是一個很有前景的新領域。切倫科夫輻射比較微弱、易被生物組織衰減、缺乏對應光譜的PS以及腫瘤靶向性不佳是限制其在臨床進一步應用的關鍵因素。如何增強基于切倫科夫輻射的光動力治療療效是未來的研究重點。
5.MDTT機制
微波是指頻率為300 MHz-3000 GHz的電磁波,MIPDT是一種新的癌癥治療方法,與傳統PDT相比,其具有更快的消融時間和可忽略的副作用。相對磁導率、介電常數和阻抗匹配是定義微波吸收特性的主要參數。其中,離子限制效應影響金屬有機框架(MOF)中的微波熱效應。有限空間中離子碰撞比在自由空間中更頻繁地發生;因此,MOF微孔中的多次碰撞有利于將微波電磁能轉化為熱能。MIPDT有兩種不同的機制。在液態金屬中,微波誘導液態金屬中的電子轉移,其中電子與不同分子的反應產生ROS。在摻雜有過渡金屬的MOF中,由于在微波照射下電子-空穴對的發生分離,自由電子與分子氧發生作用產生1O2。
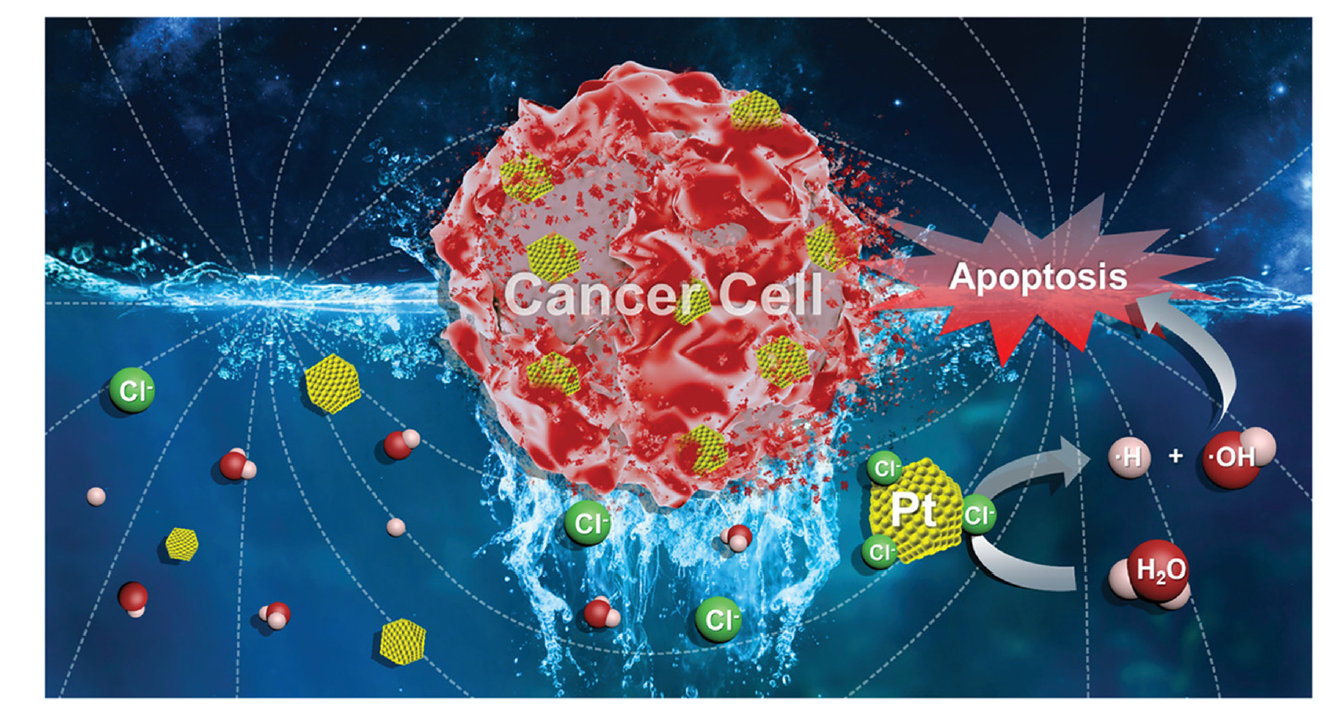
圖5. MDTT機制示意圖(圖片來源:Chem. Soc. Rev.)
總結
近年來,已經開發了各種能量驅動的癌癥治療方法。然而,目前只有PDT、SDT和TTF少數能源用于臨床試驗。PDT廣泛用于治療淺表腫瘤。SDT雖然未獲得FDA的批準,但它已在歐洲和日本得到應用。此外,醫生在臨床試驗中并未使用單一療法,而是使用雞尾酒療法,通過互補效應增強整體臨床結果。
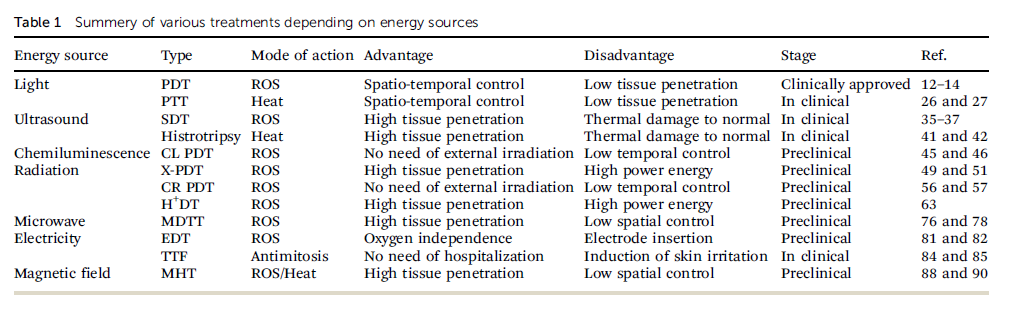
表1. 各種能量驅動的癌癥治療方法的臨床進展(圖片來源:Chem. Soc. Rev.)
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn