美國Scripps研究所的K. Barry Sharpless教授、丹麥哥本哈根大學的Morten Meldal教授以及美國斯坦福大學的Carolyn R. Bertozzi教授分享了諾貝爾化學獎的桂冠。其中,Sharpless教授、Meldal教授因在點擊化學(click chemistry)研究中做出的卓越貢獻獲獎,Bertozzi教授則因開拓生物正交化學(bioorthogonal chemistry)領域而獲獎。
▲今年的諾貝爾化學獎得主Carolyn R. Bertozzi教授(左)、Morten Meldal教授(中)和K. Barry Sharpless教授(右)(圖片來源:諾貝爾獎官網)
值得一提的是,這也是Sharpless教授在2001年因手性催化氧化反應獲諾貝爾化學獎以來,第二次摘得諾貝爾化學獎的桂冠。歷史上,兩獲諾貝爾化學獎的情景只發生過一次(Frederick Sanger教授,1958年與1980年)。Bertozzi教授也是第八位諾貝爾化學獎女性得主。接下來,我們將分別解讀這三位科學家的杰出成果。

▲Carolyn Bertozzi教授的工作將點擊化學推進到了一個全新的領域,并將其應用到了生命體中,她的生物正交反應能在不干擾細胞正常化學的情況下發生。而Barry Sharpless教授與Morten Meldal教授奠定了一類全新化學形式的基礎——點擊化學,它能讓分子模塊快速、高效地拼在一起。(圖片來源:參考資料[1])
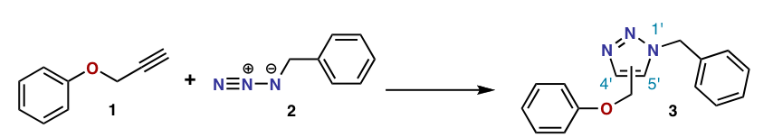
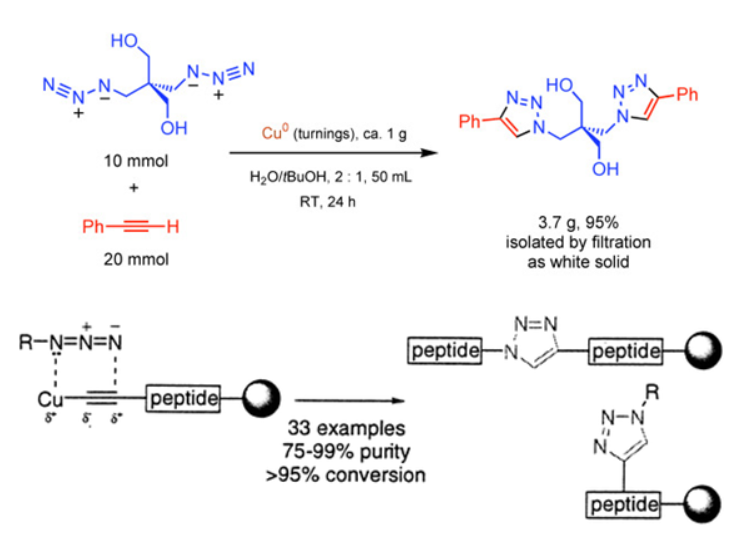
大自然是人類最好的老師,生物體內的蛋白質、核酸(DNA、RNA)大分子為生命的正常運轉與延續提供了重要的保障。盡管這兩種大分子的種類繁多復雜,但組成其結構的基本單元卻很精簡。蛋白質的基本結構單元為氨基酸,核酸則為核苷酸,前者有20種,后者只有5種。但這些結構單元可以通過不同的次序、空間取向進行排列,得到成千上萬種行使不同功能的生命大分子,進而形成我們眼中的大千世界。這種組合方式有些像樂高玩具,基礎模塊的種類并不多,但可以憑借豐富的想象力搭建出變化無窮的造型。▲很多生物大分子的結構就像樂高玩具,造型千變萬化,基礎模塊的種類卻并不多(圖片來源:123RF)樂高積木可以通過一個模塊的凹槽與另一個模塊的凸起契合完成兩個組件的拼接。類似的,化學家也希望找到一種合適的“分子接口”,眾多分子中只要這兩種基團相遇,便可以像搭扣一樣“click”(咔嗒)一聲將兩種分子緊鎖在一起。如此一來,小分子砌塊只需要分別修飾這些咬合接口,便可以實現兩兩拼接,進而構建復雜結構的大分子。時間回到2001年。就在Sharpless教授第一次榮膺諾貝爾化學獎的四個月前,他的另一篇重磅論文發表在了知名期刊Angewandte Chemie International Edition上。在這篇論文中,他與同事們寫道:“考察自然界的分子,表明相比碳-碳鍵,自然界更喜歡碳-雜原子鍵。”無論是核酸、蛋白質、還是多糖,都是由小型分子通過碳-雜原子鍵拼接起來的,而這些小型分子的總數量僅在35個左右。如果人類能將這套法則學到手,就能快速并可靠地合成大量有用的分子……▲這篇論文目前已被引用超過14000次(圖片來源:參考資料[2])于是,點擊化學(click chemistry)的概念應運而生,其強調以碳-雜原子鍵鍵合的方式進行分子組合,與此同時反應需具備產率高、適用性廣、副產物無害等特點,這也正符合Sharpless教授一直倡導的“簡單而有用的化學”。通常我們所說的點擊反應,即是指1,3-偶極環加成反應,又叫作Huisgen環化反應。該反應最早由德國化學家Rolf Huisgen教授(已于2020年去世,享年100歲)提出,他發現炔烴與疊氮化物混合時可發生[3+2]環化,從而得到五元雜環化合物。不過,這一反應需要在高溫條件下進行,并且以不對稱的炔烴作為底物時,經常會出現兩種區域異構體混合物。顯然,分子在反應體系中“煮”一遍,很多敏感的官能團會出現不兼容的現象,由此便限制了底物的適用范圍。加上得到的產物為混合物,效率較低,也為后續分離帶來了麻煩,并不符合點擊化學的理念。▲Huisgen環化反應:一個經典的“點擊化學”反應(圖片來源:By Greginnd [Public domain], from Wikimedia Commons)但這個問題可通過使用Cu(I)催化劑得以解決。2002年,Sharpless教授與Fokin教授合作報道了Cu(I)催化末端炔烴與疊氮化物的環加成反應。同年,Meldal教授也將末端炔烴負載在樹脂基底上,在Cu(I)催化劑的作用下實現了其與疊氮化物的環化。這兩項工作使得反應在室溫條件下便可進行,且具有良好的區域選擇性,最終主要得到單一的環化產物,成功實現了對Huisgen環化反應的改良。▲Sharpless教授與Fokin教授的工作(上),以及Meldal教授的工作(下)(圖片來源:參考資料[3])
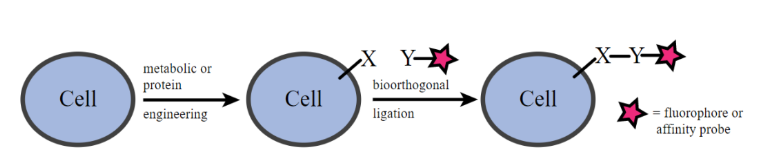
這類反應的底物適用范圍十分廣泛。將炔烴與疊氮化物的取代基進行適當的變換,便可以實現多種不同分子的構建。目前,點擊反應已在藥物研發、功能材料、超分子自組裝、化學生物學等諸多領域得到廣泛的應用。毫不夸張地講,該反應就是人們一直尋找的那種“分子接口”,改變了合成復雜結構分子的命運。“(2001年)諾貝爾獎證書上的墨印還沒有干透,他就提出了點擊化學的概念和實例。這一概念在化學和化學生物的偶聯反應中,已經占據了統治性的地位。”在Sharpless教授斬獲2019年美國化學會最高榮譽普里斯特利獎章(Priestley Medal)時,科學家們就已對點擊化學的重要意義做了很好的總結。今日點擊化學獲得諾貝爾化學獎的垂青,可謂實至名歸。兩位作為該領域代表的杰出科學家得此殊榮,也是對他們貢獻的最好認可。自然界中,生物體內發生的化學過程吸引了化學家和生物學家的共同興趣。然而,構成生命的基本單元——細胞,是一個極其復雜的系統,時刻發生著無數反應,要在活體內研究核酸、脂質、蛋白質等眾多生物分子極具挑戰,尤其是,如何在不受任何其他過程干擾的情況下研究目標分子。▲2008年,開發GFP的三位科學家同樣獲得了諾貝爾化學獎(圖片來源:The Nobel Prize in Chemistry 2008. NobelPrize.org. Nobel Media AB 2019. Tue. 8 Oct 2019.)化學和生物交叉領域的一些科學家為此開發新工具和方法,一個典型的例子就是我們已熟悉的發光蛋白(例如綠色熒光蛋白GFP)。以基因編碼的發光蛋白作為標簽,與感興趣的蛋白相連,讓我們看到蛋白的運動、定位、相互作用等。發現和發展GFP的三位科學家也因此在2008年榮膺諾貝爾化學獎。不過,還有很多生物分子,以及分子各種各樣的修飾,很難用基因編碼的報告分子來示蹤,需要發展其他的手段實現多聚糖、脂質、核酸等生物分子的標記。生物正交化學的概念便是在這樣的背景下產生的。這類反應要求在研究活體生物系統內給定的化學反應時,不會干擾其中固有的生物化學過程,即不產生細胞毒性。發展該反應的目的不僅在于充分理解生物體內已知的反應,更是為了發現其中的新反應。正如Carolyn Bertozzi教授在2011年Accounts of Chemical Research期刊的一篇文章中總結回顧:“生物正交反應可以幫助人們更準確地理解生物化學反應過程中分子層面的細節,而要在如此復雜的環境下研究生物分子,就需要引入相應的成像探針、親和性試劑或者具有特定功能的基團。”▲2011年發表的綜述文章概述了生物正交化學十余年發展的歷程(圖片來源:參考資料[7])Bertozzi教授在這一交叉領域做出的開拓性貢獻與她的經歷分不開。她在哈佛大學獲得化學學士學位后,在加州大學伯克利分校完成化學博士研究,專注于低聚糖類似物的化學合成。低聚糖是一類結構多樣的分子,在細胞識別和細胞結合中發揮重要作用。細胞表面的糖鏈分子可以用于免疫系統過程,有助于識別細菌和病毒感染。順理成章地,在博士后期間,Bertozzi教授進入免疫學領域,關注與促炎反應有關的細胞粘附,積累了大量關于細胞生物學的知識。因為在細胞相互作用方面做出的貢獻,1999年,33歲的她成為麥克阿瑟天才獎歷史上最年輕的獲獎者之一。▲生物正交反應的示意圖(圖片來源:public domain)在此基礎上,Bertozzi教授開始尋找適合不同類型生物分子的標記方式。生物正交反應的基本策略,是將細胞或生物體與修飾特定功能基團的前體分子(化學報告分子)共同孵育。這種前體分子可以是用于標記多聚糖的單糖、標記核酸的核苷酸、標記蛋白質的氨基酸以及標記脂質的脂肪酸等。一旦化學報告分子引入目標生物分子中,就可以利用探針分子對其進一步處理,研究給定的生物化學過程。由于細胞內主要的介質為水,該類反應需要能在水作為溶劑的條件下進行。同時,目標生物分子在生物體內濃度通常較低,化學報告分子在此情況下仍具備順利結合靶標分子的能力,并滿足一定的反應速率。
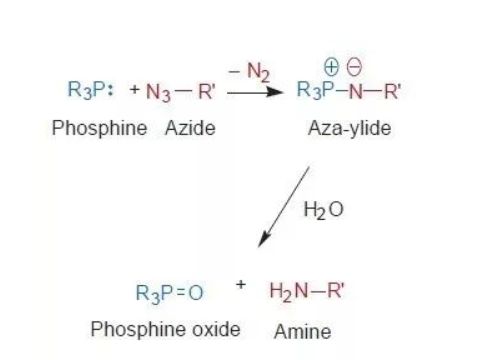
Bertozzi教授發展的生物正交反應借鑒了Staudinger還原(Staudinger Reduction)反應,該反應最早由德國化學家Hermann Staudinger先生提出,疊氮化物與有機膦或亞磷酸酯反應得到氮雜葉立德(aza-ylide)中間體,進一步水解便可形成相應的胺類產物。這兩類物質在生物體內并不存在,因此不會與其他生物分子發生反應。此外,疊氮基團體積小,可以最小程度地影響被修飾的目標生物分子,更真實地還原生物化學過程。
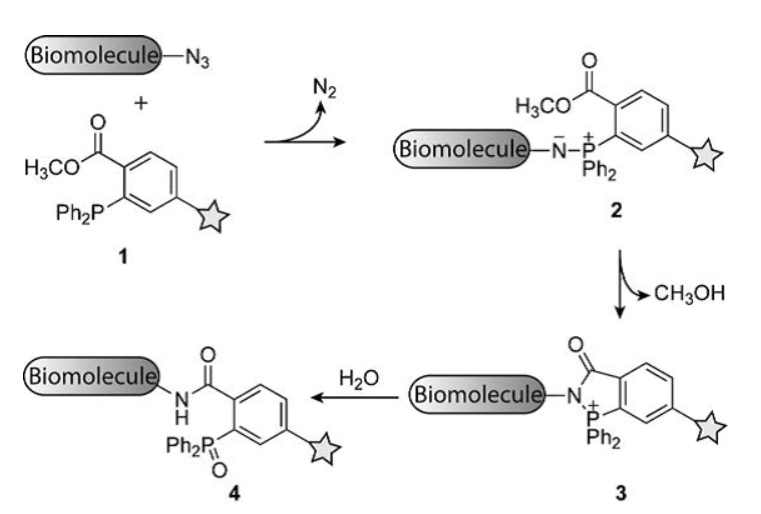
▲經典的Staudinger還原反應的過程(圖片來源:參考資料[8])于是,他們設計了Staudinger連接(Staudinger Ligation)反應,其反應過程如下圖所示:三芳基膦1的其中一個芳香基團鄰位修飾一個酯基,同時標記了探針基團。修飾疊氮基團的目標生物分子與之反應后形成氮雜葉立德中間體2,酯基進而捕獲該中間體發生分子內環化,形成相應的內酰胺中間體3,隨后在水性環境下水解得到最終酰胺基修飾的靶標分子4。內酰胺中間體3可謂該反應的核心,常規的Staudinger還原反應在得到氮雜葉立德中間體2后直接水解得到氨基修飾的靶標分子,無法引入探針基團。 ▲生物正交反應Staudinger連接反應的過程(圖片來源:參考資料[9])有了以上工作的啟發,許多研究者紛紛加入到生物正交反應的研究中。一系列不同的生物正交反應相繼涌現,并在蛋白質、多聚糖、脂質、核酸等生物分子的選擇性標記中得到了廣泛的應用。毫不夸張地講,生物正交反應的提出為生物體內原位研究生物化學過程提供了重要的手段,具有劃時代的意義。如今,Carolyn R. Bertozzi教授作為該反應的重要開拓者。摘取諾貝爾化學獎的桂冠,也同樣是對其在化學生物學中貢獻的最好褒獎。參考資料:
[1] The Nobel Prize in Chemistry 2022, Retrieved October 5, 2022, from https://www.nobelprize.org/uploads/2022/10/press-chemistry2022.pdf
[2] Hartmuth C. Kolb et al., (2001), Click Chemistry: Diverse Chemical Function from a Few Good Reactions, Angewandte Chemie International Edition in English, DOI: 10.1002/1521-3773(20010601)40:11%3C2004::AID-ANIE2004%3E3.0.CO;2-5
[3] Vsevolod V. Rostovtsev et al., (2002). A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective “Ligation” of Azides and Terminal Alkynes. Angew. Chem. Int. Ed., DOI: 10.1002/1521-3773(20020715)41:14<2596::AID-ANIE2596>3.0.CO;2-4
[4] Christian W. Torn?e et al., (2002). Peptidotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides. J. Org. Chem., DOI: 10.1021/jo011148j
[5] American Chemical Society names K. Barry Sharpless 2019 Priestley Medalist, Retrieved October 7, 2020, from https://www.acs.org/content/acs/en/pressroom/newsreleases/2018/june/acs-names-k-barry-sharpless-2019-priestley-medalist.html
[6] Dr. Carolyn Bertozzi pioneers bioorthogonal chemistry to study molecules within living systems. from https://www.ipwatchdog.com/2017/10/05/evolution-of-tech-dr-carolyn-bertozzi-invents-bioorthogonal-chemistry-to-study-molecules-within-living-systems/id=88882/
[7] Carolyn R. Bertozzi et al., (2011) A Decade of Bioorthogonal Chemistry. Acc. Chem. Res., DOI: 10.1021/ar200193f
[8] Eliana Saxon et al., (2000) Cell Surface Engineering by a Modified Staudinger Reaction. Science, DOI: 10.1126/science.287.5460.2007
[9] Ellen M. Sletten et al., (2009) Bioorthogonal Chemistry: Fishing for Selectivity in a Sea of Functionality. Angew. Chem. Int. Ed., DOI: 10.1002/anie.200900942