



正文
化學(xué)選擇性轉(zhuǎn)化是指在不通過繁瑣的保護(hù)基策略下實(shí)現(xiàn)的復(fù)雜分子的官能團(tuán)轉(zhuǎn)化。羧基普遍存在于多種復(fù)雜分子中,可以被還原為醇。由于羧基本身不具備突出明顯的親核與親電性質(zhì),致使當(dāng)分子中存在其他官能團(tuán)時(shí),很難完全選擇性地還原羧酸為醇。比如強(qiáng)的陰離子還原劑(如LiAlH4)可以還原羧酸,但當(dāng)其他官能團(tuán)如酮、酯、酰胺或硝基存在于同一分子中時(shí),這類還原劑將不具有選擇性地將其他官能團(tuán)同時(shí)還原。還有一種常見方法是將NaBH4與各種添加劑結(jié)合,其在反應(yīng)過程中可以在原位生成BH3從而實(shí)現(xiàn)對(duì)羧酸還原。但硼烷通常也與更多的親核官能團(tuán)如酰胺和烯烴反應(yīng),且硼烷對(duì)水分不穩(wěn)定,因此,它仍然不是一種理想的試劑。在復(fù)雜分子中,如何高選擇性地實(shí)現(xiàn)對(duì)羧酸還原仍是一個(gè)難題。
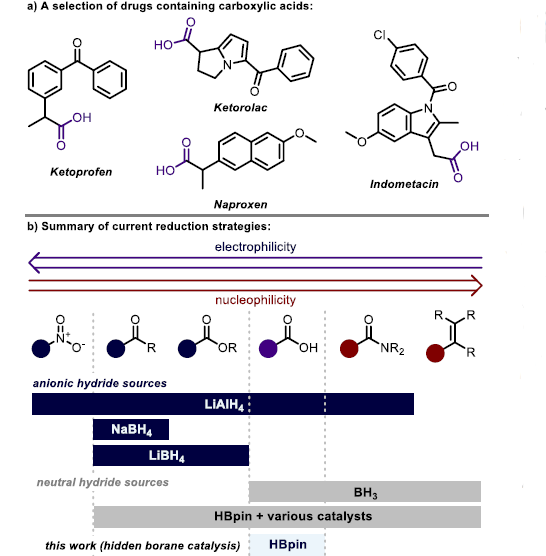
圖1.復(fù)雜分子中羧基的還原(圖片來源:Angew. Chem. Int. Ed.)
HBpin于20世紀(jì)90年代初首次被報(bào)道,因其穩(wěn)定性而被廣泛用于硼氫化反應(yīng)。通過與各種催化劑的結(jié)合,HBpin的反應(yīng)性得以增加。值得注意的是,這些大多數(shù)增加反應(yīng)性的方法具有較好的選擇性且適用于復(fù)雜底物。在此背景下,作者此前報(bào)道了一種獨(dú)特的鈷催化反應(yīng),該反應(yīng)可以通過可見光控制酮酸硼氫化還原的化學(xué)選擇性,根據(jù)之前的經(jīng)驗(yàn),作者認(rèn)為羧酸硼氫化反應(yīng)與Co(0)/Co(I)催化循環(huán)是具有相同之處,因此HBpin具備實(shí)現(xiàn)選擇性活化羧酸的可能性。
通過原位核磁共振對(duì)羧酸選擇性氫化硼酸的進(jìn)一步機(jī)理探測(cè),作者注意到11B核磁共振的關(guān)鍵特征。與之前的結(jié)果不同,作者注意到BH3 (δ- 12 ppm)和BH4- (δ - 42 ppm)在整個(gè)反應(yīng)過程中出現(xiàn)的小峰。然而,在整個(gè)反應(yīng)過程中,HBpin (28 ppm)仍然是存在的主要硼物種,這排除了直接生成BH3還原羧酸的可能性。
Stephen Thomas的團(tuán)隊(duì)最近在“隱藏硼烷”催化方面的開創(chuàng)性工作證明了許多報(bào)道的硼氫化催化體系(包括基于金屬配合物、負(fù)氫物種和堿的催化劑)實(shí)際上是通過促進(jìn)HBpin分解成BH3和BH4-來進(jìn)行的,。此外,Jones課題組還證明羧酸可以與HBpin反應(yīng)生成BH3。認(rèn)識(shí)到這些事實(shí),作者決定看看是否可以利用HBpin重現(xiàn)此前鈷催化反應(yīng)實(shí)現(xiàn)的選擇性。

圖2.促進(jìn)劑的選擇(圖片來源:Angew. Chem. Int. Ed.)
經(jīng)過對(duì)多個(gè)氫源物種的篩選,作者發(fā)現(xiàn)叔丁醇鉀作為促進(jìn)劑時(shí)反應(yīng)效果最佳。并在這一條件下進(jìn)行底物范圍的拓展。,簡單羧酸的氫化率(2b-2h)較好,但對(duì)硝基取代的2i并未發(fā)生反應(yīng)。為證明該方法適用于更復(fù)雜的底物,作者選擇了萘普生、酮洛芬、吲哚美辛和異氧哌酸這四種藥物進(jìn)行選擇性還原,得到2t-2w的產(chǎn)物,表現(xiàn)出酮、酰胺和芳鹵官能團(tuán)的耐受性。對(duì)映體萘普生以99% ee給出了還原產(chǎn)物2t,表明手性中心處沒有受到還原反應(yīng)的影響。在規(guī)模化反應(yīng)方案的基礎(chǔ)上,作者以1克萘普生為起始原料,以57%的收率獲得2t。
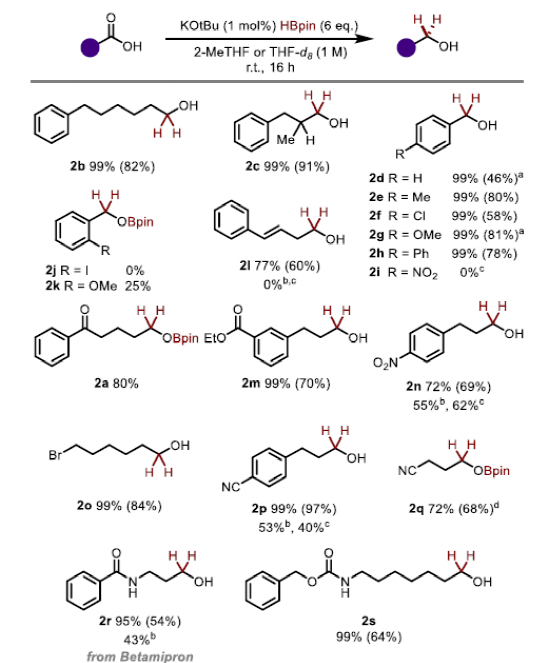
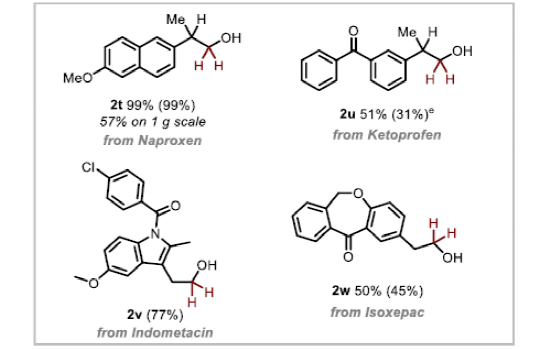
圖3.底物拓展(圖片來源:Angew. Chem. Int. Ed.)
為了表明該方法與經(jīng)典方法相比的進(jìn)步,作者用化學(xué)計(jì)量BH3·DMS對(duì)幾種底物進(jìn)行還原。從起始原料1n, 1p和1r得到的產(chǎn)率顯著低于該方法方法。這種方法的主要限制是要求相對(duì)較高的濃度。因此,可溶性較差的起始物料反應(yīng)活性有限,稀釋顯著降低了反應(yīng)速率。但作者也證明了不同的促進(jìn)劑可以與不同的溶劑結(jié)合使用,從而可以拓寬該反應(yīng)的用途。
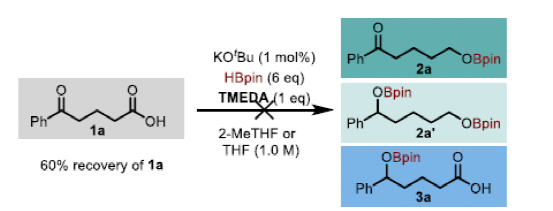
圖4.機(jī)理實(shí)驗(yàn)(圖片來源:Angew. Chem. Int. Ed.)
為了進(jìn)一步揭示HBpin激活時(shí)選擇性增強(qiáng)的原因,作者進(jìn)行了DFT計(jì)算研究。當(dāng)反應(yīng)中產(chǎn)生BH3時(shí),活化酸中-OH在動(dòng)力學(xué)和熱力學(xué)上都是可達(dá)的。自由能壘僅10.6 kcal/mol,比HBpin主導(dǎo)的激活低11.1 kcal/mol。然后,作者探索剩余B-H鍵轉(zhuǎn)化的順序,最終在一個(gè)放熱的過程中(-51.9 kcal/mol)形成中間IV。從中間IV開始,作者探索了高濃度HBpin插入時(shí)的選擇過程。H-Bpin鍵直接插入到酮的C=O鍵時(shí)由于四元環(huán)過渡態(tài)(TSIV-V’)的存在是很困難的。因此,自由能壘很高(35.6 kcal/mol)。相比之下,由于相鄰的硼酯物種(TSIV-V)對(duì)進(jìn)入HBpin起到的額外的穩(wěn)定作用,使得在酸位點(diǎn)上的C=O硼氫化比酮位點(diǎn)低8.0 kcal/mol,反應(yīng)的自由能壘為27.6 kcal/mol,從而解釋了在BH3催化活化下反應(yīng)的選擇性。
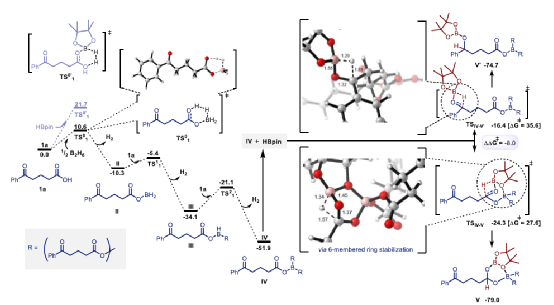
圖5.DFT計(jì)算結(jié)果(圖片來源:Angew. Chem. Int. Ed.)
總結(jié)
作者通過大量分析嘗試與機(jī)理研究發(fā)現(xiàn)了一種獨(dú)特溫和的化學(xué)選擇性還原羧酸的方法。該方法大大擴(kuò)大了“隱藏硼烷”催化反應(yīng)的范圍,證明了這一概念的普遍存在,提供了和傳統(tǒng)的過渡金屬催化不同的新思路。
文獻(xiàn)詳情:

長按或掃碼左側(cè)二維碼查看原文
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn