



正文
含硫化合物由于其獨特的理化性質(zhì),在天然產(chǎn)物、藥物分子、功能材料分子中十分常見,同時在合成化學(xué)中作為通用的中間體、催化劑以及配體廣泛存在。含硫化合物的重要性與實用性推動了其高效合成策略的發(fā)展,但是可能由于硫原子的特殊性質(zhì),使得合成手性含硫化合物過程中存在兼容性差、可控性差等問題。因此含硫化合物的不對稱合成仍是一項重要且具有挑戰(zhàn)性的研究課題。
上海交通大學(xué)陳志敏課題組致力于通過發(fā)展新穎的不對稱催化策略、發(fā)展新型的手性催化劑解決含硫化合物不對稱合成中的一些難題。
該課題組首先發(fā)展了一類基于氫鍵相互作用的手性路易斯堿/手性磷酸的協(xié)同催化策略實現(xiàn)了前人未能解決的1,1-二取代烯烴及三取代烯烴的高對映選擇性的親電芳硫基化反應(yīng),高效合成了一類含有全碳季碳手性中心的β-芳硫基酮化合物(圖1a, Angew. Chem. Int. Ed. 2019, 58, 12491)。
同時,作者利用該協(xié)同催化體系進(jìn)一步實現(xiàn)了分子間的三組分親電芳硫基化反應(yīng),以催化量的手性磷酸替代PTSA等強(qiáng)酸,反應(yīng)條件溫和,克服了該類型反應(yīng)在強(qiáng)酸條件下易發(fā)生兩組分副反應(yīng)的缺點;而且實現(xiàn)酚類化合物作為氧親核試劑參與反應(yīng),與之前報道中作為碳親核試劑不同。親核試劑可進(jìn)一步拓展到醇類和水,并都能以中等至優(yōu)異的產(chǎn)率和高對映選擇性得到一系列含硫芐基芳基醚以及芐基烷基醚類化合物(圖1b,CCS Chem. 2022, 10.31635/ccschem.021.202101590)。
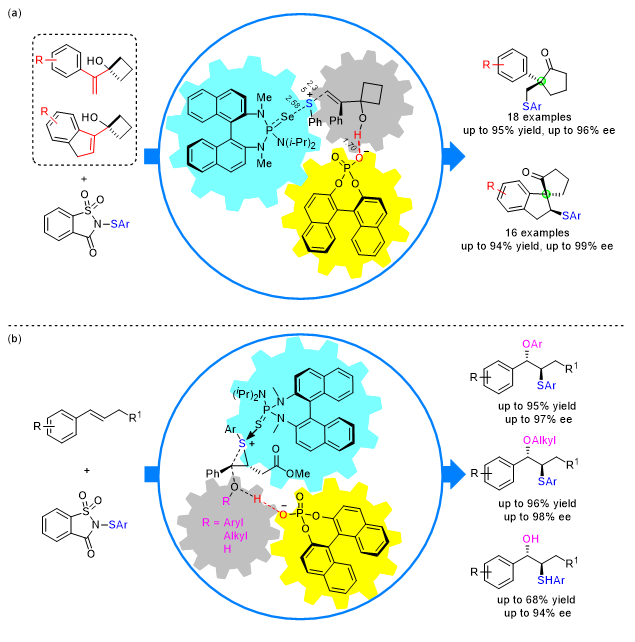
▲圖1. 手性路易斯堿/手性磷酸的協(xié)同催化體系
在以上工作的基礎(chǔ)上,陳志敏課題組發(fā)展了一類基于BINOL骨架且含有潛在氫鍵受體的新型路易斯堿催化劑(圖2),并結(jié)合非手性磺酸提出了一種基于雙氫鍵作用的協(xié)同催化策略。通過這一催化策略實現(xiàn)聯(lián)芳基酚類化合物的阻轉(zhuǎn)選擇性親電芳硫基化反應(yīng),高效地合成了一類含手性軸的有機(jī)硫化合物(圖3, J. Am. Chem. Soc.2022, 144, 2943)。其中磺酸與底物、催化劑之間的雙氫鍵作用對反應(yīng)的對映選擇性控制起到了重要作用。
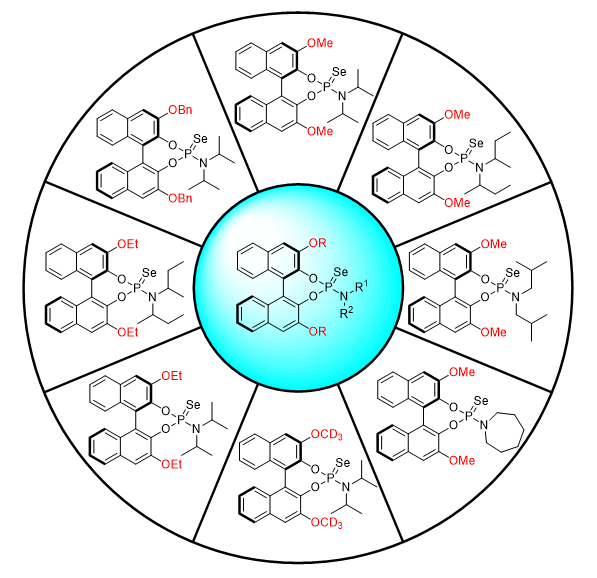
▲圖2. 基于BINOL骨架的新型路易斯堿催化劑
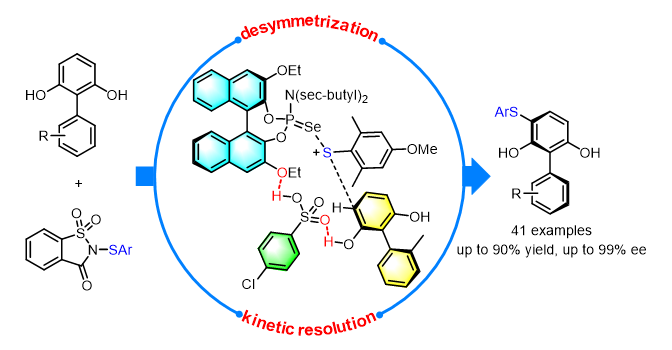
▲圖3. 聯(lián)芳基酚類化合物的親電芳硫基化反應(yīng)
近日,陳志敏課題組針對含兩個相鄰C-N軸的雙芳基仲胺類化合物的不對稱合成開展研究。這類化合物由于兩個相鄰的C-N軸易發(fā)生外消旋化,導(dǎo)致不對稱合成該類化合物極具挑戰(zhàn)性,之前成功的案例很少 (圖4a)。該課題組以N-芳基氨基醌類化合物為底物,提出通過向N-芳基氨基醌類化合物中引入可作為氫鍵受體的含硫基團(tuán),既形成分子內(nèi)N?H···S氫鍵作用固定一個C-N軸,也能實現(xiàn)另一個C-N軸的阻轉(zhuǎn)選擇性控制的策略(圖4b)。
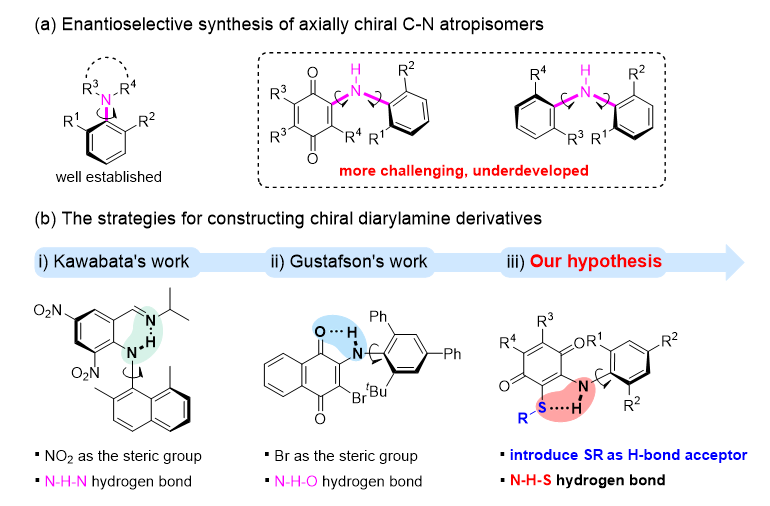
▲圖4. N-芳基氨基醌的阻轉(zhuǎn)選擇性磺酰化反應(yīng)的設(shè)計思路(圖片來源:Angew. Chem. Int. Ed.)
最終通過發(fā)展一類基于SPINOL骨架的路易斯堿作為催化劑(圖5),成功實現(xiàn)了N-芳基氨基醌的阻轉(zhuǎn)選擇性磺酰化反應(yīng)(圖6,Angew. Chem. Int. Ed., 2022, 10.1002/anie.202211782)。該反應(yīng)具有對映選擇性優(yōu)秀、底物適應(yīng)性廣、反應(yīng)收率高等特點。
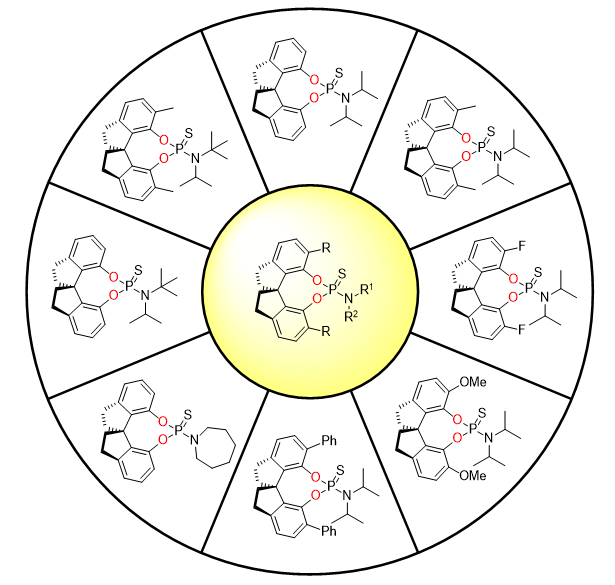
▲圖5. 基于SPINOL骨架的新型路易斯堿催化劑(圖片來源:Angew. Chem. Int. Ed.)

▲圖6. N-芳基氨基醌的阻轉(zhuǎn)選擇性磺酰化反應(yīng)(圖片來源:Angew. Chem. Int. Ed.)
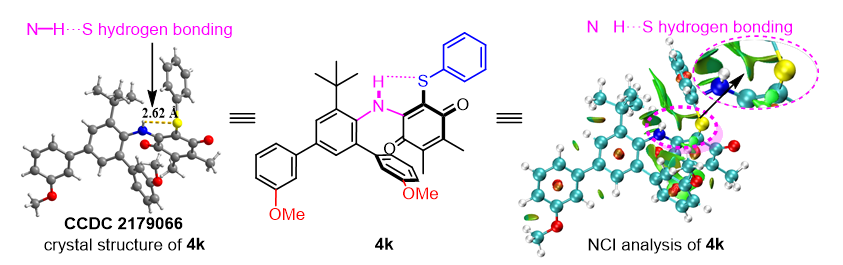
▲圖7. 產(chǎn)物的單晶衍射與NCI分析(圖片來源:Angew. Chem. Int. Ed.)
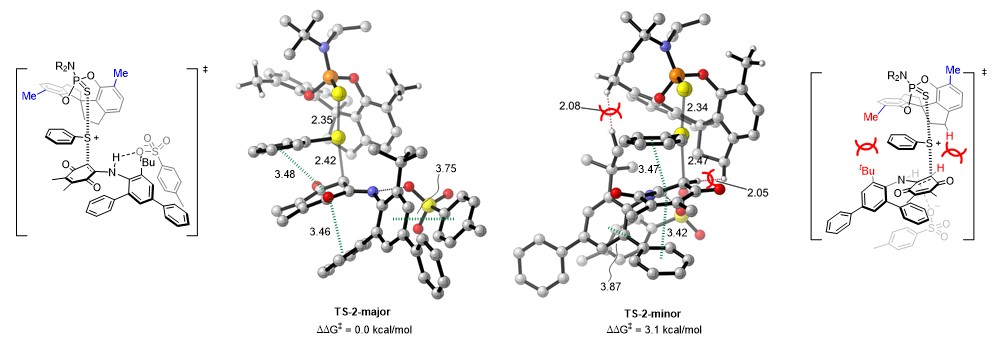
▲圖8. 阻轉(zhuǎn)選擇性來源的計算研究(圖片來源:Angew. Chem. Int. Ed.)
總結(jié)
上海交通大學(xué)陳志敏課題組發(fā)展了一類新穎的SPINOL骨架作為路易斯堿催化劑,首次實現(xiàn)N-芳基氨基醌的阻轉(zhuǎn)選擇性磺酰化反應(yīng),高效合成了一系列含硫的雙芳基胺類化合物,為手性含硫化合物的進(jìn)一步應(yīng)用研究提供了物質(zhì)基礎(chǔ),也為手性含硫化合物的高效合成提供了新思路。
以上研究工作得到了國家自然科學(xué)基金委、國家科技部、上海市教委、上海市科委的資助。涂永強(qiáng)院士、李長坤老師和葉俊濤老師對研究工作提出了許多寶貴的指導(dǎo)意見。
文獻(xiàn)詳情:

長按或掃碼左側(cè)二維碼查看原文
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點或證實其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn