



(圖片來源:J. Am. Chem. Soc.)
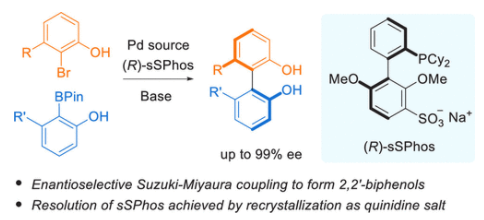
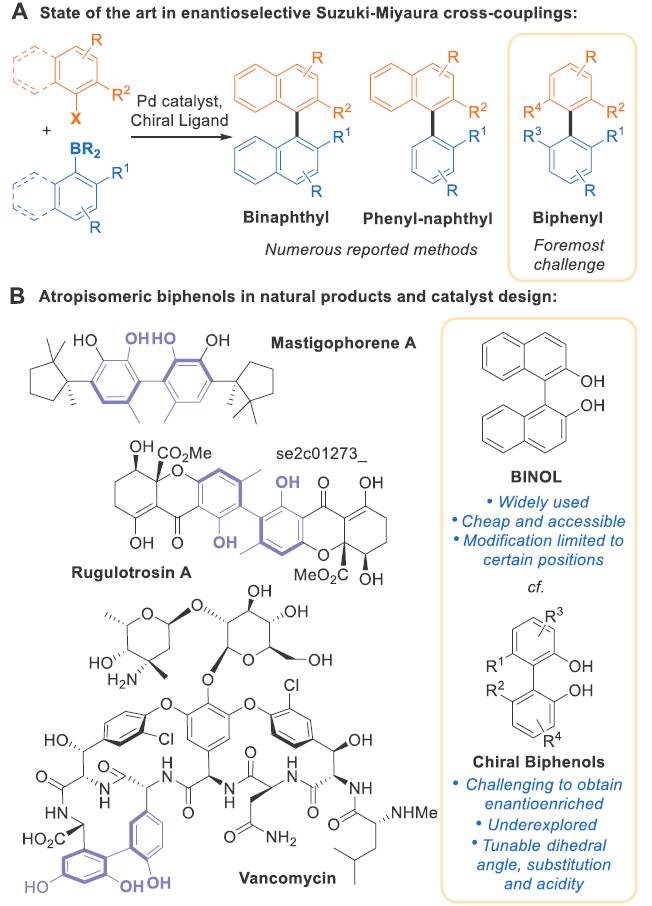
過渡金屬催化的交叉偶聯(lián)反應(yīng)可以高效構(gòu)建聯(lián)芳基化合物,而Suzuki-Miyaura偶聯(lián)反應(yīng)就是其中重要的合成方法之一。近些年,金屬配體的發(fā)展使得大位阻聯(lián)芳基化合物的合成成為了可能,因此會產(chǎn)生阻旋異構(gòu)現(xiàn)象。由于阻旋異構(gòu)體往往具有不同的生物活性,目前已成為藥物化學(xué)研究的重點(diǎn)。因此在有機(jī)合成方法學(xué)的發(fā)展中能夠?qū)崿F(xiàn)良好的立體化學(xué)控制是至關(guān)重要的。自從2000年首例不對稱Suzuki偶聯(lián)反應(yīng)報道以來,化學(xué)家們發(fā)展了大量的手性配體來高對映選擇性實(shí)現(xiàn)Suzuki-Miyaura偶聯(lián)反應(yīng)。盡管目前已經(jīng)取得了很大的進(jìn)展,但是大部分反應(yīng)均需要較大π體系的底物(如萘環(huán)),從而得到聯(lián)萘或苯基萘基產(chǎn)物(Figure 1A)。盡管2020年湯文軍課題組高對映選擇性實(shí)現(xiàn)了聯(lián)苯類型產(chǎn)物的合成。但是在大多數(shù)例子中均需要在聯(lián)苯C-C鍵附近連有甲酰基和甲氧基,從而限制了反應(yīng)的應(yīng)用。因此發(fā)展高效的不對稱催化體系高對映選擇性實(shí)現(xiàn)聯(lián)苯產(chǎn)物的合成仍具有很大的挑戰(zhàn)。
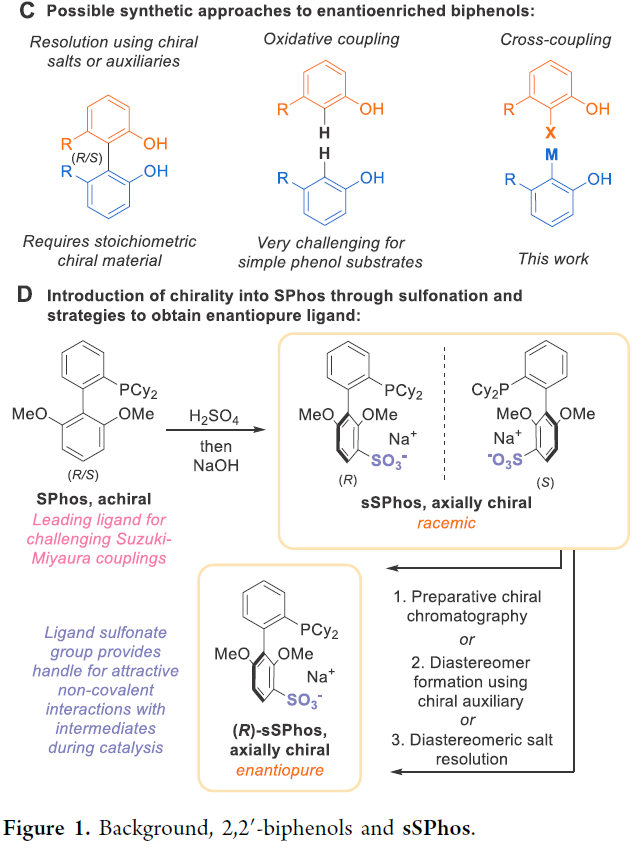
在軸手性聯(lián)苯化合物中,最重要的一類就是2,2’-聯(lián)酚,其廣泛的存在于天然產(chǎn)物中。此外,其在催化劑和配體設(shè)計(jì)上具有重要的應(yīng)用(如BINOL) (Figure 1B)。而目前高對映選擇性實(shí)現(xiàn)2,2’-聯(lián)酚的合成方法包括手性拆分、酶催化以及過渡金屬催化的氧化偶聯(lián)等,但是均具有一定的缺陷(如需要化學(xué)計(jì)量的手性試劑,底物兼容性差等)。最近,英國劍橋大學(xué)Robert J. Phipps課題組利用sSPhos作為手性配體,高對映選擇性的實(shí)現(xiàn)了Suzuki-Miyaura偶聯(lián)過程,一步構(gòu)建多種具有軸手性的2,2’-聯(lián)苯酚產(chǎn)物(Figure 1C)。
(圖片來源:J. Am. Chem. Soc.)
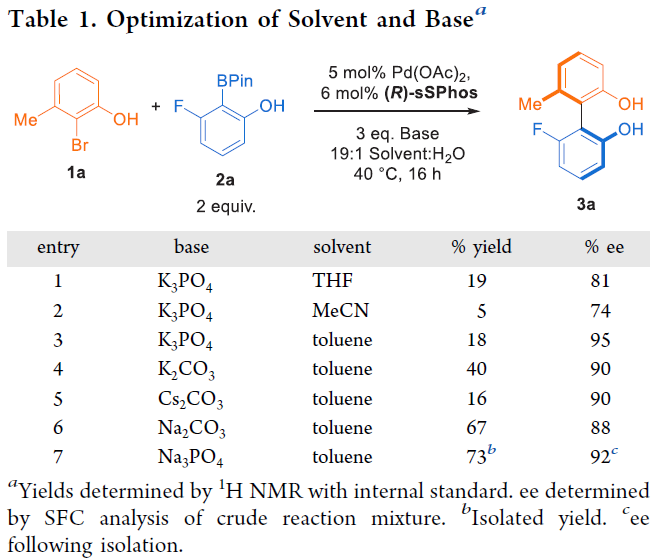
作者首先利用手性超臨界流體色譜(SFC)制備出光學(xué)純的sSPhos (Figure 1D),隨后嘗試實(shí)現(xiàn)芳基溴化物1a與硼酯2a的Suzuki-Miyaura偶聯(lián)過程,進(jìn)而實(shí)現(xiàn)具有軸手性的2,2’-聯(lián)苯酚產(chǎn)物3a的合成。通過一系列條件篩選,作者發(fā)現(xiàn)當(dāng)使用 5 mol% Pd(OAc)2, 6 mol% (R)-sSPhos, Na3PO4 (3.0 equiv), 甲苯/水(19:1)作溶劑,40 oC 反應(yīng)16小時可以以73%的分離產(chǎn)率,92%的ee值得到聯(lián)苯酚產(chǎn)物3a(Table 1, entry 7)。
(圖片來源:J. Am. Chem. Soc.)
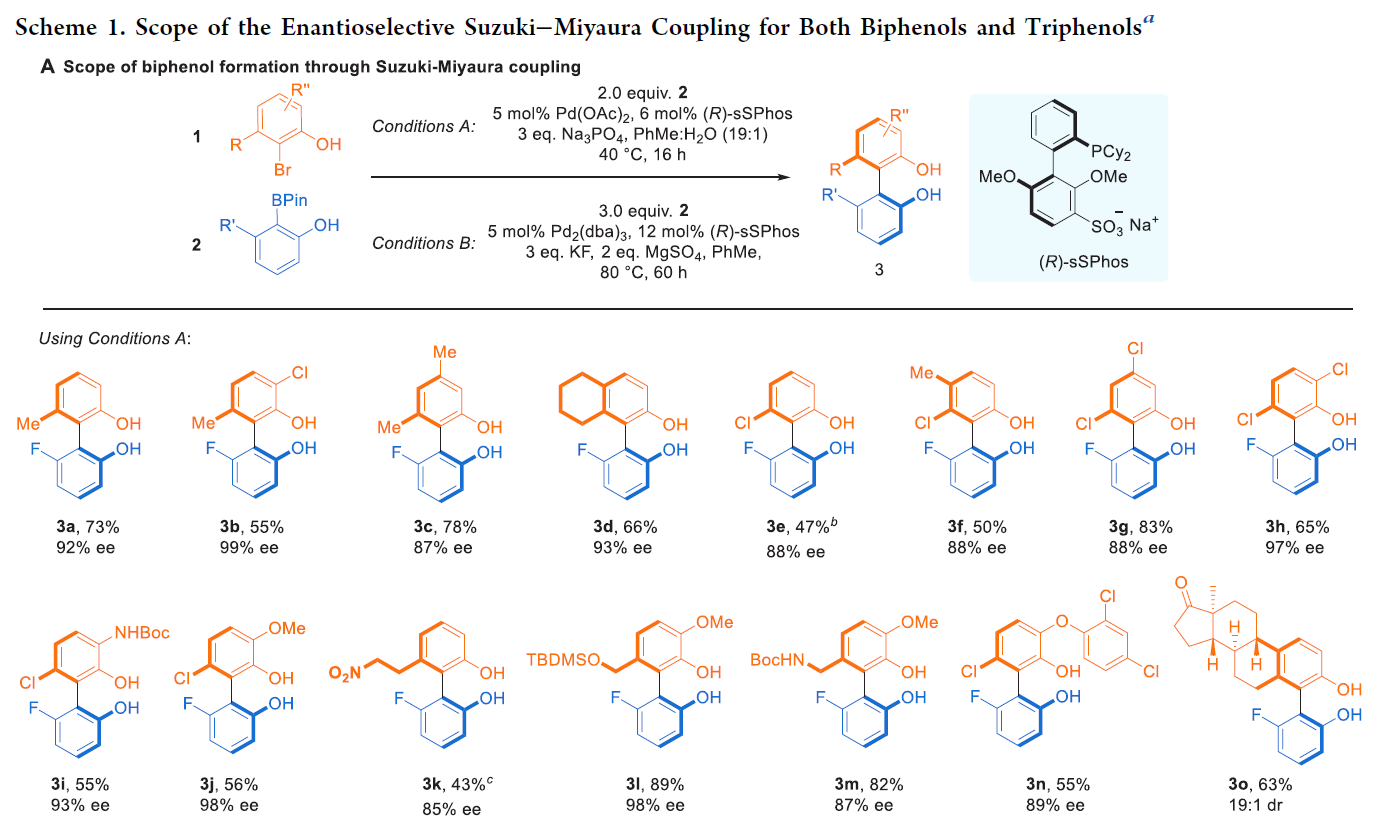
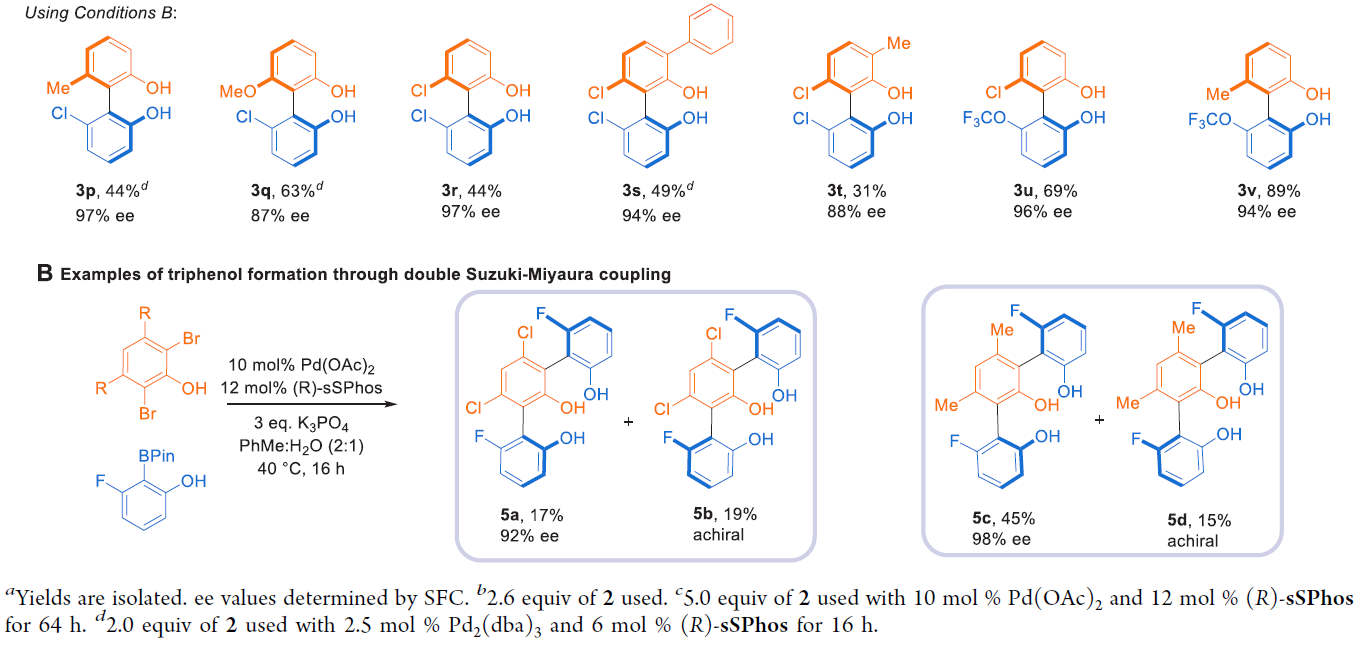
隨后,作者對此不對稱Suzuki-Miyaura反應(yīng)的底物范圍進(jìn)行探索(Scheme 1)。實(shí)驗(yàn)結(jié)果表明烷基、鹵素、硝基、硅基保護(hù)的羥基、Boc保護(hù)的胺基等官能團(tuán)均可兼容此轉(zhuǎn)化。此外,對于復(fù)雜分子,如抗菌劑triclosan、estrone等骨架也可以兼容此體系。對于一些氯和三氟甲氧基取代的硼酸酯,通過簡單的條件變化即可以良好的效率和對映選擇性實(shí)現(xiàn)產(chǎn)物3p-3v的合成(Scheme 1A)。最后,作者還利用二溴苯酚底物實(shí)現(xiàn)了雙Suzuki-Miyaura偶聯(lián)過程(Scheme 1B)。
(圖片來源:J. Am. Chem. Soc.)
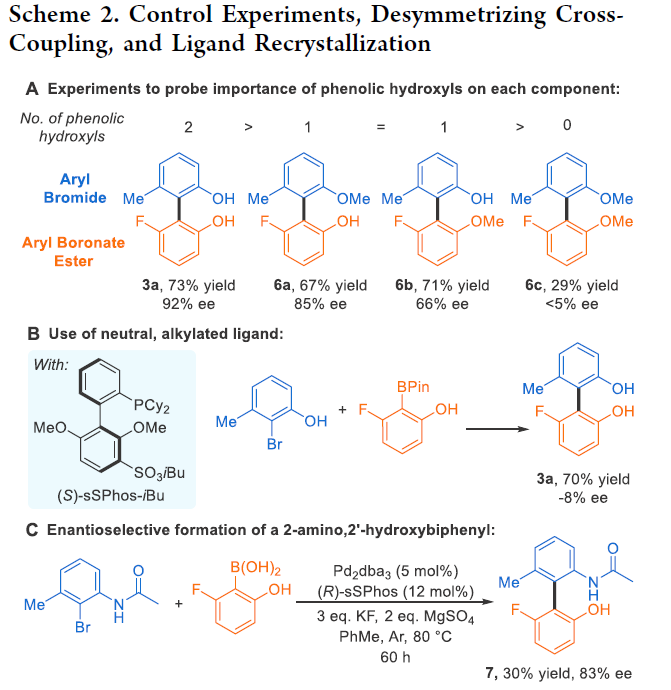
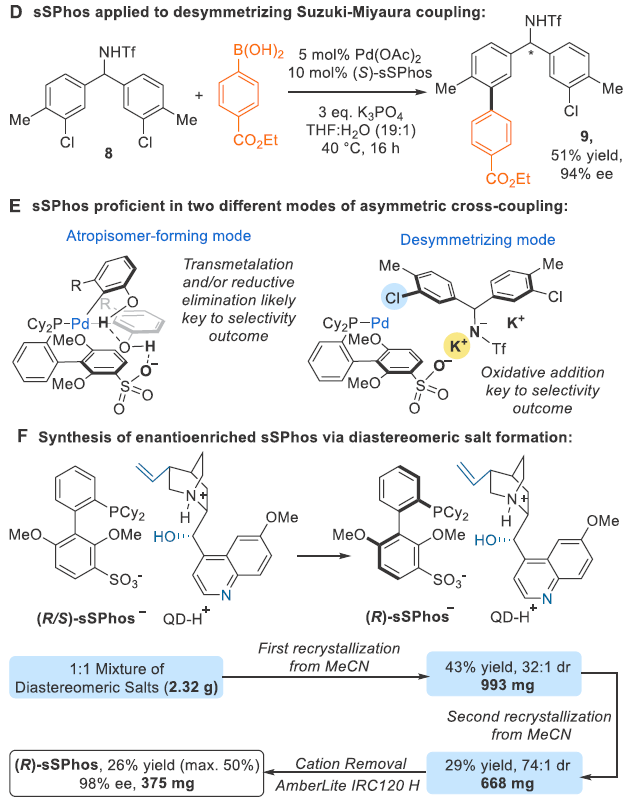
接下來,為了對反應(yīng)有更深入的了解,作者進(jìn)行了一系列控制實(shí)驗(yàn)。首先,作者發(fā)現(xiàn)硼酸和芳基溴上的酚羥基是此反應(yīng)獲得較高對映選擇性的關(guān)鍵(Scheme 2A)。此外,作者證明配體sSPhos上離子型的磺酸鹽對不對稱誘導(dǎo)過程起到了至關(guān)重要的作用(Scheme 2B)。當(dāng)?shù)孜镏蟹恿u基替換成乙酰胺基時,仍可以以83%的ee值得到產(chǎn)物,但是產(chǎn)率相對較低。由此表明此體系在類似NOBIN的骨架構(gòu)建中具有一定的應(yīng)用潛力(Scheme 2C)。接下來,作者利用光學(xué)純的sSPhos配體實(shí)現(xiàn)了去對稱化Suzuki-Miyaura偶聯(lián)過程,可以以51%的產(chǎn)率,94%的ee值得到產(chǎn)物9(Scheme 2D)。作者認(rèn)為,在阻旋異構(gòu)體形成的模型中,轉(zhuǎn)金屬化或者還原消除過程為實(shí)現(xiàn)立體選擇性的關(guān)鍵步驟;而在去對稱化過程中,氧化加成為實(shí)現(xiàn)立體選擇性的關(guān)鍵過程(Scheme 2E)。最后,作者探索了在不使用制備色譜,利用質(zhì)子化的奎尼丁作為手性陽離子,通過離子對結(jié)合以及重結(jié)晶過程實(shí)現(xiàn)了配體sSPhos的拆分(Scheme 2F)。
(圖片來源:J. Am. Chem. Soc.)
總結(jié) 英國劍橋大學(xué)Robert J. Phipps課題組利用sSPhos作為手性配體,高對映選擇性的實(shí)現(xiàn)了Suzuki-Miyaura偶聯(lián)反應(yīng),一步構(gòu)建了多種具有軸手性的2,2’-聯(lián)苯酚產(chǎn)物。此外,作者發(fā)展了高效的sSPhos拆分方法并證明了此類配體在不對稱催化過程中的應(yīng)用潛力。此反應(yīng)的發(fā)展為具有軸手性的2,2’-聯(lián)苯酚類化合物的合成提供一種新的策略。
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn