

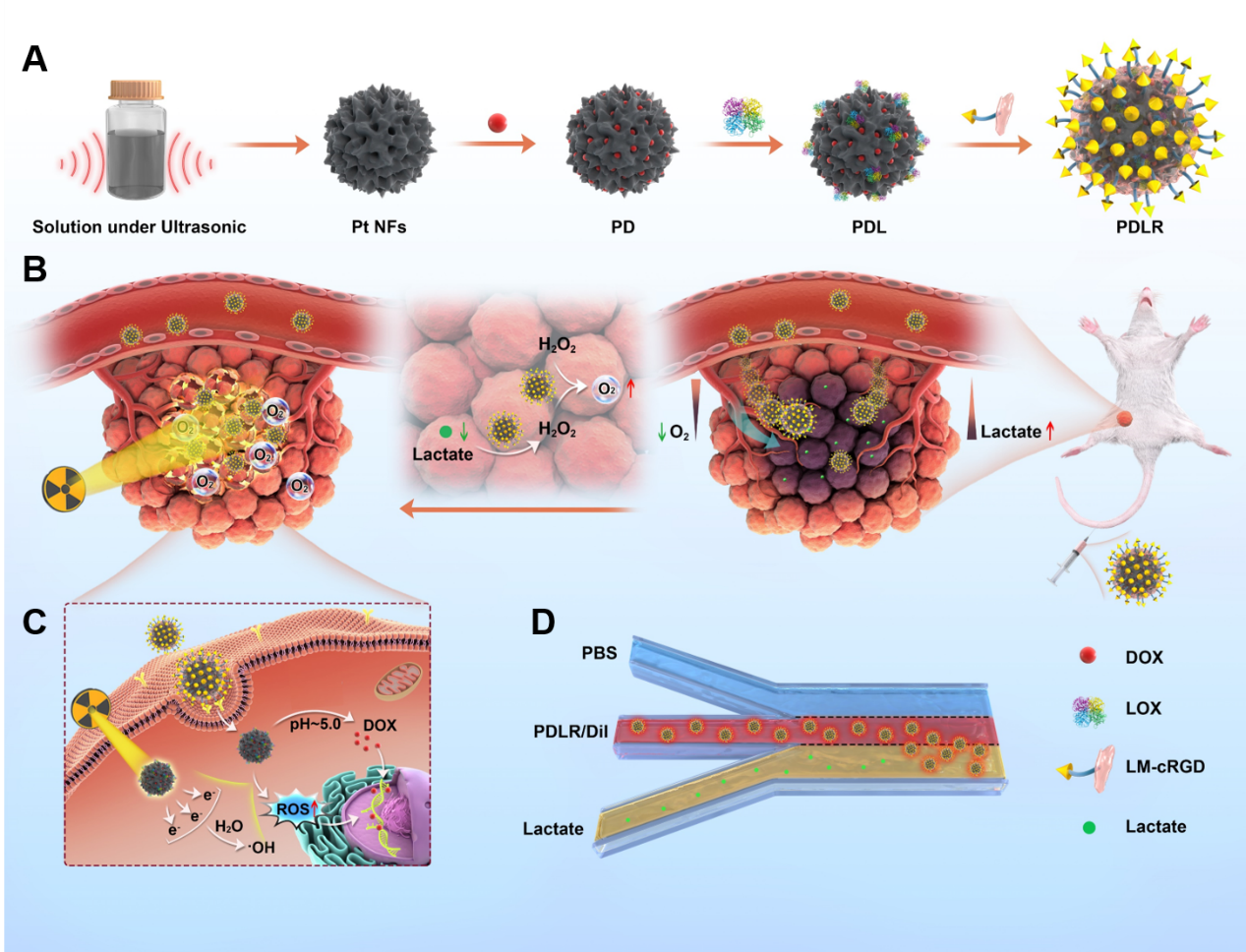
細胞或細胞成分響應特定的化學信號進行定向趨化運動(靠近或遠離化學刺激)對于許多生物活動都至關重要,這為研究者們設計“智能型”自主運動納米馬達帶來了啟發。
基于腫瘤微環境具有高濃度乳酸的特征,研究團隊采用乳酸氧化酶(LOX)修飾多功能鉑(Pt)納米粒,構建了一種具有乳酸驅動定向趨化性和級聯催化產氧作用的多功能放療增敏劑,有效促進腫瘤內部小劑量放療增敏作用,并初步驗證了其具有向乳酸溶液側偏移和腫瘤內部滲透的定向移動行為,為基于腫瘤微環境特性開發酶底物濃度梯度驅動的納米制劑定向趨化遞送和小劑量放療增敏策略提供借鑒意義,同時也為促進藥物腫瘤內部滲透等領域提供新策略。這是繼該團隊在Nature Communications(2022 May 25;13 (1) : 2906. doi: 10.1038/s41467-022-30634-8)上發表“納米毯”抑制腫瘤轉移前微環境后在抗腫瘤領域的又一進展。該研究論文的第一作者為浙江大學藥學院碩士生張振濤和仲海清,通訊作者為浙江大學藥學院高建青教授和韓旻副教授。

中樞神經組織修復是當今醫學的一大難題,脊髓損傷等中樞神經系統疾病目前尚缺少有效的治療手段,而血管生成是組織修復過程中的重要和首要環節。干細胞療法在組織修復中顯示了良好的前景,其中,多方面的證據顯示間充質干細胞(MSC)可通過對微環境中的信息進行響應和反饋從而調節損傷組織微環境并最終促進組織修復。但實際應用中,血管內皮細胞來源受限且易產生體內免疫排異反應。
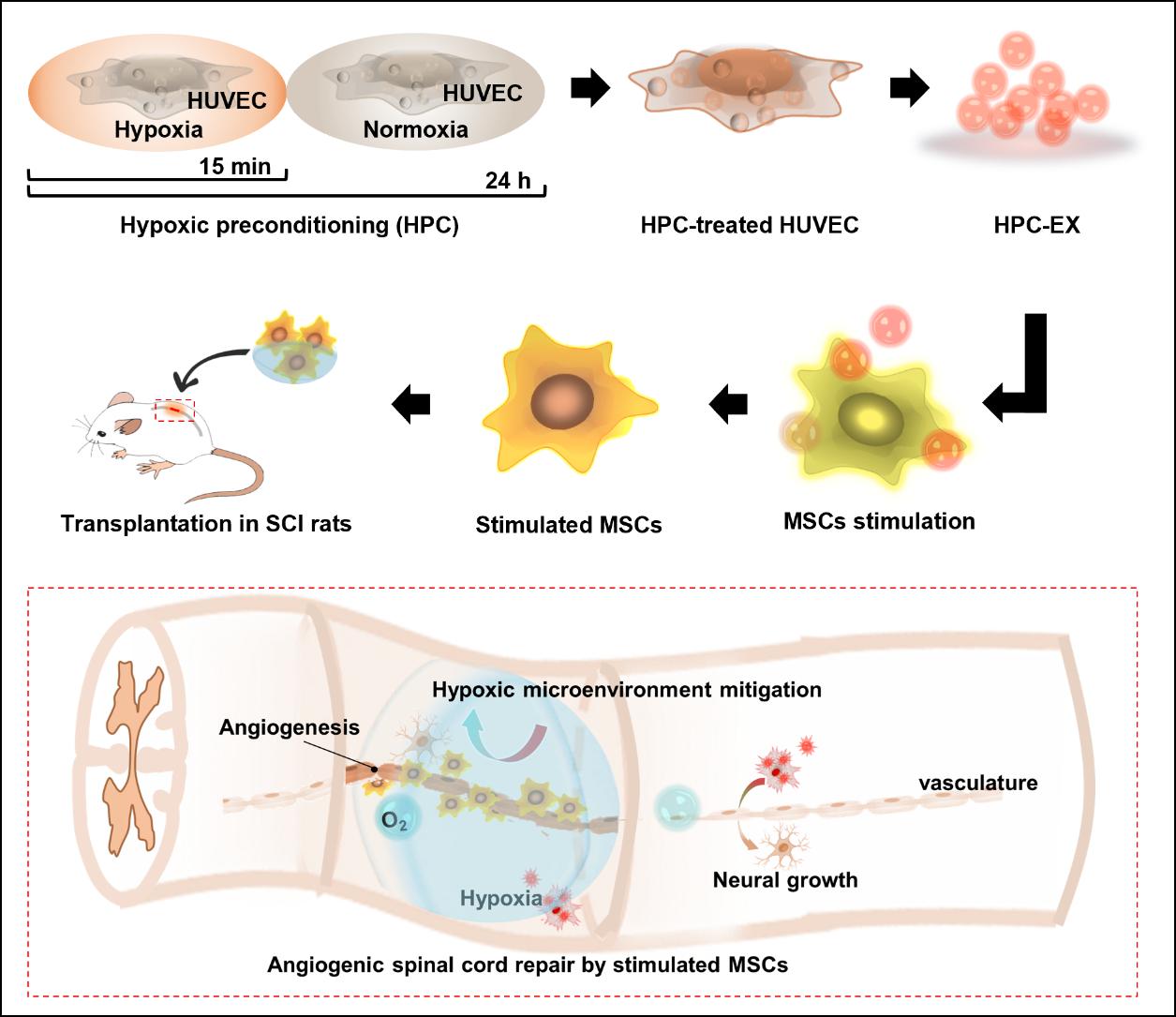
研究團隊針對脊髓損傷的缺血微環境和成血管修復治療,基于細胞外泌體在細胞-細胞交流與細胞-微環境交流中的作用,對人臍靜脈血管內皮細胞(HUVEC)進行低氧預適應(HPC)刺激并獲取其外泌體(HPC-EX),進一步利用該外泌體調控MSC細胞成血管并進行脊髓損傷治療。在低氧-常氧的HPC刺激中,時長僅15分鐘的低氧刺激即可使HUVEC產生有效促進MSC成血管的HPC-EX,攝取HPC-EX的MSC可在2小時內于基質膠中顯著成管,并在植入損傷脊髓組織后促進組織中血管生成和改善炎癥微環境,有效促進了組織的修復和神經功能恢復。該項研究為脊髓損傷組織修復治療提供了高效的促血管生成治療策略,同時也為基于外泌體和干細胞的疾病治療提供了新的啟發。該研究工作得到天津醫科大學總院骨科馮世慶教授和浙江大學醫學院附屬第一醫院骨科蔡友治教授的幫助。論文的第一作者為浙江大學藥學院博士后李黎明和博士生母佳富,通訊作者為浙江大學藥學院高建青教授和韓旻副教授,該研究受到科技部重點研發計劃“人臍帶間充質干細胞修復脊髓損傷的臨床研究”的資助。

參考資料:http://www.cps.zju.edu.cn/2022/0712/c58878a2603626/page.htm
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn