- 首頁
- 資訊
JACS:Asnovolins及相關螺環混源萜類的不對稱全合成
來源:化學加網原創 2022-07-18
導讀:近日,基于對螺環混源萜類天然產物的生源合成的研究(Figure 2),波士頓大學的John A. Porco, Jr.教授課題組利用鋰-碘交換促進的偶聯反應作為關鍵步驟成功實現了Asnovolins及相關螺環混源萜類的全合成。相關成果發表在J. Am. Chem. Soc.上(DOI: 10.1021/jacs.2c05366)。
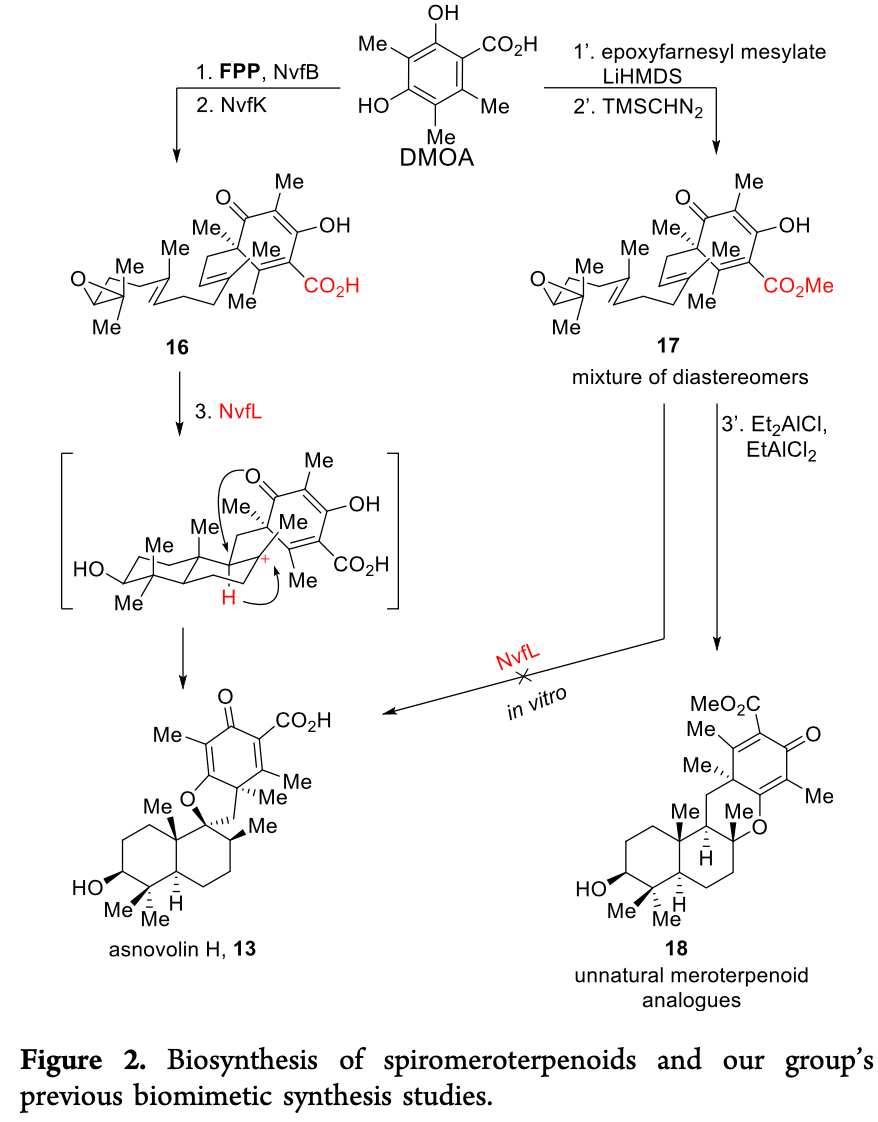
混源萜類化合物是一類雜合的源于萜類化合物的天然產物,而螺環混源萜類作為其中最獨特的存在,因其獨特的螺環骨架及萜烯和聚酮片段的高氧化態而受到了眾多有機化學家的廣泛關注。Chermesins A-D和Asnovolins A-F是分別由王斌貴團隊和Tomoo Hosoe團隊于2016年從兩種不同的真菌中分離得到的螺環混源萜類天然產物,其中chermesin B (2)具有優異的抗菌活性,而asnovolin E (3) 可抑制新生兒真皮成纖維細胞纖連蛋白的表達(Figure 1A)。2018年,Liu等人分離出fusariumins A (6) 和 fusariumins B,前者對金黃色葡萄球菌和銅綠假單胞菌具有很強的抗菌活性(MIC = 6.3 μg/mL)。從結構上看,C1'位季碳中心、螺環手性中心、熱不穩定的C12甲基和全取代二烯酮或環己酮使得螺環混源萜類的合成極具挑戰性(Figure 1D)。盡管化學家對混源萜類化合物的生物合成進行了詳細的研究(Figure 1E),但關于它們的化學合成的研究卻鮮有報道。基于對螺環混源萜類天然產物的生源合成的研究(Figure 2),波士頓大學的John A. Porco, Jr.教授課題組利用鋰-碘交換促進的偶聯反應作為關鍵步驟成功實現了Asnovolins及相關螺環混源萜類的全合成。相關成果發表在J. Am. Chem. Soc.上(DOI: 10.1021/jacs.2c05366)。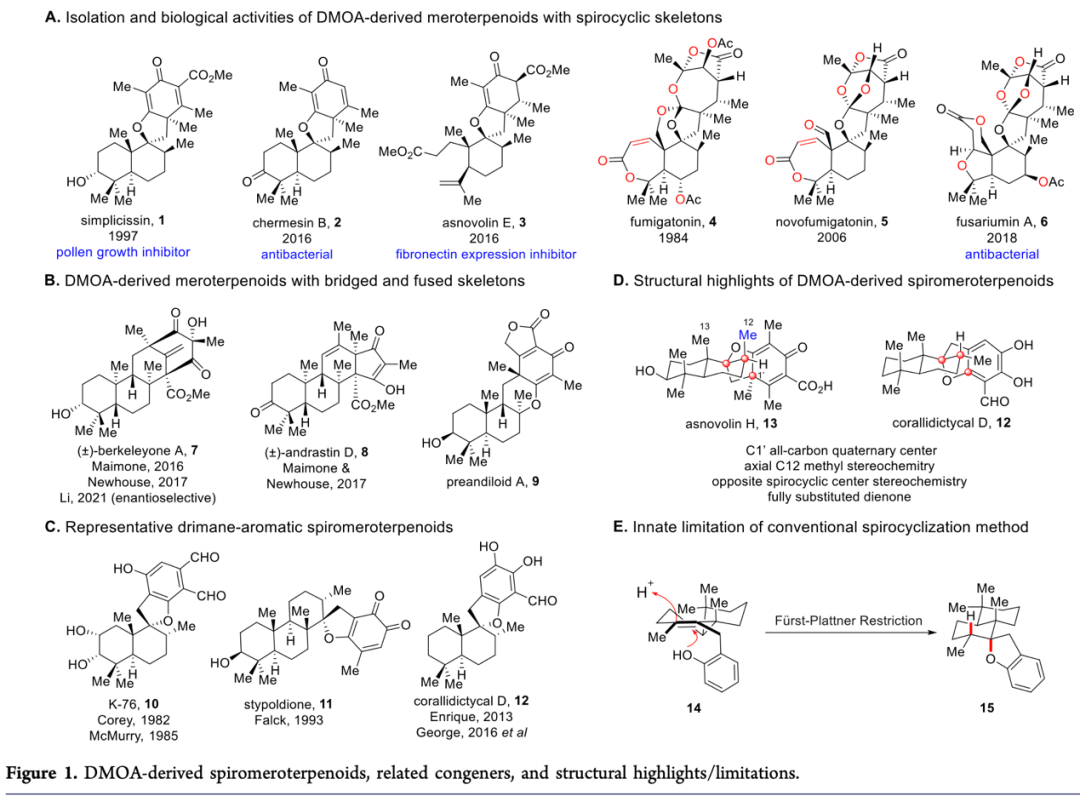
asnovolin A(19)的逆合成分析(Figure 3):基于先前提出的合成思路,作者提出假設:asnovolin A(19)可從關鍵中間體20通過后期D環官能團化得到,而中間體20可由羥基烯酮21通過關鍵的氧雜Michael加成反應獲得,中間體21則由雙環烯酮22和環己酮新戊基碘23經偶聯得到。其中,雙環烯酮22由商業可得的(R)-香芹酮經六步反應得到,化合物25可由順芷醛和Rawal二烯經不對稱D-A環加成反應得到,再經多步修飾得到環己酮新戊基碘23。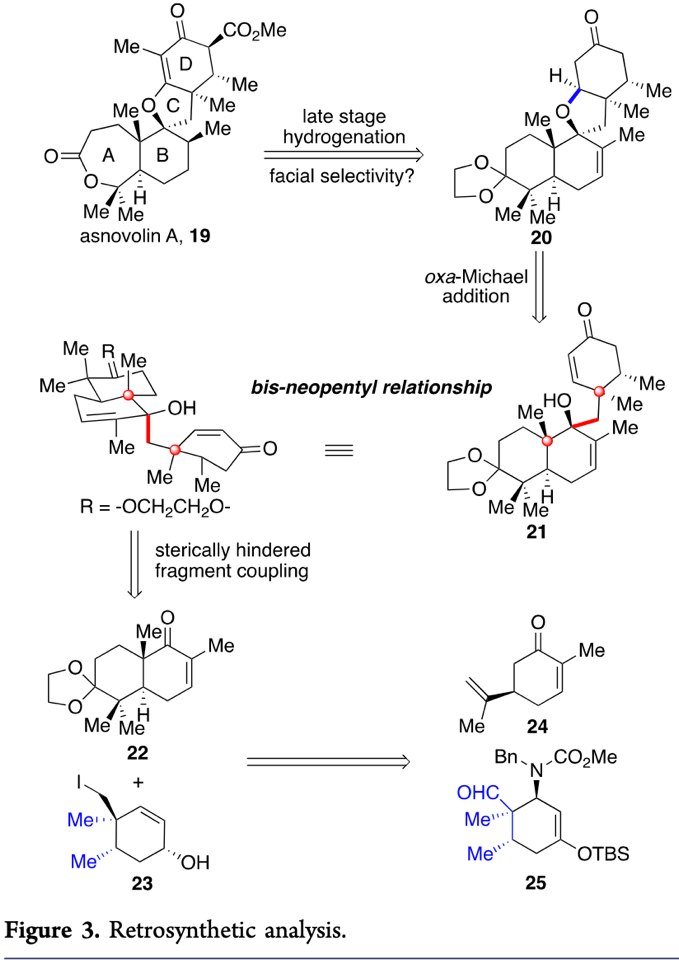
羥基烯酮26經“一鍋法”三氟甲磺酰化/SN2以兩步72%的產率得到化合物27;27經Luche還原以定量的產率得到單一非對映異構體烯丙醇23;其再經過正丁基鋰和叔丁基鋰促進的Li-I交換實現與化合物22的偶聯,并以83%的產率得到偶聯產物28,并經MnO2氧化促進的串聯烯丙基氧化/氧雜Michael加成以良好的產率得到螺環化合物20,作為關鍵的中間體片段。接下來,作者希望通過對化合物20中三取代雙鍵的立體選擇性還原實現C12甲基手性中心的構建,但DFT模型和NOESY實驗結果表明,乙烯基甲基和C6'亞甲基在空間上比較接近,且烯烴兩面的空間環境非常相似。因此,作者猜想如果β-面發生氫化,所得平伏甲基可能與C6'亞甲基發生空間相互作用。作者嘗試通過H2還原雙鍵,但反應并不發生。于是作者另辟蹊徑,利用Fe-催化的HAT還原能以優異的產率(>88%)得到單一非對映異構體還原產物29。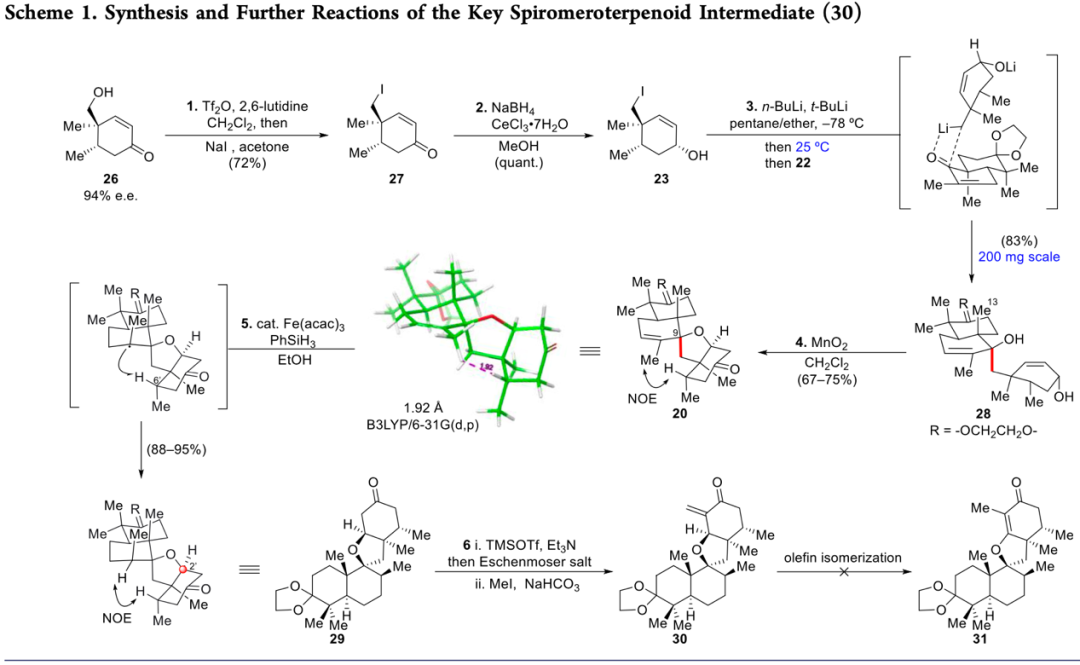
在上述研究中,HAT還原能夠立體選擇性還原雙鍵而對C6'亞甲基的立體化學沒有影響引起了作者的興趣,因此,作者利用氘代實驗對其反應機理進行了研究(Scheme 2)。結果顯示,當用PhSiD3替換PhSiH3時,僅有C7位直立H發生氘代,且氘代率為100%;當用EtOD為溶劑時,C5′位47%的H發生氘代,說明C-H提取可能發生在羰基α-位H而不是C6'亞甲基處;同時使用PhSiD3和EtOD時,C6'亞甲基仍不發生氘代。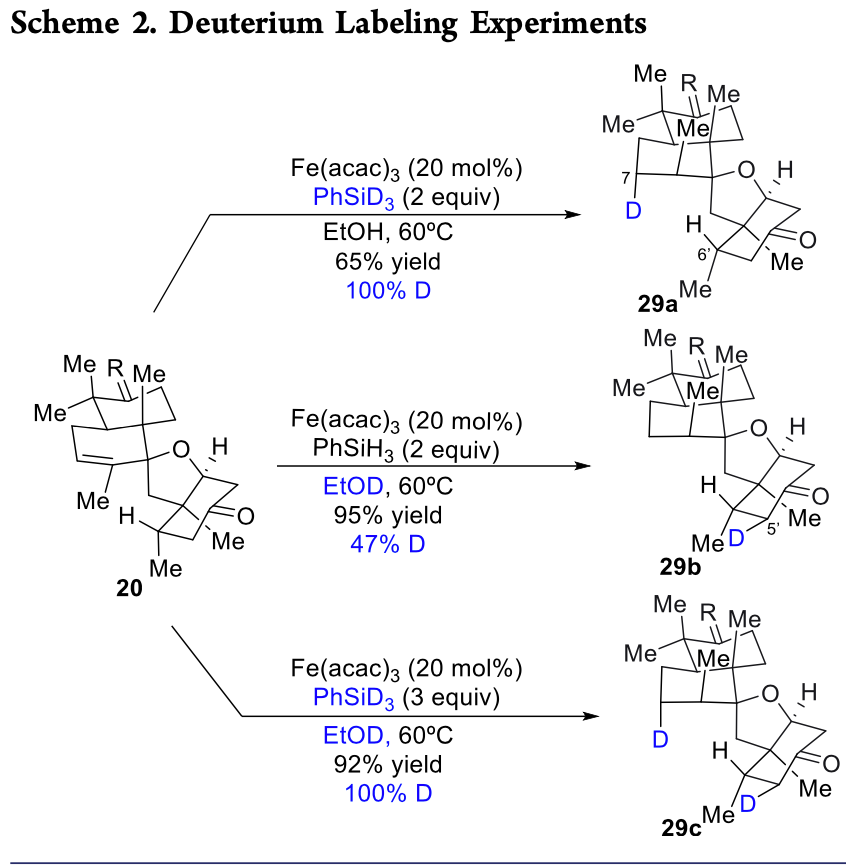
五種Asnovolin天然產物的匯聚式合成(Scheme 3):完成關鍵螺環骨架的構建后,化合物29在IBX氧化條件下發生去飽和化,以72%的產率得到烯酮32,其中4 ?分子篩和Na2HPO4能夠防止縮醛水解;化合物32經CAN/I2處理,以84%的產率引入碘得到化合物33;再經Pd-催化的Suzuki偶聯以95%的產率得到甲基化產物31。接著,作者嘗試再次利用IBX將化合物31去飽和化,但反應幾乎不發生,多番嘗試后,發現苯亞硒酸酐能夠將化合物31去飽和化,再經酸水解縮醛以86%的產率得到chermesin B (2)。此外,化合物31經KHMDS處理以94%的產率得到酰基化產物34,經縮醛水解以77%的產率得到asnovolin J (35),化合物35再經Sc(OTf)3促進的Baeyer-Villiger氧化能以76%的產率得到asnovolin A (19),而通過p-TsOH促進的內酯水解能夠將化合物19以41%轉化成asnovolin E (3)。除此之外,化合物34經“一鍋法”去飽和化/水解以兩步84%的產率得到化合物36,但C3羰基的立體選擇性還原具有挑戰性,作者發現大位阻還原劑L-Selectride和LiAlH(t-Bu)(i-Bu)2雖能夠有效還原C3羰基,但產物為非對映異構體混合物(1.5:1 dr),說明缺電子二烯酮的C5′-C6′雙鍵不適用于活潑金屬氫化物,經多次嘗試后發現通過原位生成(i-PrO)2AlCl促進的Meerwein-Ponndorf-Verley還原能以69%的產率得到構型正確的還原產物simplicissin (1)。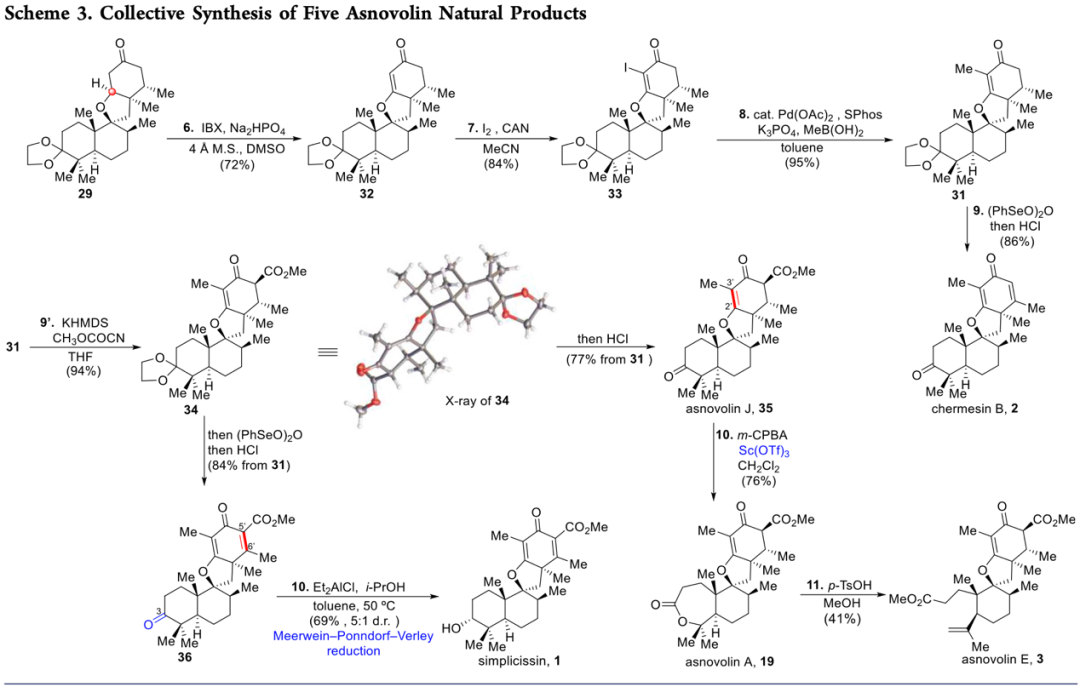
最后,作者認為這種高反應活性但條件溫和的還原方法具有顯著的化學選擇性和立體選擇性,可能能夠應用于其他天然產物全合成中。作者對其反應機理提出了假設(Figure 5),認為從β-面通過六元過渡態TS3向C3酮的分子內轉移氫是更有利的,其中鋁與遠離偕二甲基、異丙基及甲基的羰基孤對電子發生螯合,而從α-面還原可能會受到異丙基與C1-H、C5-H、C7'-Me和螺環間的空間相互作用的影響,因此不太有利。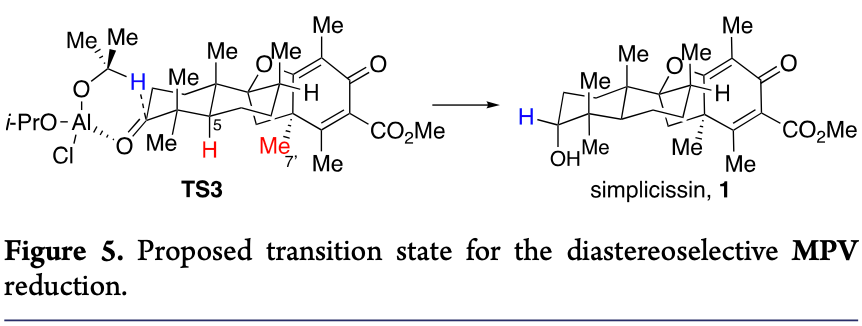
小結:波士頓大學的John A. Porco, Jr.教授課題組利用鋰-碘交換促進的偶聯反應作為關鍵步驟,以商業可得的化合物為起始物料成功實現了Asnovolins及相關螺環混源萜類的全合成,所開發的方法能夠獲得用于生物學研究的各種螺環混源萜類似物。通過這種方法獲得各種低氧化態的螺環混源萜類化合物為使用化學和化學酶促合成高度氧化的螺環混源萜類化合物(如新煙曲霉素)提供了堅實的基礎。文獻詳情:
Feng Yang and John A. Porco Jr.*.Unified, Asymmetric Total Synthesis of the Asnovolins and Related Spiromeroterpenoids: A Fragment Coupling Approach.J. Am. Chem. Soc.2022.http://doi.org/10.1021/jacs.2c05366

聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn









