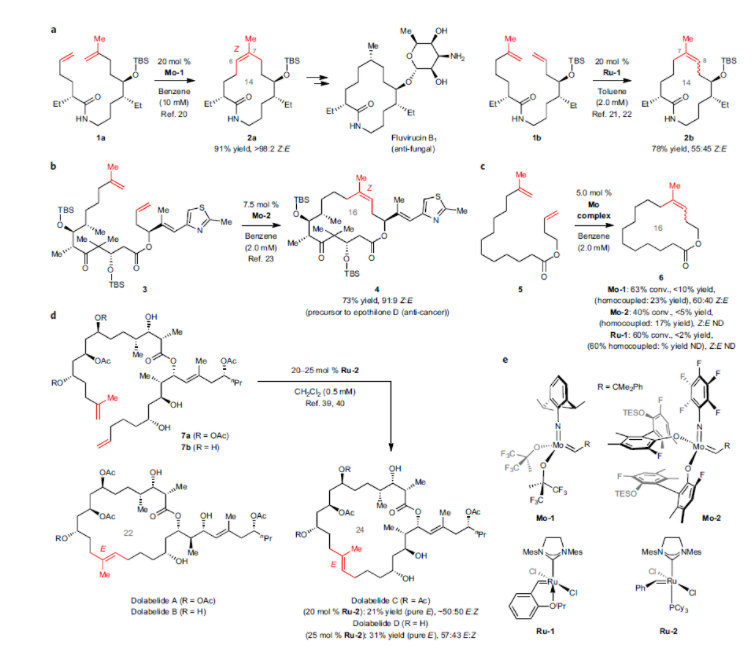
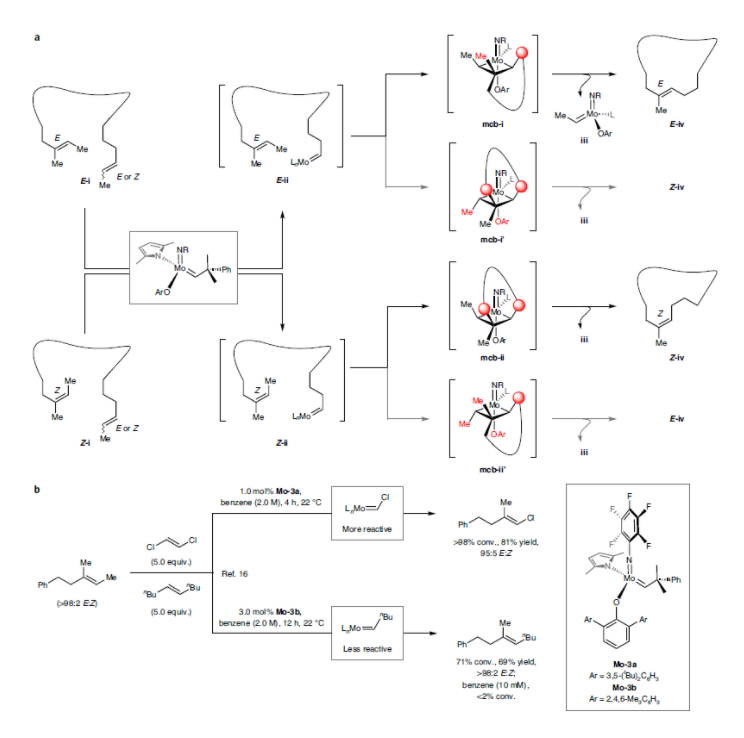
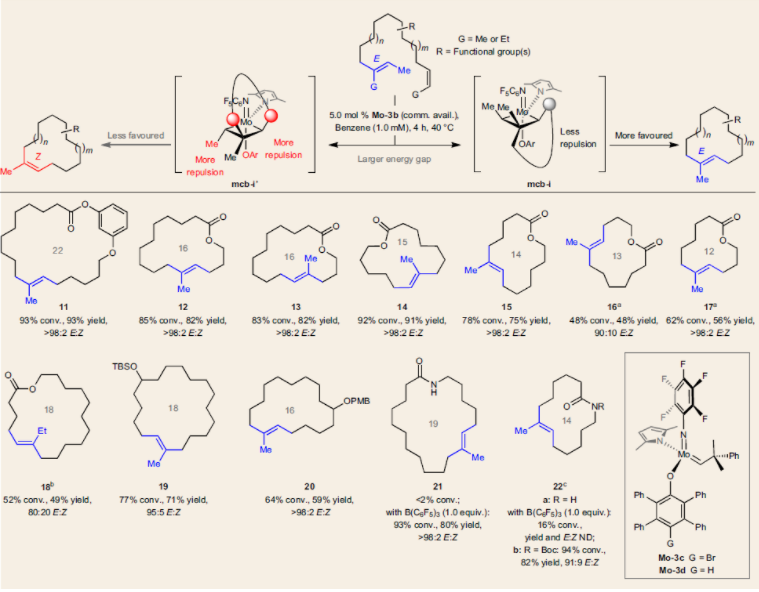
許多藥物分子都擁有大環(huán)三取代烯烴結(jié)構(gòu),而MRCM常常用來合成具有生物活性的大環(huán)三取代烯烴,然而僅僅在少數(shù)情況下可以得到單一的雙鍵異構(gòu)體,大多數(shù)情況下會得到Z/E混合的一對異構(gòu)體,產(chǎn)物大環(huán)三取代烯烴的立體化學(xué)取決于底物的構(gòu)象,往往也很難預(yù)測產(chǎn)物的具體構(gòu)型。在作者前期的對Fluvirucin B1的合成工作中,使用Mo-1催化劑以91%的收率,>98:2的 Z/E選擇性得到了十四元環(huán)產(chǎn)物2a,在后續(xù)的研究中作者發(fā)現(xiàn)高Z/E選擇性是由底物的構(gòu)象控制,而并非由催化劑控制,能得到目標Z-式的三取代烯烴2a更多的是一種巧合。而對于1a的甲基區(qū)域異構(gòu)體1b,使用Ru-1催化劑進行MRCM時,Z/E 僅為55:45(圖1,a)。隨后作者使用Mo-2催化劑在epothilone D前體的合成中進行了運用,以73%的收率,91:9的Z/E選擇性得到產(chǎn)物4,然而在缺少官能團的底物5中進行MRCM反應(yīng)時,收率和Z/E選擇性均不佳(圖1,b)。這也表明Mo-2對于立體選擇性的控制并不是很強。又比如對于使用MRCM策略合成癌癥抑制劑dolabelides也是沒有選擇性的,只能得到E-式的dolabelides C和D無法得到dolabelides A和B(圖1,c)。從上述例子可以看出,采取MRCM合成三取代大環(huán)烯烴時,如何控制產(chǎn)物的烯烴片段的立體化學(xué),仍是該領(lǐng)域的難點和熱點。圖1. MRCM中未解決的問題和挑戰(zhàn)(圖片來源:Nat. Chem.)作者采取了立體保留的MRCM策略,即通過底物中Z-(或者E-)式的三取代烯烴以得到Z-(或者E-)式的大環(huán)三取代烯烴。含有E-三取代烯烴(例如E-i)的二烯和催化劑反應(yīng)轉(zhuǎn)化為E-ii,隨后發(fā)生分子內(nèi)的[2+2]以得到中間體mcb-i/mcb-i’(金屬環(huán)丁烷)。由于mcb-i'中存在Cα甲基和芳氧基配體的空間位阻,所以mcb-i在能量上更為有利,更易形成大環(huán)三取代烯烴E-iv。類似地,Z-i更易轉(zhuǎn)化為Z-iv(圖2,a)。2017年Amir H. Hoveyda與Thach T. Nguyen曾合作報道了使用Mo-3a和Mo-3b催化劑,通過立體保留策略的分子間的交叉烯烴復(fù)分解反應(yīng)(圖2,b),可以實現(xiàn)高收率和高立體選擇性。然而對于MRCM和交叉烯烴復(fù)分解反應(yīng)仍存在很大的差異:(1) 交叉烯烴復(fù)分解反應(yīng)通常在2.0 M 濃度(溶劑僅用于添加鉬絡(luò)合物)。而對于MRCM,通常在0.5-2.0 mM 濃度中進行,低濃度溶液有利于大環(huán)的形成。(2) 交叉烯烴復(fù)分解反應(yīng)可以使某一種原料大大過量以促進反應(yīng)的進行。(3)大多數(shù)已知的交叉復(fù)分解反應(yīng)得到的三取代烯烴都帶有小的活性取代基(如鹵素或腈基)以促進反應(yīng)的進行。所以雖然作者曾報道過立體保留策略分子間的交叉烯烴復(fù)分解反應(yīng),對于MRCM而言仍是一次全新的挑戰(zhàn)。圖2. MRCM的可能反應(yīng)歷程(圖片來源:Nat. Chem.)作者首先使用E-8作為模型底物進行了MRCM的模型反應(yīng)(圖3,a)。使用Mo-2, Mo-3a的效果均不好,當(dāng)使用Mo-3b作為催化劑時,以58%的轉(zhuǎn)化率,46%的收率,E/Z為66:34。沒有觀察到自身偶聯(lián)的產(chǎn)物生成,回收的原料中發(fā)現(xiàn)了雙鍵的異構(gòu)化。據(jù)此作者也提出了可能的反應(yīng)歷程。E-8可能通過亞烷基E-10和mcb-iii,轉(zhuǎn)化E-9和syn-iii(圖3,b)。得到的亞乙基Mo配合物可以與E-8反應(yīng)再生成E-10和Z-丁烯。Z-丁烯可以與syn-iii反應(yīng)經(jīng)mcb-i得到E-丁烯和anti-iii,而anti-iii可能比syn-iii的能量更高,反應(yīng)性更強。anti-iii可以經(jīng)mcb-v與底物E-8反應(yīng)生成Z-8,然后轉(zhuǎn)化為Z-9和Z-10,導(dǎo)致烯烴立體異構(gòu)體純度的下降。同時E-丁烯可以與syn-iii反應(yīng)生成ent-anti-iii,從而進一步降低立體選擇性。根據(jù)提出的反應(yīng)機理,在反應(yīng)過程中除去生成的丁烯可以更好的保留烯烴的立體化學(xué)。隨后作者采取了如減壓,降低反應(yīng)濃度均可以提高反應(yīng)的轉(zhuǎn)化率,收率和產(chǎn)物中的三取代雙鍵的E/Z的比例(如1.0 mM時,89%的轉(zhuǎn)化率,76%的收率,>98% E/Z)(圖3,c)。圖3. MRCM模型反應(yīng)及其機理(圖片來源:Nat. Chem.)隨后,作者首先對E-三取代烯烴的底物普適性進行了探究(表1)。對于E-三取代烯烴的MRCM反應(yīng),如前文機理所探討的,mcb-i的Cβ甲基靠近大環(huán),mcb-i'與Cα甲基則存在更大的空間位阻,同時mcb-i中的芳氧基配體和大環(huán)片段的位阻較mcb-i’更小,會更有利于E-大環(huán)三取代烯烴的生成。作者合成了從12元到22元的E-大環(huán)三取代烯烴內(nèi)酯(表1,11-17),產(chǎn)率為48-93%,90:10至>98:2 的E/Z。表1. E-三取代烯烴的底物篩選(圖片來源:Nat. Chem.)對于Z-三取代烯烴的MRCM反應(yīng),mcb-ii中為順式大環(huán),存在一定的空間位阻。但是在mcb-ii’中,Cα甲基與芳氧基配體存在更大的空間位阻。所以產(chǎn)物還是以Z-大環(huán)三取代烯烴為主,其相應(yīng)的立體異構(gòu)體(三取代烯烴的順反異構(gòu)體)比例較E-三取代烯烴的反應(yīng)會較低。作者對Z-三取代烯烴的底物普適性也進行了探究(表2)。同樣合成了從12元到22元的E-大環(huán)三取代烯烴內(nèi)酯(表2,23-33b),產(chǎn)率為40-88%,E/Z為55:45至>98:2。值得一提的是,Mo-3e催化劑對于31的形成是非常關(guān)鍵的。
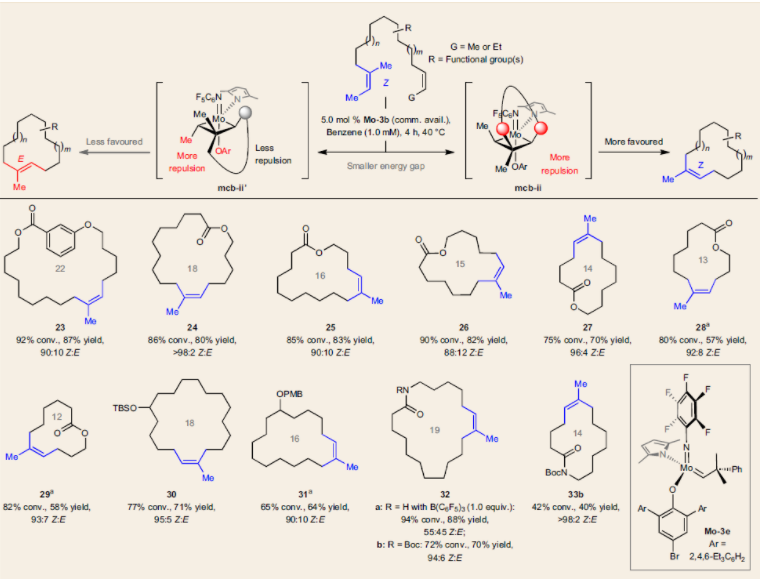
表2. Z-三取代烯烴的底物篩選(圖片來源:Nat. Chem.)
前述工作證明了立體保留策略是具有一定的可行性的,還有一個關(guān)鍵問題就是立體保留能在多大程度上對抗底物控制的選擇性。于是作者選擇了十四元大環(huán)內(nèi)酰胺fluvirucin B1的前體化合物34a進行了探究(圖4,a)。在圖1a中,1a至2a的轉(zhuǎn)化說明底物控制的情況下,是以得到Z-式產(chǎn)物為主。而當(dāng)使用三取代烯烴前體,使用Mo-3b催化劑,并加入一分子B(C6F5)3進行立體保留的MRCM反應(yīng)時,以55%收率,Z/E = 23/77得到E-式為主的產(chǎn)物E-2a。作者認為酰胺氫的存在使得底物的構(gòu)象更加自由,其中一些構(gòu)象可以發(fā)生底物控制的MRCM反應(yīng)以得到Z-式產(chǎn)物。于是作者將酰胺進行了保護得到了34b,再進行MRCM反應(yīng)時可以以66%的收率,Z/E = 8/92得到E-2c。這一實驗展現(xiàn)了立體保留的MRCM的巨大應(yīng)用前景,使用該方法可能可以對任何的大環(huán)候選藥物進行骨架的合成。

圖4. 34a和dolabelide C的合成(圖片來源:Nat. Chem.)Dolabelide C是具有11個手性中心的二十四元大環(huán)化合物,隨后作者將該方法運用到了dolabelide C的全合成中(圖4,b),進一步的展現(xiàn)了該方法的強大。首先快速合成了醛36和酮38,通過Aldol反應(yīng)以73%的收率,91:9 的d.r.值得到了β-羥基酮39。隨后通過幾步官能團轉(zhuǎn)化得到了40。另外一個片段44則是由R-1,2-環(huán)氧戊烷經(jīng)幾步簡單轉(zhuǎn)化而來。隨后44與40發(fā)生縮合反應(yīng)得到了三取代烯烴化合物45,在10 mol%的Mo-3b催化作用下,順利的以79%的轉(zhuǎn)化率,66%的收率,>98:2 E/Z得到了大環(huán)三取代烯烴46,并通過兩步轉(zhuǎn)化,以39步總步數(shù),19步最長線性步驟合成了dolabelide C。而MRCM是在整個合成的第37步,這也證明了該方法的可靠性和穩(wěn)定性。總結(jié):Amir H. Hoveyda教授課題組研究了一種新型的立體保留的,Z/E-三取代烯烴參與的MRCM反應(yīng)構(gòu)建了Z/E-大環(huán)三取代烯烴的方法,并提出了可能的反應(yīng)機理。首先介紹了MRCM領(lǐng)域存在的問題,隨后進行了使用三取代烯烴參與的MRCM的模型反應(yīng),同時對Z,E-式的三取代烯烴分別進行了底物普適性研究,可以實現(xiàn)12-22元環(huán)的合成。作者在復(fù)雜底物中進行了方法學(xué)的運用后,采用該方法完成了天然產(chǎn)物dolabelide C的合成,研究工作層層遞進,該方法為大環(huán)三取代烯烴的合成提供了很大的便利,非常具有創(chuàng)新性。Mu, Y., Hartrampf, F.W.W., Yu, E.C. et al. E- and Z-trisubstituted macrocyclic alkenes for natural product synthesis and skeletal editing. Nat. Chem. 14, 640–649 (2022). https://doi.org/10.1038/s41557-022-00935-y