

間充質干細胞(MSC)具有多向分化的潛能,可以在一定的條件下誘導分化為成骨細胞,用于治療骨質疏松等骨相關疾病,如何特異性誘導MSC成骨分化是關鍵。
使用納米材料誘導MSC定向分化近年來受到廣泛關注,特別是可以通過近紅外光進行體內調控細胞分化的上轉換納米材料(UCNP)。中山大學腫瘤防治中心楊安力/華南師范大學黎錦明制備了一種UCNP多功能納米顆粒,用于光控誘導MSC成骨分化治療骨質疏松,同時通過熒光檢測成骨分化評價治療效果。
體內外實驗結果表明,制備的多功能UCNP首先作為藥物載體,負載可以特異性誘導MSC成骨分化的小分子藥物淫羊藿苷(ICA)并將其靶向輸送到MSC內,然后通過近紅外光控制釋放ICA,誘導MSC成骨分化,治療骨質疏松大鼠癥狀。誘導MSC成骨分化后,UCNP又作為熒光探針,其表面修飾的金屬蛋白酶13(MMP13)敏感肽被成骨分化產生的MMP13酶酶切,從而恢復UCNP的650 nm發射熒光,達到熒光檢測MSC成骨分化,評估骨質疏松治療效果的目的。
綜上所述,該研究開發的多功能UCNP系統為使用納米技術治療骨質疏松提供了一種有效的工具。
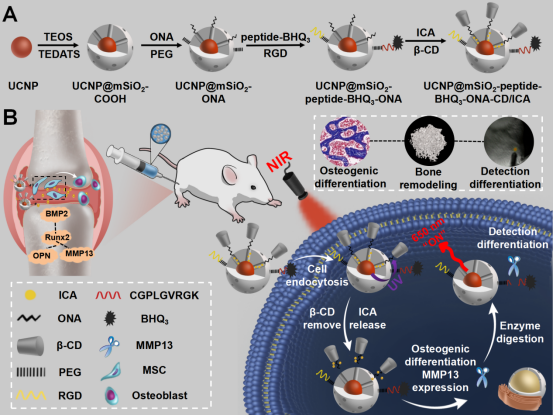
圖1. 上轉換納米粒光控誘導MSCs成骨分化治療骨質疏松。A)上轉換納米粒及其納米復合物制備示意圖。B)上轉換納米復合物光控誘導MSCs成骨分化緩解骨質疏松大鼠癥狀及實時檢測成骨分化狀態。
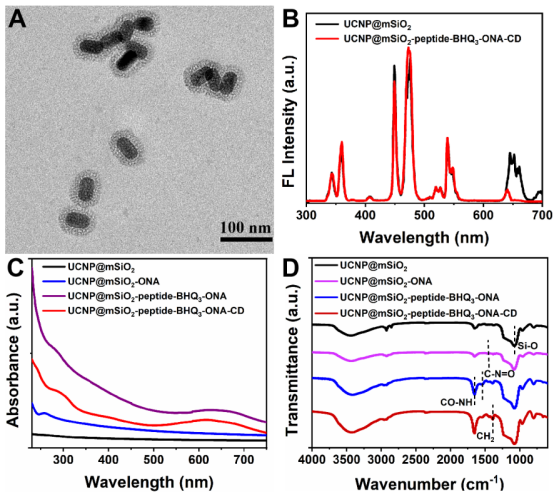
圖2. 上轉換納米粒的表征。
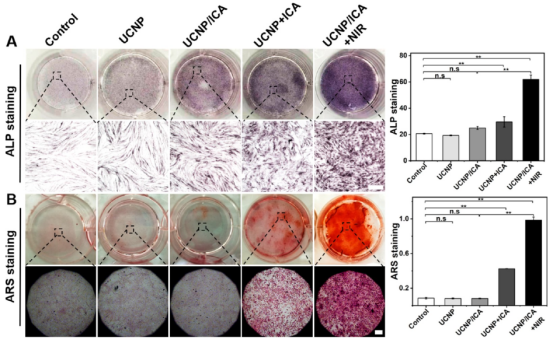
圖3. 上轉換納米復合物光控釋放藥物ICA誘導MSCs成骨分化(ALP/ARS染色)。
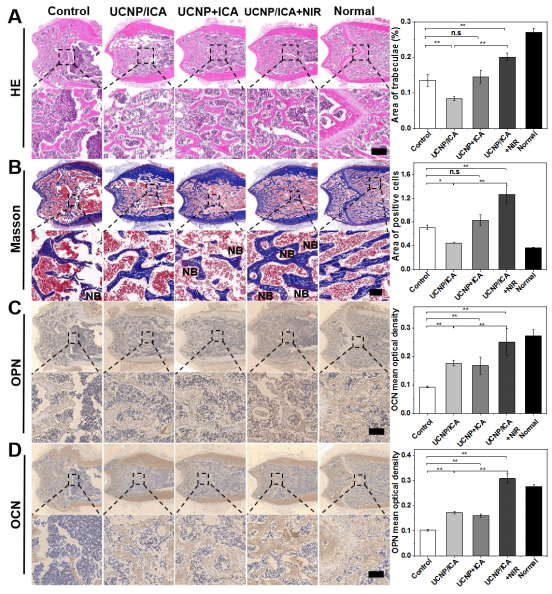
圖4. 上轉換納米復合物光控誘導MSCs成骨分化治療骨質疏松大鼠。A)HE染色。B)Masson染色。C)和D)免疫組化染色成骨分化相關蛋白表達。
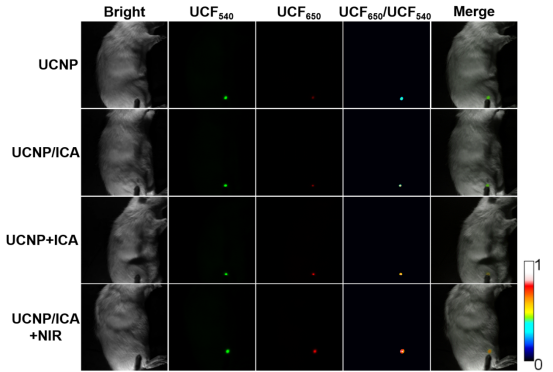
圖5. 上轉換納米粒作為熒光探針體內實時檢測MSCs成骨分化狀態,為治療骨質疏松效果提供評價。
以上成果發表在ACS Nano(2022, 16, 5, 8399-8418)上,論文第一作者為華南師范大學生物光子學研究院碩士研究生閆瑞,通訊作者為華南師范大學生物光子學研究院黎錦明研究員,共同通訊作者為中山大學腫瘤防治中心楊安力博士.
原文鏈接:https://pubs.acs.org/doi/10.1021/acsnano.2c02900
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn