



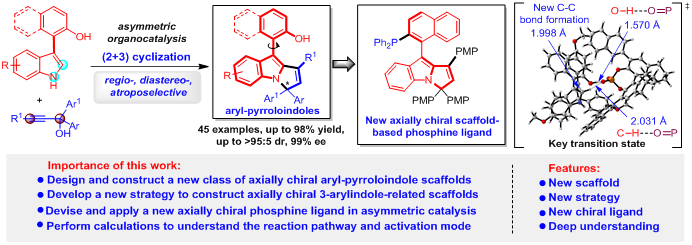
軸手性二芳基骨架是一類重要的手性結構單元,不僅廣泛存在于天然產物、藥物活性分子以及功能材料中,而且被應用于手性配體和手性催化劑中。所以,催化不對稱構建軸手性骨架引起了化學工作者們的強烈關注。目前,該領域發(fā)展尤為迅速的是軸手性六元(雜)芳基骨架的構建,例如:軸手性聯(lián)萘、聯(lián)苯和1-芳基異喹啉骨架。與之相比,軸手性五元雜芳基骨架的催化不對稱構建卻發(fā)展緩慢,主要是由于此類骨架存在鄰位基團距離較遠、旋轉能壘較低、構型穩(wěn)定性較差等挑戰(zhàn)性問題(圖1a)。因此,催化不對稱構建軸手性五元雜芳基骨架的探索依然是任重而道遠。
吲哚是一類重要的五元雜芳環(huán),不僅具有較高的富電性和芳香性,而且含有NH基團(圖1b)。吲哚的結構特點可以為軸手性吲哚骨架帶來一些獨特的性質,如改變電子云密度、調節(jié)空間位阻、實現(xiàn)后官能團化和作為氫鍵給體等。因此,近年來,催化不對稱構建基于吲哚的軸手性骨架發(fā)展為一個新興的研究領域,化學工作者構建了一系列新穎的軸手性吲哚骨架,例如:軸手性N-芳基吲哚、3-芳基吲哚、2-芳基吲哚以及雙吲哚骨架等(圖1c)。盡管如此,該領域仍然處于起步階段,存在一些亟待解決的問題,例如:(1)設計與構建基于吲哚的新型軸手性骨架;(2)開發(fā)相關軸手性骨架在手性配體、手性藥物、手性材料等領域的應用。
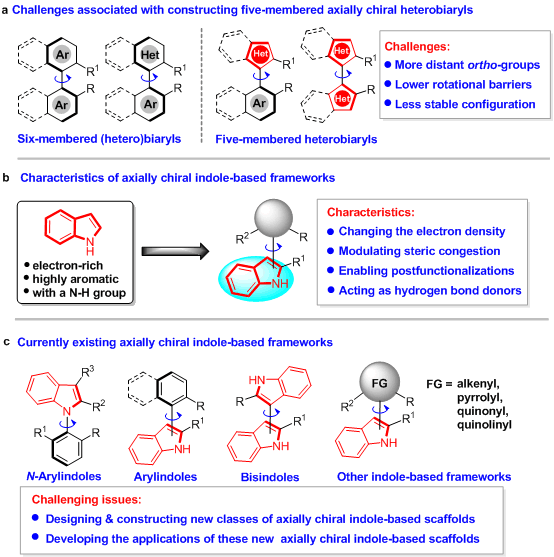
圖1 催化不對稱構建軸手性二芳基骨架的研究概況
在目前已構建的軸手性吲哚骨架中,3-芳基吲哚骨架由于在手性膦催化劑和生物活性分子中的應用(圖2a),該類骨架的構建具有重要意義,而不對稱有機催化被認為是構建軸手性骨架的一種強有力方法。目前,不對稱有機催化下構建軸手性3-芳基吲哚骨架的代表性策略主要有三種(圖2b)。第一種策略是手性磷酸(CPA)催化下吲哚環(huán)與芳環(huán)的直接偶聯(lián)策略,主要包括石楓課題組發(fā)展的2-吲哚甲醇與2-萘酚的偶聯(lián)反應(Eq. 1, Angew. Chem. Int. Ed. 2017, 56, 116)、南方科技大學譚斌課題組發(fā)展的2-取代吲哚與偶氮萘或亞硝基萘的偶聯(lián)反應(Eq. 2, Nat. Chem. 2018, 10, 58; Chem 2020, 6, 2046);第二種策略是有機催化下原位構建吲哚環(huán)的策略,主要包括譚斌課題組發(fā)展的CPA催化下2-取代吲哚與偶氮萘或亞硝基萘的重排反應(Eq. 3, Nat. Chem. 2018, 10, 58; Chem 2020, 6, 2046)、新加坡國立大學趙宇課題組發(fā)展的手性氮雜卡賓(NHC*)催化下炔丙醇與烯醛的串聯(lián)反應(Eq. 4, J. Am. Chem. Soc. 2019, 141, 17062);第三種策略是CPA催化下外消旋3-芳基吲哚的親核加成反應,主要是石楓課題組發(fā)展的3-芳基吲哚平臺分子與偶氮二羧酸酯或鄰羥基芐醇的加成反應(Eq. 5, Angew. Chem. Int. Ed. 2019, 58, 15104)。盡管有了這些報道,催化不對稱構建該類骨架的策略仍然非常有限。所以,迫切需要發(fā)展新策略,以實現(xiàn)基于3-芳基吲哚的軸手性骨架的設計與構建。
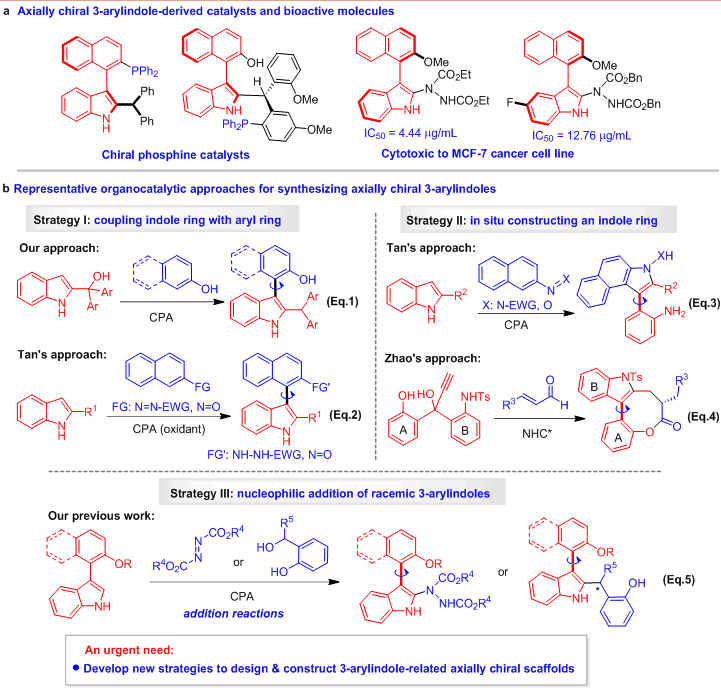
圖2 有機小分子催化不對稱構建軸手性3-芳基吲哚骨架的研究概況
為了實現(xiàn)上述目標,石楓課題組基于對手性吲哚化學的理解(For a summary: Acc. Chem. Res. 2020, 53, 425),提出了基于3-芳基吲哚平臺分子參與的催化不對稱(2 + n)環(huán)化反應的策略,用于構建新型的軸手性3-芳基吲哚稠環(huán)骨架。在該策略中,吲哚的C2-位和NH基團作為親核位點,使3-芳基吲哚平臺分子作為1,2-雙親核試劑,在手性布朗斯特酸(B*-H)催化下與合適的雙親電試劑(E1-E2)發(fā)生(2 + n)環(huán)化反應(圖3a)。由于新形成的環(huán)系與OH基團之間的空間位阻,可以實現(xiàn)新型軸手性3-芳基吲哚稠環(huán)骨架的構建。該策略的獨特優(yōu)勢是:能夠形成新的環(huán)系、構建新型的軸手性骨架、產生多重手性元素。然而,采用該策略仍然需要克服一些挑戰(zhàn),主要包括:(1)尋找到合適的能夠被B*-H活化的雙親電試劑,以實現(xiàn)其與3-芳基吲哚的(2 + n)環(huán)化反應;(2)由于兩種反應底物中均存在兩個競爭的反應位點,所以需要控制好(2 + n)環(huán)化反應的區(qū)域選擇性和對映選擇性;(3)當采用外消旋的雙親電試劑參與(2 + n)環(huán)化反應時,需要同時控制好所構建骨架的軸手性和中心手性。
為了解決這些挑戰(zhàn)性問題,作者設想:對羥基苯基或對烷氧基苯基取代的炔丙醇或許可以作為一類合適的雙親電試劑,參與所設計的(2 + n)環(huán)化反應。該設想是基于香港科技大學孫建偉課題組的首次報道(Nat. Commun. 2017, 8, 567):該類炔丙醇在B*-H催化下,可以脫水生成對亞甲基苯醌中間體(p-QMs),從而與親核試劑發(fā)生1,8-加成反應生成軸手性聯(lián)烯(圖3b)。
所以,在該工作的設計中(圖3c),作者設想此類炔丙醇可以作為合適的1,3-雙親電試劑,在CPA催化下與3-芳基吲哚發(fā)生對映選擇性的(2 + 3)環(huán)化反應,從而構建新型的軸手性芳基吡咯并吲哚骨架。該反應將通過動態(tài)動力學拆分(DKR),先發(fā)生1,8-加成反應,產生手性聯(lián)烯中間體,再經歷質子化和分子內環(huán)化過程,生成軸手性芳基吡咯并吲哚。在反應過程中,CPA可以依次活化3-芳基吲哚的OH和NH基團,從而控制(2 + 3)環(huán)化反應的區(qū)域選擇性。此外,CPA與底物和中間體之間的相互作用,將促進DKR過程和立體選擇性的分子內環(huán)化,從而控制所構建的芳基吡咯并吲哚骨架的軸手性和中心手性。因此,所設計的(2 + 3)環(huán)化反應將為構建基于吲哚的新型軸手性骨架提供新策略,并且可以同時控制多重手性元素。
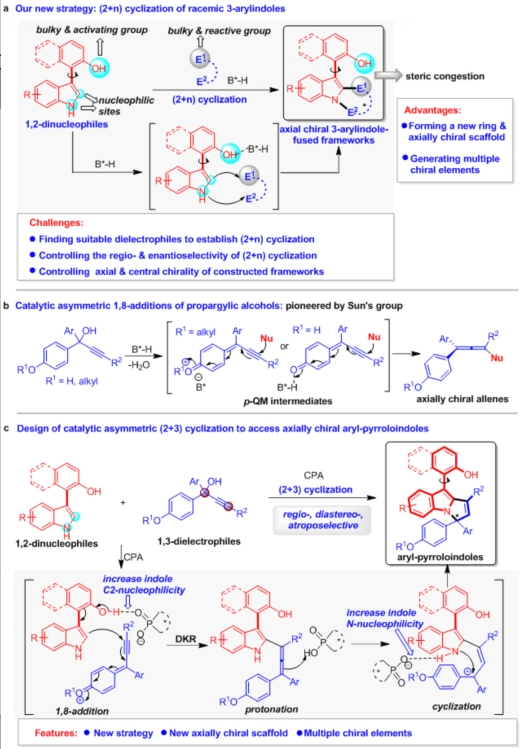
圖3 設計構建新型軸手性3-芳基吲哚稠環(huán)骨架的策略
基于上述構建策略的設計,石楓課題組成功地實現(xiàn)了新型軸手性芳基吡咯并吲哚骨架的催化不對稱構建,高收率(up to 97% yield)、高對映選擇性(up to 98% ee)地獲得了結構多樣的軸手性芳基吡咯并吲哚化合物3(圖4)。
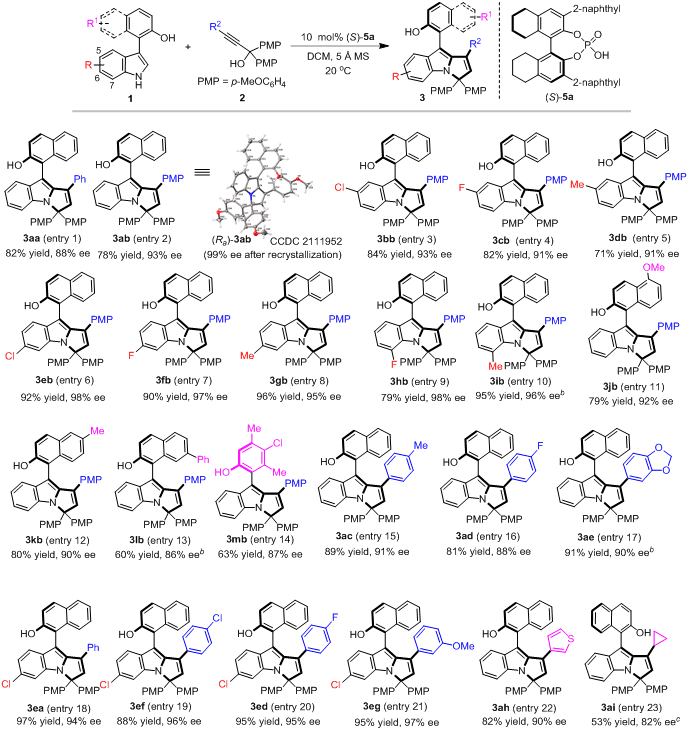
圖4 軸手性芳基吡咯并吲哚骨架的構建
此外,該課題組還進一步探索了兼具軸手性和中心手性的芳基吡咯并吲哚骨架的催化不對稱構建。該類骨架由于具有多重手性元素,所以其立體選擇性控制更具挑戰(zhàn)性。作者通過一系列嘗試,最終以中等到優(yōu)秀的收率(56-98% yield)、優(yōu)秀的非對映選擇性和對映選擇性(up to >95:5 dr, 99% ee),獲得了一系列新型的兼具軸手性和中心手性的芳基吡咯并吲哚化合物7(圖5)。
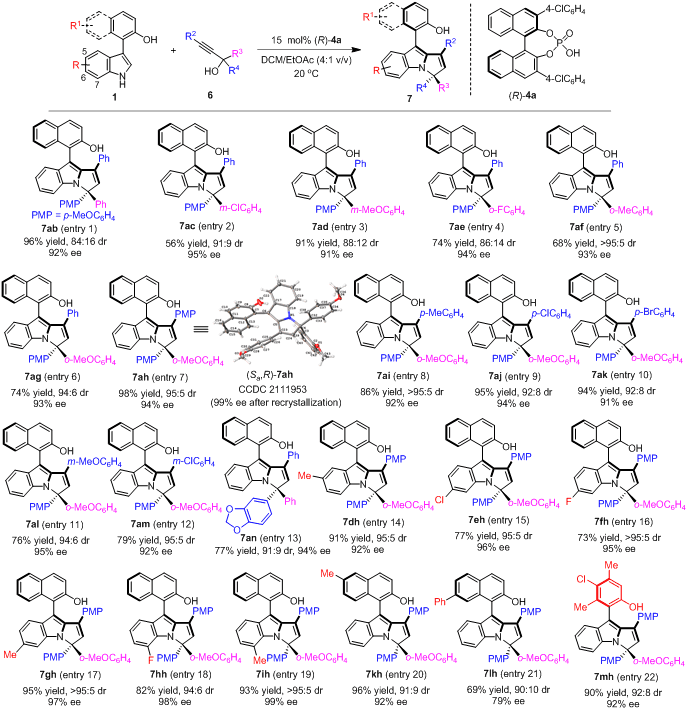
圖5 兼具軸手性和中心手性的芳基吡咯并吲哚骨架的構建
為了探究該類新型軸手性芳基吡咯并吲哚骨架的潛在應用價值,作者對產物進行了合成轉化以及嘗試其在不對稱催化中的應用(圖6)。首先,1 mmol規(guī)模的實驗結果,說明了該催化不對稱(2 + 3)環(huán)化反應可用于放大量合成(圖6a)。其次,軸手性芳基吡咯并吲哚化合物通過衍生化,可以轉化為新型的單膦配體(圖6b)。更重要的是,該類軸手性單膦配體成功地應用于苯乙烯的催化不對稱硅氫化反應和Pd(II)催化的不對稱烯丙基烷基化反應(圖6c)。這些結果表明,該類新型的軸手性芳基吡咯并吲哚骨架可用于開發(fā)新型的手性配體和催化劑,有望在不對稱催化中發(fā)現(xiàn)更多的應用。
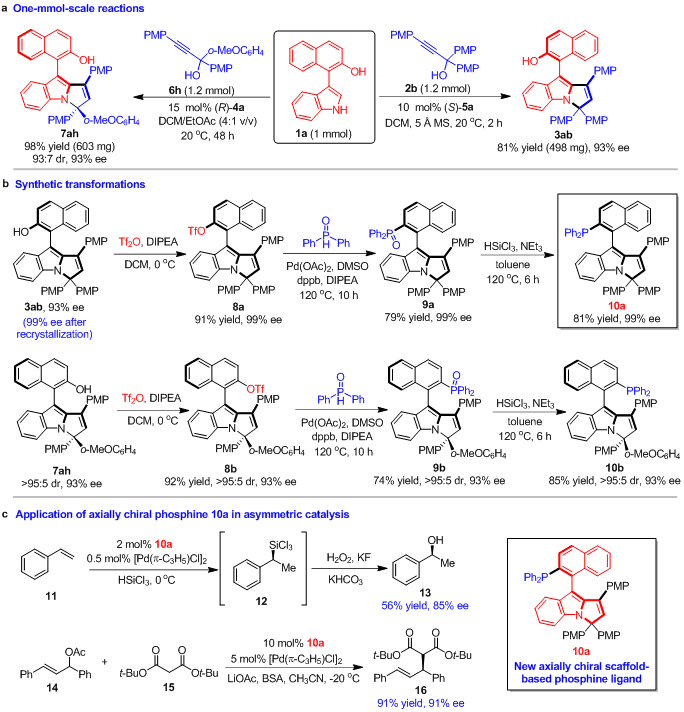
圖6 產物的合成轉化及其在不對稱催化中的應用
為了深化對該類新型軸手性骨架和催化不對稱(2 + 3)環(huán)化反應的理解,作者探究了該類骨架的穩(wěn)定性,并進行了控制實驗(圖7)。實驗顯示,該類軸手性骨架具有高的穩(wěn)定性和旋轉能壘(圖7a)。此外,作者還研究了3-芳基吲哚1中OH基團以及炔丙醇2和6中OMe基團的作用(圖7b)。控制實驗的結果表明:(1)3-芳基吲哚1中的OH基團很可能與CPA形成了氫鍵,從而在控制反應的立體選擇性方面起著至關重要作用;(2)炔丙醇2和6中的OMe基團有助于其生成p-QM陽離子中間體,并與CPA形成離子對,從而在控制反應性和對映選擇性方面發(fā)揮著重要作用。
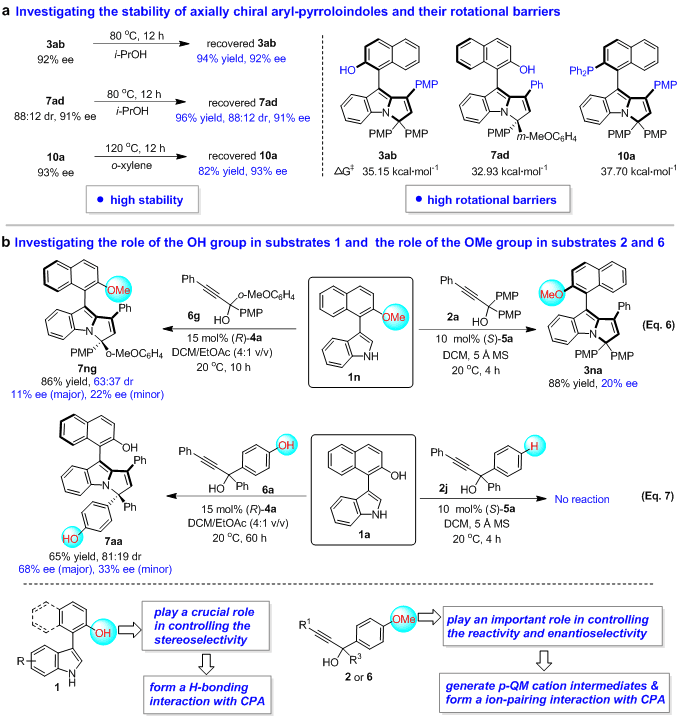
圖7 探究軸手性芳基吡咯并吲哚骨架的穩(wěn)定性及控制實驗
為了深入理解這一反應,石楓課題組與湖南科技大學焦銀春課題組進行合作,對合成產物(Ra)-3ab的可能反應路徑和活化模式進行了理論計算(圖8)。首先,計算出底物1a的旋轉能壘為19.79 kcal mol-1(圖8a),遠低于可分離出阻旋異構體所需的24 kcal mol-1,這說明(Ra)-1a在室溫下很容易轉化為(Sa)-1a,從而有利于后續(xù)的DKR過程。同時,計算表明,炔丙醇2b在CPA (S)-5a的催化下容易脫水,經過過渡態(tài)TS-1生成p-QM陽離子中間體INT-1(圖8b)。隨后,作者詳細計算了可能的反應路徑和活化模式(圖8c),并且歸納了反應過程的自由能壘圖(圖8d)。值得注意的是,在反應的關鍵過渡態(tài)TS-2中,催化劑(S)-5a不僅與底物(Sa)-1a的OH基團和CH基團同時形成兩個氫鍵,而且與p-QM陽離子產生離子對作用,從而促進它們之間的1,8-加成反應。然而,在TS-2’中,由于底物(Ra)-1a的OH基團距離催化劑(S)-5a較遠,使(S)-5a只能與(Ra)-1a的CH基團形成氫鍵,并不能與(Ra)-1a的OH基團形成氫鍵,導致底物(Ra)-1a比(Sa)-1a難以進行1,8-加成反應。所以,TS-2與TS-2’中底物與催化劑之間的不同活化模式導致了它們能壘的差異(3.05 kcal mol-1),從而解釋了反應的DKR過程和高對映選擇性生成(Ra)-3ab的原因。
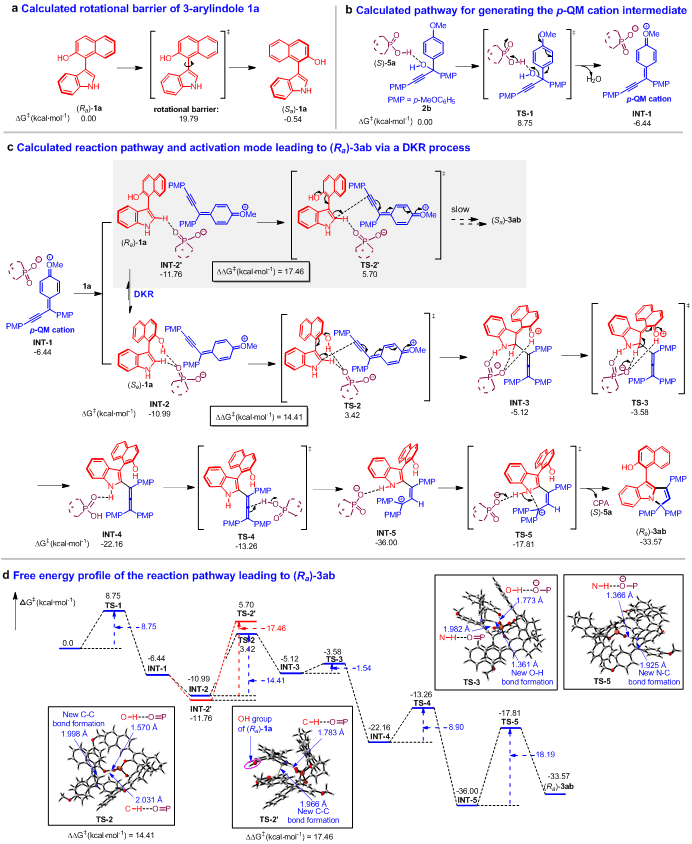
圖8 通過理論計算探究可能的反應路徑和活化模式
綜上所述,石楓課題組通過有機催化不對稱(2 + 3)環(huán)化反應的策略,實現(xiàn)了新型軸手性芳基吡咯并吲哚骨架的設計及對映選擇性構建。該策略通過手性磷酸催化下3-芳基吲哚平臺分子的動態(tài)動力學拆分,高收率(up to 98% yield)、高立體選擇性(up to >95:5 dr, 99% ee)地獲得了兼具軸手性和中心手性的芳基吡咯并吲哚化合物。更重要的是,這種新型的軸手性骨架具有很高的穩(wěn)定性,可以衍生為新型的膦配體,應用于鈀催化的不對稱反應。此外,通過理論計算,深化了對反應機理和活化模式的理解。該工作不僅為軸手性家族增添了芳基吡咯并吲哚這一新成員,而且為設計和構建基于3-芳基吲哚的軸手性骨架提供了新策略。該類軸手性骨架有望被開發(fā)為新型手性配體或催化劑,在不對稱催化中得到更多的應用。
上述研究成果作為特邀稿件發(fā)表在Fundamental Research, 2022, DOI: 10.1016/j.fmre.2022.01.002。《Fundamental Research》是由國家自然科學基金委員會主管、主辦的英文學術期刊,于2021年1月創(chuàng)刊(CN 10-1722/N)。期刊立足展示國家自然科學基金資助的代表性成果,充分反映國內外基礎研究前沿與動態(tài),促進國際學術交流,提升中國基礎研究在國際科學界的顯示度和影響力。作為反映世界、特別是中國基礎研究最高水平的綜合性英文學術期刊,將為科學家打造一個高端的基礎研究國際交流平臺。期刊內容涵蓋數(shù)學與物理、化學與化工、生命、地球、工程與材料、信息、管理、健康與醫(yī)學、交叉科學等九大科學領域。
我院碩士研究生伍平為第一作者,實驗部分由我院石楓教授和譚偉副教授共同指導完成,理論計算部分由石楓教授和湖南科技大學焦銀春副教授共同指導完成。該項工作主要得到了國家自然科學基金和江蘇省自然科學基金的資助。
石楓課題組主頁:https://www.x-mol.com/groups/Shi_Feng
部分作者簡介
石楓 教授

石楓,江蘇師范大學化學與材料科學學院教授。1998年和2004年于江蘇師范大學分別獲得學士和碩士學位,2010年至2013年攻讀了蘇州大學與中國科學技術大學聯(lián)合培養(yǎng)的博士學位,2012年至2013年赴新加坡南洋理工大學從事訪問學者工作。先后獲得國家杰出青年科學基金(2021)、江蘇省杰出青年基金(2016)、江蘇省“六大人才高峰”高層次人才、江蘇省“333高層次人才”中青年學術技術帶頭人、江蘇省高校“青藍工程”中青年學術帶頭人等人才項目。主要從事催化不對稱合成手性雜環(huán)分子的研究,聚焦手性吲哚化學這一研究領域,為構建結構復雜多樣的手性生物活性雜環(huán)骨架(尤其手性吲哚化合物)提供了高效、高選擇性的方法。以通訊作者在Acc. Chem. Res., Fund. Res., J. Am. Chem. Soc., Angew. Chem. Int. Ed., Chin. J. Chem., ACS Catal., Org. Lett., Chem. Commun., Adv. Synth. Catal., J. Org. Chem. 等業(yè)界公認的國際重要科技期刊發(fā)表學術論文120余篇,入選Elsevier 2020高被引學者;榮獲江蘇省第二屆“十佳研究生導師”提名獎、江蘇省研究生教育改革成果獎優(yōu)秀獎、江蘇省科學技術二等獎、教育部自然科學二等獎、Thieme Chemistry Journal Award、Asian Core Program Lectureship Award、新和成《中國化學》創(chuàng)新獎等獎項。擔任有機化學、Chem. Synth. 青年編委, Org. Chem. Front., J. Org. Chem. 和Eur. J. Org. Chem. 國際編委。
譚偉 副教授

譚偉,江蘇師范大學化學與材料科學學院副教授。2015年于江蘇師范大學獲得碩士學位(導師:石楓教授),2019年于華東師范大學獲得博士學位(導師:姜雪峰教授),同年被引進到江蘇師范大學。主要從事軸手性五元雜環(huán)骨架的催化不對稱構建、生物活性手性雜環(huán)分子的催化不對稱合成的研究,近年來以通訊作者或第一作者在Fund. Res., J. Am. Chem. Soc., Chin. J. Chem., Org. Lett., Chem. Commun., Chem. Eur. J. 等業(yè)界公認的國際重要科技期刊發(fā)表學術論文10余篇。
石楓課題組簡介:

石楓課題組成立于2013年,課題組指導教師目前包括石楓教授(中間)、張宇辰副教授(左一)、譚偉副教授(右一),課題組學生包括碩士研究生和本科生。課題組對學生的培養(yǎng)理念是“英雄不論出身”,努力把每一個學生都培養(yǎng)成優(yōu)秀的學生、同齡人中的佼佼者,不放棄任何一個學生。課題組培養(yǎng)的碩士研究生中,有13人獲得研究生國家獎學金,有16人以第一作者在業(yè)界公認的國際重要科技期刊Fund. Res., J. Am. Chem. Soc., Angew. Chem. Int. Ed., Chin. J. Chem. 發(fā)表高質量學術論文18篇,1人獲得“江蘇省三好學生”榮譽稱號,有90%以上通過“申請-考核制”進入名校繼續(xù)攻讀博士學位。
石楓課題組長期致力于催化不對稱構建生物活性手性雜環(huán)骨架,尤其是含有吲哚母核的手性雜環(huán)骨架。通過設計和開發(fā)新型的吲哚平臺分子及其參與的催化不對稱反應,為構建手性吲哚類雜環(huán)骨架提供了高效、高立體選擇性的方法,促進了手性吲哚化學的發(fā)展(工作總結:Acc. Chem. Res. 2020, 53, 425)。課題組不僅在催化不對稱構建中心手性吲哚類雜環(huán)骨架領域取得了標志性成果(代表性工作:Angew. Chem. Int. Ed. 2014, 53, 13912; Angew. Chem. Int. Ed. 2015, 54, 5460; ACS Catal. 2017, 7, 6984; Angew. Chem. Int. Ed. 2018, 57, 5398; Angew. Chem. Int. Ed. 2019, 58, 8703; Angew. Chem. Int. Ed. 2021, 60, 2355),而且在催化不對稱構建軸手性吲哚骨架及其應用領域取得了創(chuàng)新性成果(代表性工作:Angew. Chem. Int. Ed. 2017, 56, 116; Angew. Chem. Int. Ed. 2019, 58, 8703; Angew. Chem. Int. Ed. 2019, 58, 15104; Chin. J. Chem. 2020, 38, 543; J. Am. Chem. Soc. 2020, 142, 15686; Chin. J. Chem. 2021, 39, 2163; Angew. Chem. Int. Ed. 2022, 10.1002/anie.202112226; Angew. Chem. Int. Ed. 2022, 10.1002/anie.202116829; Fund. Res. 2022, 10.1016/j.fmre.2022.01.002),促進了該領域的發(fā)展(綜述:Chem. Eur. J. 2020, 26, 15779)。
聲明:化學加刊發(fā)或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn