

漸入佳境的背后,是亞盛醫藥過去十多年前埋下的創新種子飽經風霜后開花結果的前序,這種歲月鑄就的品質類似大家耳熟能詳的“毛竹生長故事”——毛竹需要用5年時間來扎根,才能在第6年開始瘋狂生長。按照成功開發1款新藥平均需要10年的理論,亞盛醫藥花了10年的時間來扎根,接下來還有哪些值得期待?醫藥魔方就此專訪了亞盛醫藥董事長兼CEO楊大俊博士。

楊大俊博士
孤兒藥市場“不孤”,堅持去做就有收獲
在新冠疫情的挑戰下,亞盛醫藥依舊取得眾多里程碑式進展:遞交了在中國的首個新藥上市申請(HQP1351),并被納入優先審評;HQP1351第三次入選ASH年會口頭報告,數據令人振奮;一年內獲得FDA授予的9項孤兒藥資格以及1項審評快速通道資格;細胞凋亡管線重要品種Bcl-2抑制劑APG-2575獲得初步臨床概念驗證數據;首次在歐洲開展臨床試驗等;與阿斯利康血液研發卓越中心、默沙東分別達成全球臨床合作。
其中值得關注的是,亞盛醫藥2020年囊獲的孤兒藥資格數量為單年全球第一,并且僅次于2019年的冠軍安進(12個),與2018年的狀元阿斯利康(9個)齊平;同時也創下了中國藥企歷來之最。
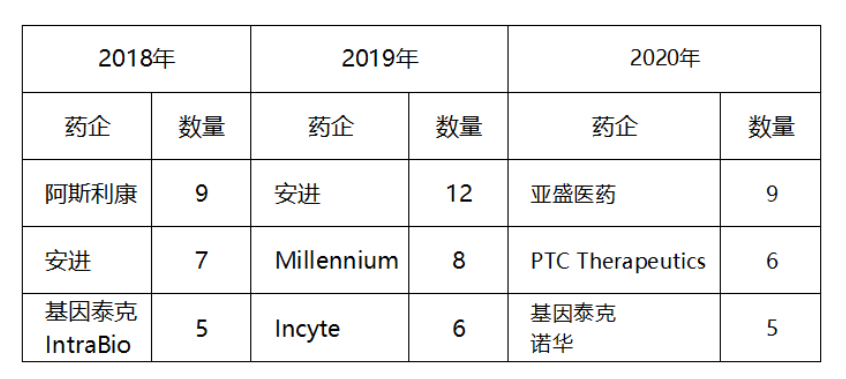
近3年收獲FDA孤兒藥資格數量Top3藥企
根據美國法規,獲得孤兒藥資格認定的產品在美國的后續研發及商業化開展將享受多種政策支持,包括臨床試驗費用稅收減免、免除NDA費用、獲得研發資助以及上市后可獲得美國市場7年獨占權,甚至還可能獲得一張寶貴的優先審評券等等。
“大家可能會有問,你們報這么多孤兒藥干什么?市場前景也不一定可觀……”,楊大俊對來自投資者的挑釁并不避諱。“堅持是我們亞盛的重要標簽。就像我們一開始就定位做first in class,當時也沒人敢做。在10年前,這是最難走的一條路,也有質疑聲,但我們仍然堅持到了今天。”
“利用孤兒藥的政策紅利進行申報是我們效仿國際制藥巨頭,作為重要的注冊策略之一。相信國內會有越來越多企業會這么做,我們算是走在前面。”楊大俊坦言。
的確在國外,新分子實體找到一個合適的適應證去申請孤兒藥資格認定早已是一種常態。2020年FDA全年共批準了53個新藥,其中有31個品種被FDA授予孤兒藥資格,占所有獲批新藥的58%。
與此同時,孤兒藥也逐漸成為了中國創新藥開發的突破口,是中國創新藥走向國際的一個捷徑。根據醫藥魔方的梳理,2020年中國創新藥企業共拿下36項FDA孤兒藥資格認定(亞盛占有1/4),申報孤兒藥已成為國內創新藥企業尋求國際化的重要途徑之一。
那孤兒藥的未來前景一定會“孤單”嗎?答案顯然是否定的。孤兒藥市場不“孤”早已成為業內共識。孤兒藥不僅市場不孤,并且諸多獲得過孤兒藥稱號的藥物在上市后“一戰成名”,成為了超級重磅炸彈藥物。
比如是電影《我不是藥神》中提到的“格列寧”的原型格列衛(甲磺酸伊馬替尼片)。數據顯示:當年諾華在開發該藥物的時候,其首個適應證的患者人群還不到1萬名,是名副其實的孤兒藥,但是這款藥物借力孤兒藥“特權”快速開發快速獲批,上市后年銷售額最高逼近50億美元。
還有近年來獲批上市的PD-1藥物,比如Keytruda和Opdivo在未上市時也是通過孤兒藥策略進行開發,進入市場后亦是快速放量,尤其是Keytruda,已經被分析師譽為下一個取代Humira的“藥王”,年銷售額有望升至200億美元。
科學創新不是一蹴而就的,需要時間的積累。對于知識密集型的創新藥企業來言,更是需要在日趨激烈的市場競爭中找到一個生存點。認識到孤兒藥策略的重要性可能并不僅僅有亞盛醫藥,亞盛醫藥在此領域的成績為何能走在國內一批藥企中遙遙領先?
“可能是我們對政策的理解更透徹。美國對孤兒藥的定義目前是針對患病人數少于20萬人的疾病。而某些疾病受外部環境的影響,每年發病人數是在不斷攀升。”楊大俊解釋道。
在別人還在猶豫時提前下手,堅信“堅持就有收獲”的樸素價值觀,使得亞盛醫藥在孤兒藥競技中成為全球制藥企業的“一枝獨秀”。截至目前,亞盛醫藥共有4個在研新藥獲得9項FDA孤兒藥資格認證,這或是對該企業當初的決定和努力最實在的回報。
堅持做對的事,未來5年值得期待
亞盛醫藥基于蛋白-蛋白相互作用靶點建立了極具國際競爭力的產品管線。據楊大俊在JP摩根大會上的介紹,目前亞盛醫藥已獲得臨床批件33項,正在全球層面開展40多項臨床研究。這些產品最終將幫助腫瘤尤其是血液瘤患者延緩生命。

亞盛醫藥產品管線
在楊大俊看來,腫瘤患者的生命非常寶貴,藥企應該爭分奪秒的研發,盡快將產品推向市場。除了前文提到的通過孤兒藥策略加快研發進度,亞盛醫藥的另一招便是選擇具有同樣理念的團隊同行。
2020年6月15日,亞盛醫藥向CDE遞交了格列衛耐藥新藥HQP1351的NDA,用于治療伴有T315I突變的CML慢性期和加速期患者,這比預期提前了3個多月。
在突如其來的新冠疫情影響下,亞盛醫藥算是克服了種種困難,做到疫情防控和企業發展兩不誤,其背后的艱辛并不為外界所知。為了公司的諸多項目能夠順利開展,楊大俊曾冒著生命危險在多個國家的領空穿行。
在飛機上度過了51個小時、并隔離14天,做了6次核酸檢測后,終于出現在團隊面前的楊大俊看到HQP1351的所有資料超出他預期提前向國家藥監局申報時,總算舒了口氣。他不禁感慨,如果沒有團隊的熱情、奉獻和爭分奪秒的付出,HQP1351的申報肯定不會如此順利。
“按照計劃,HQP1351的關鍵臨床試驗得在去年3月底給到統計師基礎數據。去年這個時候疫情開始爆發,并且越來越嚴重,很多第三方物流暫停了相關服務,”楊大俊回憶道,“當時我們醫學部十分著急,患者也很焦灼,他們出不了城且沒有藥可用。后來我們同事想盡各種辦法,終于將藥品送達患者手中。”
亞盛醫藥是國際上最早進入細胞凋亡與自噬雙通道調節新靶點小分子抑制劑研發領域者之一。由于細胞凋亡靶點小分子抑制劑的成藥前景高度不確定性及研發工作極困難性,讓不少藥企望而卻步。
“亞盛不做fast follow,所有在研項目均為新化合物結構,我們始終堅持定位全球創新與瞄準全球市場,也堅信創新和國際化是生物醫藥企業乃至行業做大做強的根本。”楊大俊眼神中充滿無所畏懼。
為加速產品開發,亞盛醫藥正在全球攬才,隨著越來越多高級別人才的加盟,讓楊大俊可以有更多的時間思考更前瞻的戰略。在人才引進方面,楊大俊認為,“公司所吸引的人,一定也是看好公司未來的人,不僅僅是投資者,也包括愿意下場一起踢球的參與者。”
亞盛醫藥早期堅持讓創始人控股并堅持做原創的理念受到越來越多投資者的認可,二級市場也逐漸認識到這家企業的內核所在。“一個企業的成功與否,不能只看過去和現在,要著眼于未來。未來5~10年,亞盛醫藥的產品將陸續進入收獲期。”楊大俊對此頗有信心。
楊大俊是時代的幸運兒,上世紀70年代恢復高考后考入中山醫科大學(現中山大學),求學期間他創辦了著名醫學期刊《家庭醫生》。80年代赴美留學、獲得博士學位后先后在科研院所工作及創辦企業。2008年金融危機后回到國內創辦亞盛醫藥。
“亞盛醫藥是我全身心的第三次創業。雖然這一路走得有些艱辛,但我覺得很值得。因為創業者最幸運的莫過于「腦心合一」,腦袋決定了你擅長什么,內心告訴你喜歡什么。”楊大俊坦言,“做創新藥,進行全球開發,正好既是我擅長,又是我喜歡的。讓我累并快樂著。因為選擇,所以堅持!”
后記
聆聽楊大俊講述在疫情期間漂洋過海之后又被隔離辦公的窘迫,手舞足蹈的描述中流露出的滿腔熱忱,讓筆者的思緒仿佛回到了八十年代,那個白衣翩翩的少年踩著腳踏車,將親手創辦的雜志送到讀者手中的興奮與喜悅。三十余載的光陰似水流年,但少年對事業的熱忱有增無減。「出走半生,歸來仍是少年;遍歷百折,仍覺做藥值得。」這可能是對楊大俊堅持原創不懼艱難最適合的寫照。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn