

如下圖所示,Hecker提出tigliane骨架可能是ingenane、daphnane和rhamnofolane的生物合成前體,從生物合成上講,tigliane可以由大量易得的香葉基香葉基焦磷酸(GGPP)通過casbene和lathyrane的形成而初步實現,因此,研究tigliane、ingenane、daphnane和rhamnofolane相互之間的化學轉化,探索其生物合成機理具有重要的意義;從結構上看,這些天然的二萜類化合物都包含一個類似的三環骨架,骨架上嵌有多個立體手性中心,如圖所示,天然產物crotophorbolone具有一個trans, trans-5/7/6三環環系,并含有六個相鄰的立體手性中心,其中包括兩個季碳中心。2015年,Inoue課題組報道了crotophorbolone的首例全合成(Angew. Chem. Int. Ed., 2015, 54, 14457)。
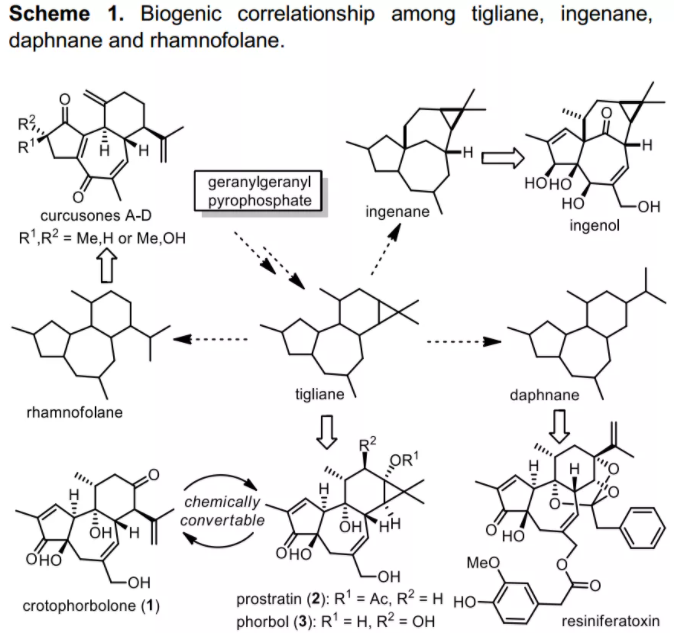
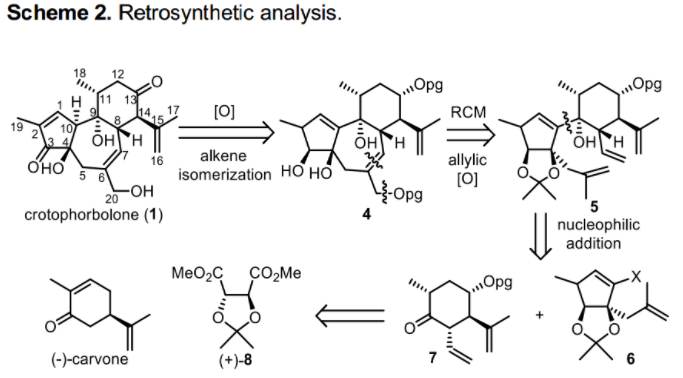
四川大學劉波課題組近期發表了二萜類天然產物crotophorbolone的全合成工作(Chem. Sci., DOI: 10.1039/D0SC02829K)。逆合成分析如圖所示,設想crotophorbolone (1)可以由化合物4通過后期氧化羥基以及烯烴異構化得到,具有天然產物環系骨架的三環化合物4可以通過二環化合物5經烯烴復分解反應構建7元環并氧化烯丙位得到。二環化合物5中的C9-C10可由片段6與7經親核加成連接,最后片段6與7可分別由商業可得8和香芹酮制備得到。
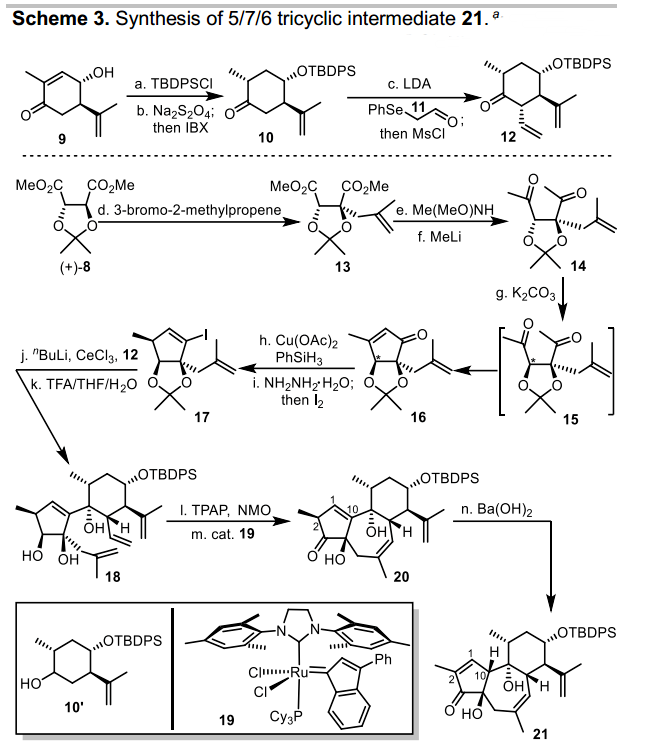
在具體合成路線中,首先需要分別合成片段化合物6與7,起始化合物9可由香芹酮在銅鋁合金氧化條件下獲得(Eur. J. Org. Chem., 2013, 2013, 8307),隨后二級羥基經TBDPS保護,還原烯酮結構再經IBX氧化,即可得到單一化合物10,接著與醛11在堿性條件下發生Aldol反應,得到二級羥基中間體,隨后經甲磺酰化并消除,得到六元環片段化合物12。另一五元環片段的構建由化合物8出發,經非對應選擇性的甲基烯丙基化得到烯烴化合物13,隨后雙甲酯經Weinreb酰胺化,甲基鋰親核進攻獲得雙酮化合物14。14在碳酸鉀條件下翻轉三級碳手性,并發生分子內Aldol縮合反應,得到熱力學穩定的cis 5/5雙環化合物16。在銅催化下,雙環化合物16與苯硅烷發生1,4-親核加成反應,隨后酮羰基與肼縮合形成腙,經碘化處理得到烯基碘化合物17。接著嘗試兩個片段的連接,化合物17先經鋰鹵交換,隨后對酮化合物12進行親和加成,并在酸性條件下脫除縮酮保護得到二環化合物18,然后氧化化合物18中的二級羥基,并經烯烴復分解反應完成5/7/6三環骨架的組裝。最后考慮通過烯烴異構構建trans-5/7環系,但經過大量實驗都未能實現,只得到了cis-5/7環系化合物21。
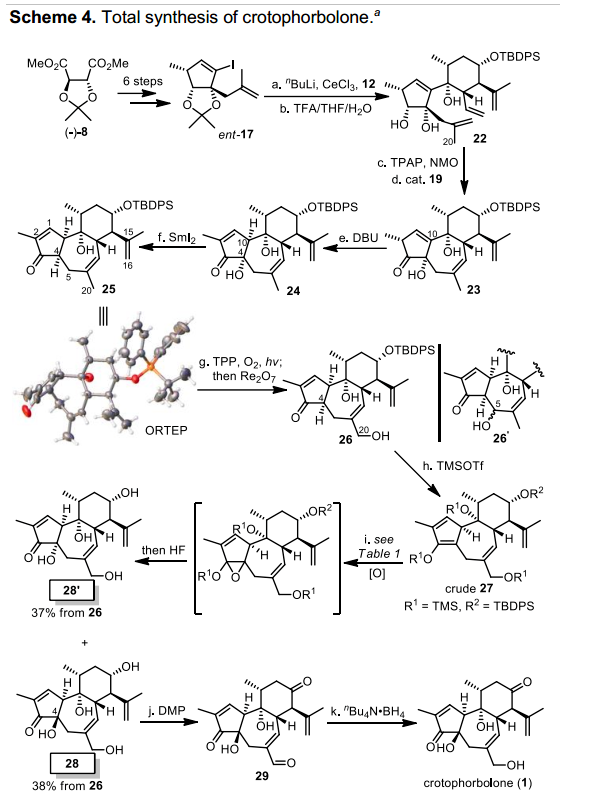
為了可以正確引入C10位手性中心,劉波課題組決定從最初階段反轉手性,采用(-)-8作為起始化合物,隨后經相同操作得到化合物17的對映異構體,接著可順利完成三環化合物23的構建,然后在DBU堿性條件下發生雙鍵遷移,順利引入C10位手性中心得到化合物24。化合物24中C4位α-OH在二碘化釤條件下脫除,隨后對烯丙位氧化并經TMS保護得到化合物27,接著對雙鍵環氧化,并脫除硅保護基,成功引入C4位β-OH,最后采用Dess-Martin氧化一級、二級羥基,隨后還原醛基,完成天然產物crotophorbolone的全合成。
總結:劉波教授課題組通過高效簡潔的匯聚式合成路線完成了crotophorbolone的全合成。合成路線包含以下亮點:(1)采用匯聚式策略分別構建五元環與六元環片段;(2)通過親核加成反應完成兩片段連接;(3)利用烯烴復分解反應完成7元環構建;(4)立體選擇性引入C20和C4位手性羥基。
參考資料
[1]微信公眾號國內有機全合成資訊(ID:OrgChemNews),「往期」四川大學劉波課題組完成天然產物Crotophorbolone的全合成
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn