1、不對(duì)稱合成科研團(tuán)隊(duì)在催化不對(duì)稱自由基-偶極交叉反應(yīng)方面取得重要進(jìn)展
近日,四川大學(xué)馮小明教授課題組結(jié)合手性雙氮氧(L-PiPr3)-Ni(II)配合物催化劑和Ag2O,成功實(shí)現(xiàn)了茚酮甲酰胺、酯與富電子烯烴的催化不對(duì)稱自由基-偶極交叉反應(yīng)。羰基a位對(duì)醛、酮的不對(duì)稱親核加成反應(yīng)在過去幾十年被廣泛研究。文獻(xiàn)報(bào)道通過單電子氧化可以實(shí)現(xiàn)羰基a位的極性反轉(zhuǎn),生成親電型的a-碳自由基,這極大豐富了羰基化學(xué)在有機(jī)合成中的應(yīng)用。然而,由于自由基的反應(yīng)活性高,副反應(yīng)多,背景反應(yīng)強(qiáng)等特點(diǎn),實(shí)現(xiàn)高對(duì)映選擇性不對(duì)稱催化反應(yīng)仍具有很大挑戰(zhàn)。盡管目前已經(jīng)發(fā)展了一些創(chuàng)造性的催化模式和策略來促進(jìn)羰基a-碳自由基參與催化不對(duì)稱反應(yīng),但存在催化劑的用量高,催化模式單一,底物的普適性不好,反應(yīng)結(jié)果差等缺點(diǎn)。在本文中,他們利用課題組發(fā)展的手性[Ni-L-PiPr3]*配合物作為手性Lewis酸催化劑,高收率、高對(duì)映選擇性的實(shí)現(xiàn)了不對(duì)稱自由基-偶極交叉反應(yīng)。各類烯烴和茚酮甲酰胺經(jīng)歷自由基加成、環(huán)化反應(yīng)得到一系列螺環(huán)亞胺內(nèi)脂以及螺環(huán)內(nèi)脂類化合物。同時(shí),根據(jù)所使用的富電子烯烴的不同,可以利用同一催化體系得到手性烯烴、醛、酮、醇四種不同類型的產(chǎn)物。在機(jī)理研究上,利用TEMPO捕獲到了自由基中間體,并且通過自由基鐘與EPR實(shí)驗(yàn)證明了自由基機(jī)理的合理性。
手性雙氮氧-Ni(II)配合物催化的不對(duì)稱自由基-偶極交叉反應(yīng)
以上研究結(jié)果以論文形式發(fā)表在國際期刊Angewandte Chemie International Edition上,論文題目為“Enantioselective Radical-Polar Crossover Reactions of Indanonecarboxamides with Alkenes”。四川大學(xué)博士張皙穎為本論文的第一作者,四川大學(xué)為本文的第一作者單位和通訊作者單位。該項(xiàng)研究工作得到了國家自然科學(xué)基金的經(jīng)費(fèi)支持。原文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/anie.201914151
2、游勁松教授團(tuán)隊(duì)在基于高度扭曲的七元環(huán)二酰亞胺聚集誘導(dǎo)延遲熒光材料構(gòu)建高效非摻雜OLED器件方面取得重要進(jìn)展
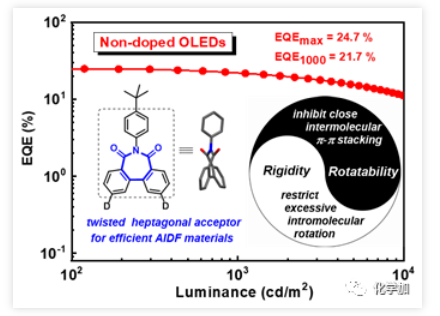
四川大學(xué)游勁松團(tuán)隊(duì)最近在非摻雜OLED器件中取得了突破性進(jìn)展,發(fā)展了一種基于扭曲七元環(huán)二酰亞胺受體的聚集誘導(dǎo)延遲熒光材料(AIDF),實(shí)現(xiàn)了最優(yōu)性能的非摻雜OLED器件。OLED顯示技術(shù)具有亮度高、能耗低、響應(yīng)快、可柔性化等諸多優(yōu)異的性質(zhì),已逐漸替代液晶顯示(LCD),成為下一代的主流平板顯示技術(shù)。作為第三代OLED顯示技術(shù)的熱活化延遲熒光(TADF)材料,因其100%的激子利用率,且不含貴金屬,在OLED中具有非常廣闊的應(yīng)用前景。迄今為止,基于TADF發(fā)光材料的摻雜OLED器件,其外量子效率已經(jīng)可以和磷光OLED相媲美,但是由于嚴(yán)重的聚集淬滅效應(yīng)(ACQ),高性能的非摻雜OLED器件十分難以實(shí)現(xiàn)。
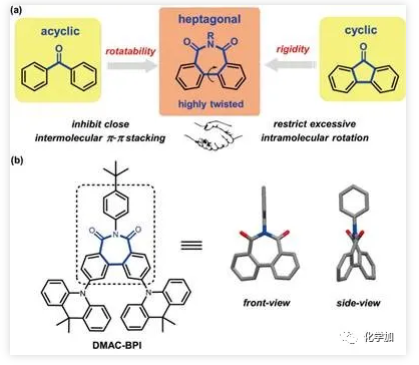
七元環(huán)二酰亞胺類AIDF分子的設(shè)計(jì)策略
游勁松教授團(tuán)隊(duì)一直致力于碳?xì)滏I活化領(lǐng)域的研究,發(fā)展了“電子差異原則”和“螯合導(dǎo)向作用構(gòu)筑稠雜環(huán)策略”,該策略為構(gòu)筑聯(lián)雜芳基骨架以及稠雜環(huán)提供了高效高選擇性的合成方法,為有機(jī)功能材料分子的高效合成提供了重要途徑。在該項(xiàng)研究中,作者通過釕催化的4-溴苯甲酸氧化自偶聯(lián)反應(yīng),構(gòu)筑了一種新型七元環(huán)二酰亞胺(BPI)受體,其不僅可以保持非環(huán)結(jié)構(gòu)的柔性,抑制分子間緊密堆積,減弱ACQ效應(yīng);又可以維持環(huán)狀結(jié)構(gòu)的剛性,限制分子的過度旋轉(zhuǎn),減小非輻射躍遷。作者以BPI為受體,以9,10-二氫-9,9-二甲基吖啶(DMAC)作為給體,設(shè)計(jì)合成了一種新型AIDF材料,DMAC-BPI,其具有極小的?EST (0.02 eV)和極高的量子產(chǎn)率(95.8%)。將DMAC-BPI用作發(fā)光層,制備得到高性能綠光非摻雜OLED器件,器件結(jié)構(gòu)為ITO/TAPC (25 nm)/DMAC-BPI (35 nm)/TmPyPb (55 nm)/LiF/Al,其最大外量子效率為19.4%;進(jìn)一步利用TCTA作激子阻擋層,效率提高至24.7%,即使在1000 cd/m2的亮度下,效率可以維持21.7%,展現(xiàn)出非常小的效率滾降。因此,環(huán)狀結(jié)構(gòu)的剛性和七元環(huán)結(jié)構(gòu)的可旋轉(zhuǎn)性之間的微妙平衡使DMAC-BPI成為一類出色的AIDF發(fā)光材料,從而實(shí)現(xiàn)了目前非摻雜OLED的最優(yōu)性能。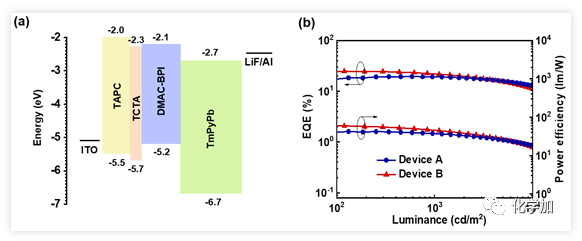
DMAC-BPI的非摻雜OLED器件結(jié)構(gòu)及效率隨亮度變化曲線
這一成果近期發(fā)表在Angewandte Chemie International Edition上,文章的第一作者是碩士研究生黃珍梅,通訊作者賓正楊副研究員,共同通訊作者游勁松教授。https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201915397Molecular Design of Non‐doped OLEDs Based on a Twisted Heptagonal Acceptor: A Delicate Balance between Rigidity and RotatabilityZhenmei Huang, Zhengyang Bin*, Rongchuan Su, Feng Yang, Jingbo Lan, Jingsong You*, Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.201915397.
3、余孝其課題組在基于聚集誘導(dǎo)發(fā)光的快速、超靈敏的細(xì)胞膜成像探針方面取得重要進(jìn)展
除了細(xì)胞屏障的基本功能外,細(xì)胞膜在許多細(xì)胞行為中發(fā)揮著非常重要的作用,如細(xì)胞遷移、細(xì)胞擴(kuò)散、神經(jīng)通訊、細(xì)胞運(yùn)輸和信號(hào)級(jí)聯(lián)等。此外,細(xì)胞膜異常對(duì)于細(xì)胞狀態(tài)和許多疾病而言是一個(gè)重要的標(biāo)志。因此,開發(fā)高選擇性、高靈敏度的檢測(cè)技術(shù)以準(zhǔn)確對(duì)細(xì)胞膜進(jìn)行可視化,尤其是活體可視化監(jiān)測(cè),對(duì)于探索與解決醫(yī)學(xué)早期診斷和研究生物學(xué)中的基本問題具有重要意義。近日,四川大學(xué)余孝其課題組與韓國高麗大學(xué)Jong Seung Kim教授課題組合作,設(shè)計(jì)了一種基于聚集誘導(dǎo)發(fā)光特性的熒光探針,用于生物體內(nèi)細(xì)胞膜快速、靈敏的免洗成像。探針以嘌呤骨架作為核心,裝配疏水的烷基鏈與帶有正電荷的季銨鹽,在水中保持良好溶解性的同時(shí)使無發(fā)光特性;探針通過疏水相互作用與靜電相互作用嵌入到細(xì)胞膜中,受到磷脂雙分子層的限制激活RIR過程,從而可以被激發(fā)出明亮的熒光。
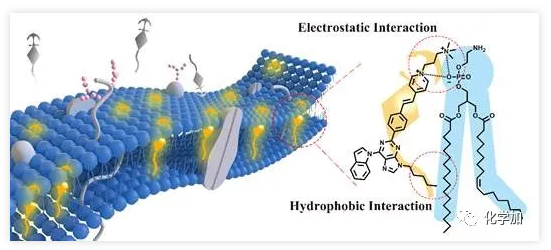
探針與細(xì)胞膜的標(biāo)記示意圖(左);探針與磷脂雙分子層的標(biāo)記策略(右)。
探針可以對(duì)多種細(xì)胞的細(xì)胞膜進(jìn)行快速的免洗成像,并且在保持高信噪比的情況下較長時(shí)間的標(biāo)記細(xì)胞膜(圖 2A);其優(yōu)良的細(xì)胞膜靶向性與生物安全性使其可以快速無損的標(biāo)記神經(jīng)元細(xì)胞的細(xì)胞膜(圖 2B-C)。此外,探針在多細(xì)胞腫瘤球中表現(xiàn)出良好的細(xì)胞間滲透性與細(xì)胞膜特異性,可在免洗的情況下較快地滲透120微米的細(xì)胞球,并標(biāo)記出其蜂窩狀的細(xì)胞膜結(jié)構(gòu)(圖 2D-F)。
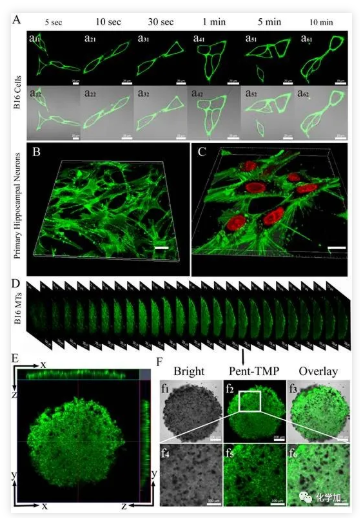
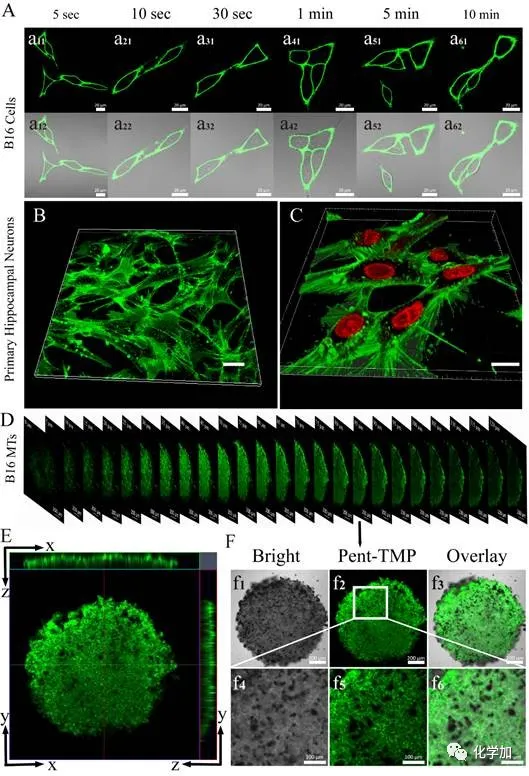
圖2. (A) B16細(xì)胞以探針孵育不同時(shí)間后未經(jīng)洗滌的熒光圖與明場疊加圖;原代海馬神經(jīng)元細(xì)胞以(B) 探針、(C) 探針和細(xì)胞核染料孵育1分鐘后的熒光圖;(D)多細(xì)胞腫瘤球0-120微米的Z軸層掃熒光圖;(E) 多細(xì)胞腫瘤球的x-y、x-z、y-z軸的熒光強(qiáng)度分布圖;(F) Z軸為60微米處的層切圖。比例尺:(A-C) 20微米,(D,f1-f3) 200微米,(f4-f6)100微米。除了體外染色,探針也可以對(duì)活體斑馬魚進(jìn)行染色。探針可以穿透常規(guī)染料無法滲入的斑馬魚表面的粘膜層,對(duì)其表皮細(xì)胞進(jìn)行染色(圖 3A-C)。此外,探針也可進(jìn)入斑馬魚眼組織,對(duì)其眼部結(jié)構(gòu)進(jìn)行部分成像(圖 3D)。
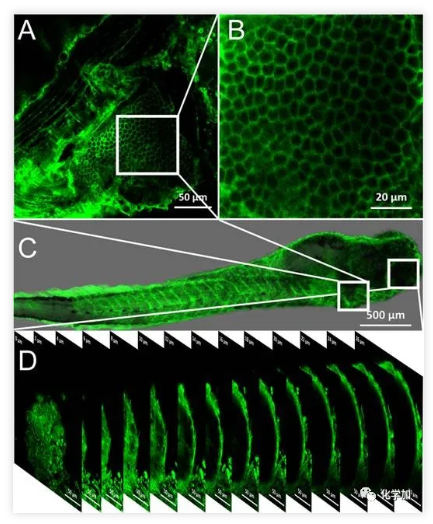
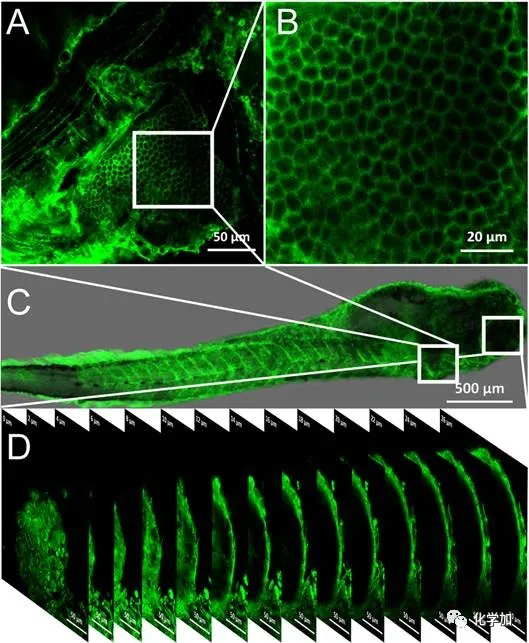 圖3. (A) 活體斑馬魚腮部的熒光圖;(B)活體斑馬魚腮部的局部放大圖;(C)活體斑馬魚整體染色的熒光圖;(D)活體斑馬魚眼部0-26微米的Z軸層掃熒光圖。比例尺:(A, D) 50微米,(B) 20微米,(C) 500微米。
圖3. (A) 活體斑馬魚腮部的熒光圖;(B)活體斑馬魚腮部的局部放大圖;(C)活體斑馬魚整體染色的熒光圖;(D)活體斑馬魚眼部0-26微米的Z軸層掃熒光圖。比例尺:(A, D) 50微米,(B) 20微米,(C) 500微米。
以上研究結(jié)果以論文形式發(fā)表在國際期刊《Angewandte Chemie International Edition》上,論文題目為“An AIE-Based Probe for Rapid and Ultrasensitive Imaging of Plasma Membranes in Biosystems”。論文的第一作者為四川大學(xué)化學(xué)學(xué)院博士生石磊,通訊作者為李坤教授、Jong Seung Kim教授和余孝其教授。近期,該課題組還深入研究了探針中疏水鏈的長度和電荷對(duì)其細(xì)胞膜靶向性能的影響(Bio-inspired assembly in a phospholipid bilayer: effective regulation of electrostatic and hydrophobic interactions for plasma membrane specific probes, Chem. Commun., 2020, 10.1039/d0cc00679c)。四川大學(xué)為本文的第一作者單位和通訊作者單位。該項(xiàng)研究工作得到了國家自然科學(xué)基金的經(jīng)費(fèi)支持。https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201909498https://pubs.rsc.org/en/content/articlelanding/2020/CC/D0CC00679C#!divAbstract











圖3. (A) 活體斑馬魚腮部的熒光圖;(B)活體斑馬魚腮部的局部放大圖;(C)活體斑馬魚整體染色的熒光圖;(D)活體斑馬魚眼部0-26微米的Z軸層掃熒光圖。比例尺:(A, D) 50微米,(B) 20微米,(C) 500微米。