

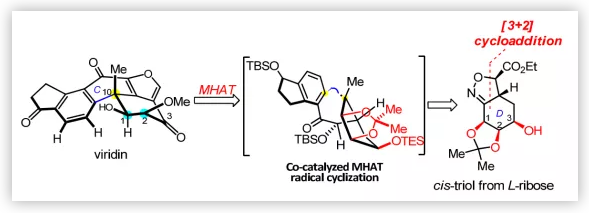
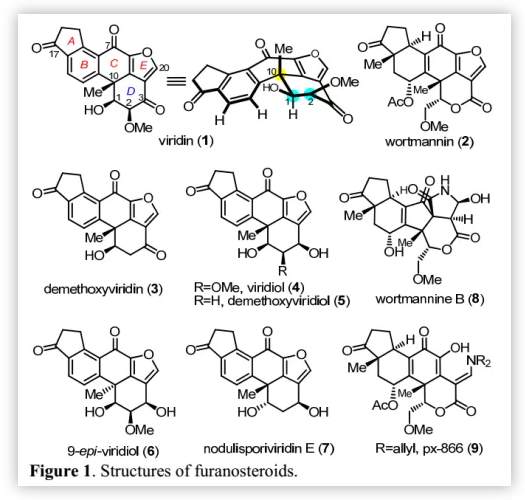
源于Gliocladium virens的呋喃甾體化合物viridiin(1)和源于Penicillium wortmannii的化合物wortmannin(2)與天然產物demethoxyviridin(3)、viridiol(4)、demethoxyviridiol(5),9-epi-viridiol(6)和nodulisporiviridin E (7)和dinor-carbon wortmannin衍生物如wortmannine B(8)(Figure 1)生源相關。呋喃甾體化合物具有很強的磷脂酰肌醇3-激酶(PI3K)抑制活性,而后者與腫瘤細胞的存活和生長密切相關。因此,這些化合物可以作為抗癌藥進一步開發,但該類化合物如wortmannin(2)在體內降解迅速且有劇毒。Wipf等人對wortmannin進行結構修飾得到的PX-866(9)成藥性增加,目前正在進行II期臨床試驗。近日,華東師范大學高栓虎教授課題組通過匯聚式方法完成了(-)-viridin(1)和(-)-viridiol(4)的不對稱全合成。
(圖片來源:J. Am. Chem. Soc.)
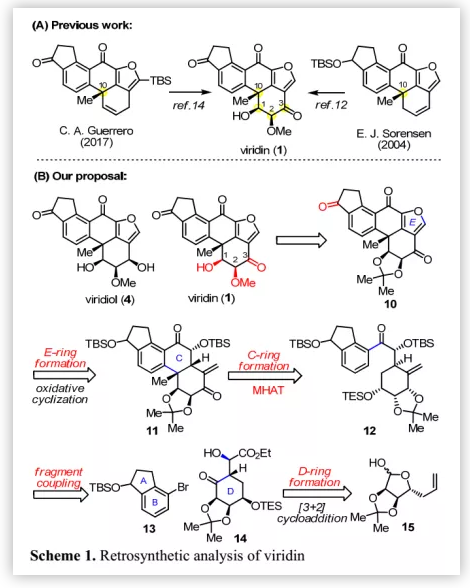
Viridin(1)含有高度氧化的甾體骨架(A-B-C-D環)和額外的呋喃環(E環)(Figure 1);其中,D環含有三個連續的手性中心,包括C-10位的芐位季碳手性中心和C-1,2位順式二醇單元。基于結構分析,作者認為通過快速構建甾類骨架和立體控制氧化態可以提高其合成效率。2004年,Sorensen課題組通過銠催化的環三聚、閉環復分解和熱電環化重排完成了viridin(1)和viridiol(4)的首次全合成;Guerrero課題組以不對稱分子內Heck反應構建五環母核為關鍵步驟完成了1和4的不對稱全合成。基于前人的工作,作者認為在D環中構建擁擠的順式二醇片段最具挑戰。迄今為止,所有的合成努力都集中在官能團引入和后期操作的立體化學控制上(Scheme 1A)。
Viridin的逆合成分析(Scheme 1B):作者嘗試通過易得的手性源L-核糖引入手性順式二醇片段,利用分子內[3+2]環加成反應構建含有關鍵的手性順式三醇片段的D環中間體14,其與二氫茚三醇片段13偶聯得到中間體12,其經鈷催化的金屬-氫化物氫遷移(MHAT)自由基反應實現C環閉環并構建出C-10位季碳手性中心。作者認為,MHAT環化的立體化學受底物控制,從而得到預期的四環化合物11。通過引入呋喃E環并改變D環的氧化態可以得到viridin(1)和viridiol(4);MHAT自由基反應不僅可以實現viridin(1)的大量制備,還是逆合成分析中進行斷鍵的重要依據。
(圖片來源:J. Am. Chem. Soc.)
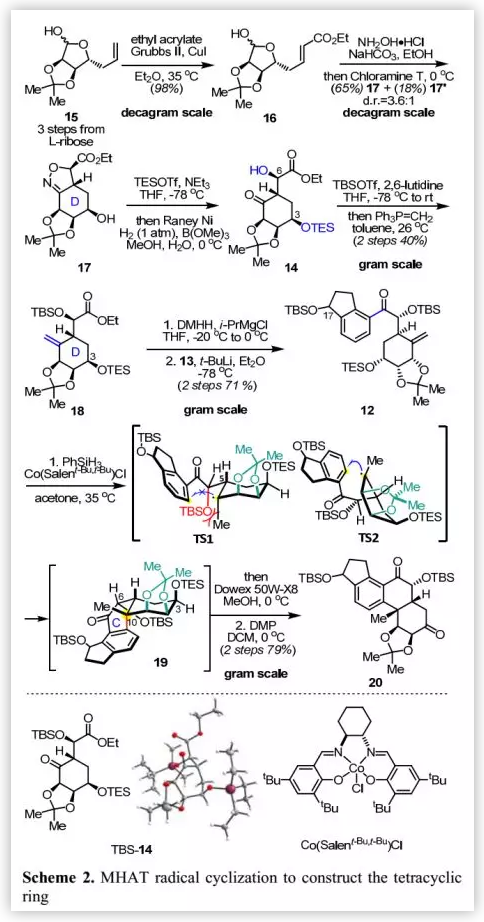
具體的合成路線(Scheme 2):作者以L-核糖為起始原料通過三步反應制備得到已知的糖衍生物15(>30 g),其經釕催化的烯烴交叉復分解反應轉化為不飽和酯16(98%),再經羥胺處理得到的肟中間體直接用于后續[3+2]環加成反應。粗品肟經Chloramine T氧化生成腈氧化物后,被分子內不飽和酯捕獲得到預期的異噁唑啉17(65%)及其非對映異構體17'(18%)(d.r.=3.6:1)。隨后,將C-3位羥基進行TES保護后,通過“一鍋”法進行異噁唑啉環的還原裂解得到含多個敏感官能團(如α-和β-羥基羰基片段)的化合物14,不經純化,直接用于下一步轉化。C-6位羥基經TBS保護得到的TBS-14的結構和立體化學通過單晶X-射線衍射確認,其經Wittig烯化得到末端烯烴18(40%,2步)。
將含D環所有必需官能團和立體中心的化合物18轉化為其Weinreb酰胺后,與二氫茚酚片段(±)-13的陰離子反應得到12,作為C-17位非對映異構體混合物。受Shenvi和Baran等人工作的啟發,作者嘗試進行C環閉環并通過MHAT自由基反應在C-10位引入季碳手性中心。在PhSiH3存在和Co(Salent-Bu,t-Bu)Cl催化下,12以極好的收率轉化為預期的四環母核19,作為單一非對映異構體。需要指出的是,這是MHAT反應首次用于合成芳香類甾體化合物。
作者認為,MHAT環化的立體化學受自由基中間體TS1和TS2的構型控制(Scheme 2),其中C-5位的側鏈處于環己烷D環的平伏鍵。結構分析表明,TS1的D環轉化為“椅式”構象可以避免由額外的縮酮環而引起的環張力,從而導致OTBS和甲基之間產生1,3-相互作用;TS2為扭曲的“船式”構象,但未產生上述空間效應。因此,TS2盡管具有更大的環張力,但仍是進行自由基環化得到四環母核19的優勢過渡態。隨后,選擇性脫除TES保護基裸露C-3位羥基,經Dess-Martin氧化得到二羰基化合物20(79%,2步)。
(圖片來源:J. Am. Chem. Soc.)
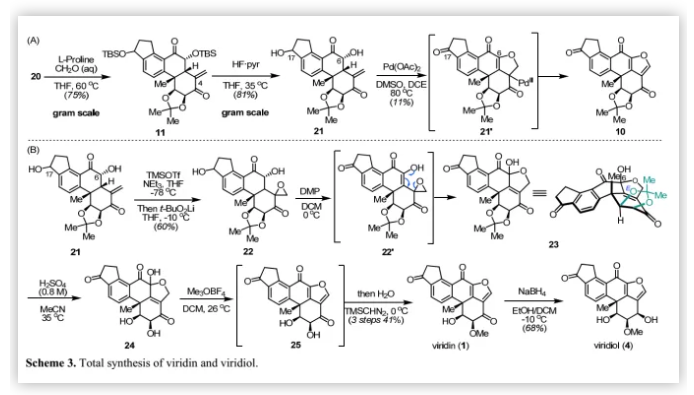
對于(-)-viridin和(-)-viridiol的合成,作者嘗試通過在C-4位進行增加一個碳單位的同系化構建多取代呋喃環,但該方法對高度氧化的D環不可行。經過廣泛的研究,作者發現烯胺化學是有效的(Scheme 3A)。在甲醛存在下,用L-脯氨酸處理20得到不飽和酮11(75%),再脫保護得到21(81%)。隨后,作者研究了鈀催化的脫氫還原和Wacker型環化以調節氧化態并構建呋喃E環。經過條件優化后,作者用Pd(OAc)2的1,2-二氯乙烷溶液處理21僅以11%的收率得到預期產物10。作者認為,化合物10的合成可以通過C-17和C-6位羥基的串聯脫氫、分子內烯醇-鈀化和中間體21'的還原消除實現。隨后,將10中的丙酮叉保護基脫除,然后甲基化得到viridin(1)。由于10處于高氧化態,在酸性條件下(BCl3)不穩定;因此,加入甲基化試劑(Me3OBF4)會產生微量的viridin(1)。
接下來,作者通過改變合成策略即利用t-BuO2Li對21的末端烯烴進行環氧化得到環氧化物22(Scheme 3B),其C-6位羥基經Dess-Martin氧化得到五環產物23。作者認為活性四羰基中間體22'以烯醇形式存在可以促進環氧開環和半縮酮化,從而得到呋喃E環。在H2SO4作用下,脫除23中丙酮叉保護基得到的順式二醇24在堿性條件下的極度不穩定性,作者選擇在離子交換樹脂上淬滅反應,然后濃縮洗脫液得到粗品24;其與Me3OBF4反應得到脫水產物25,但是其甲基化速度很慢,需加入TMSCHN2加速甲基化,最終以3步41%的收率得到viridin(1);隨后,用硼氫化鈉選擇性還原C-3位羰基以68%的收率得到viridiol(4)。作者合成的化合物1和4的1H、13C NMR和HR-MS數據與Sorensen和Guerrero等人報道的數據一致。
(圖片來源:J. Am. Chem. Soc.)
總結:華東師大高栓虎教授課題組以市售的L-核糖為起始原料分別經17和18步反應完成了呋喃類甾體天然產物viridin和viridiol的不對稱全合成。合成亮點:1)通過分子內腈氧化物-烯烴環加成構建具有關鍵手性順式三醇片段的高度取代的D環;2)利用鈷催化的MHAT自由基環化在C-10位構建C環和季碳手性中心。此外,作者開發的新合成策略可以用于生源相關的天然產物及其類似物的全合成,從而用于藥物化學和生物學研究。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn