

過渡金屬催化的1,4-加成、[2+2+2]、關環復分解、C-H鍵活化、N-雜環卡賓催化烯丙基烷基化和酰化反應,可廣泛合成P-手性化合物(圖1a)。二級膦與各種親電試劑的直接偶聯是一種更為直接的獲得具有不同官能團的手性膦化合物的方法,如過渡金屬催化烷基化、芳基化、1,4-和1,6-加成反應等(圖1b)。在溫和條件下,二級膦兩種對映體之間的簡單相互轉化是使這些反應通過動態動力學不對稱轉化(DYKAT)進行的關鍵因素之一,從而可從消旋體中獲得了對映體富集的手性膦化合物,然而,二級膦的毒性限制了其應用。
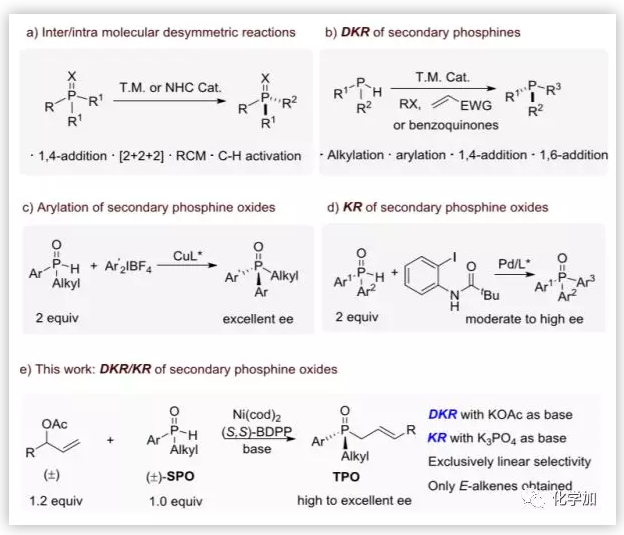
圖1. 催化不對稱合成手性膦(圖片來源:J. Am. Chem. Soc.)
相比較而言,二級膦氧化物(SPO)具有穩定、無毒、無臭等優點,然而,目前只有兩例SPO的催化不對稱反應用于合成P-手性化合物。2016年,Gaunt課題組首次報道了SPO的催化不對稱反應,該反應以優良的ee有效地得到了手性TPO。不久,蔡倩課題組報道了鈀催化的SPO的動力學拆分芳基化反應,具有中等到優良的對映選擇性。盡管有了這兩例報道,然而,為了抵消氧化副反應或確保更好的對映選擇性和產率,反應需要2當量的SPO。此外,由于SPO的消旋,大規模的DYKAT反應極具挑戰。
過渡金屬催化的不對稱烯丙基化反應在有機合成化學中取得了巨大的成就,是構建具有手性碳中心的C-C和C-X鍵的強力策略。其中,以鎳配合物為催化劑的報道較少。鎳催化的一個缺點是只有官能團耐受性差的硬親核試劑才能以滿意的對映選擇性得到產物。近日,中國科學技術大學張清偉特聘研究員課題組報道了鎳催化SPO的DKR/KR烯丙基化反應,可高效合成手性膦化合物,文章發表在J. Am. Chem. Soc.上(DOI:10.1021/jacs.9b08734)。
首先,作者以苯基甲基氧化膦(1a)和乙酸烯丙酯(2a)為模型底物,以Ni(cod)2為催化劑,對反應條件進行了優化 (圖2)。在篩選開始時,作者意識到1a的消旋可能會影響對映選擇性,1a完全轉換會導致對映選擇性的降低。因此,產物3a的ee是在<50%轉化率的情況下測定的。
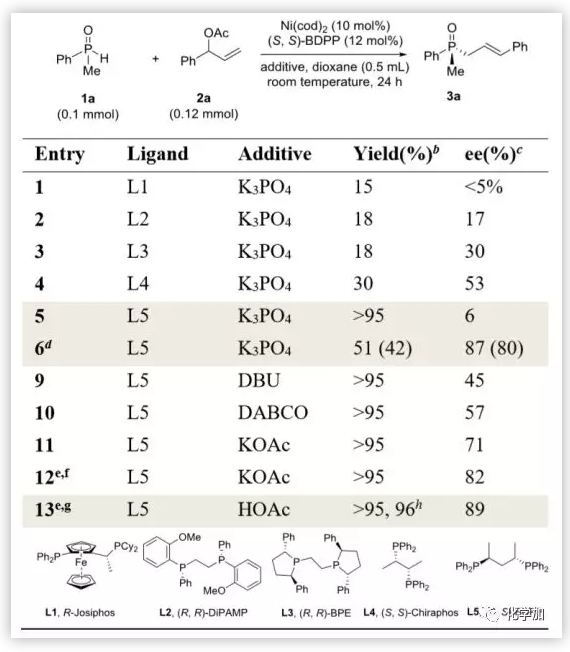
圖2. 反應條件優化(圖片來源:J. Am. Chem. Soc.)
作者初步篩選了一系列手性雙膦配體,其中(R)-Josiphos(L1)的收率僅為15%,ee<5%。以(R, R)DiPAMP(L2),(R, R)-BPE(L3)和(S, S)-Chiraphos(L4)為配體,反應的對映選擇性分別為17%,30%,53%。(S, S)-BDPP(L5),一種Chiraphos的類似物,具有良好的反應活性,3a的產率>95%,但ee只有6%。反應以50%左右的收率淬滅,3a和剩余1a的對映選擇性均較高(87%和80%ee)。這一現象表明反應是通過動力學拆分過程進行的。作者試圖進一步實現SPO的更理想的DKR,其成功的關鍵因素是平衡對映選擇性決定步驟的相對反應速率和剩余的SPO的消旋化。基于這一概念,作者篩選了大量的添加劑,以加速1a的消旋化,同時降低烯丙基化反應。在弱堿KOAc存在下,3a的ee值提高到了71%,反應稀釋后的ee值進一步提高到82%(0.05 M)。該反應可在酸性條件下進行,3a對映體選擇性優良(89% ee),分離產率96%。而底物1b與HOAc反應較慢,產率為79%,ee為92%。改用KOAc,3b的ee值為94%,且具有96%的分離產率。反應的對映選擇性與烯丙基酯的離去基團無關,含有OBz、OBoc或對甲氧基OBz基團的底物均能得到94% ee的產物,產率分別為96%、22%和95%。這可能涉及一種π-烯丙基鎳中間體,線性烯丙基酯2a’可以得到類似于2a的95%產率和94% ee,這一結果進一步證實了π-烯丙基鎳中間體的假設。
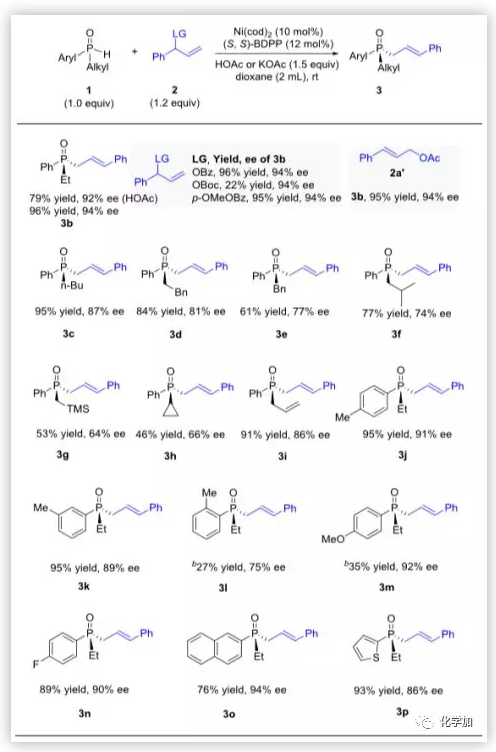
圖3. 膦氧化物底物擴展(圖片來源:J. Am. Chem. Soc.)
有了最佳反應條件,作者對底物范圍進行了考察(圖3)。對不同烷基(1c-1i)或芳基(1j-1p)的SPO進行了初步測試。烷基取代基的空間位阻對反應有重要影響。雖然這些底物(1c-1h)具有較高的對映選擇性,但空間位阻較小的底物在反應活性和對映選擇性方面(87%-64% ee,3c-3h)更有利。具有烯丙基取代基的底物1i也與反應相容,產率91%,產率86%。對于二級芳基乙基膦氧化物,間位或對位甲基苯基(1j,1k)的底物反應平穩,產物3j和3k的產率為95%,ee分別為91%和89%。而含鄰甲基苯基的底物1l反應活性差(40 ℃時產率27%),對映選擇性降低(75% ee)。帶有給電子基對甲氧基的底物1m反應也不利,產率為35%。帶有吸電子基對位氟的1n與反應條件相容,產率為89%,ee為90%。帶有2-萘基、2-噻吩基的底物1o和1p反應順利,產率分別為76%、93%,ee分別為94%、86%。
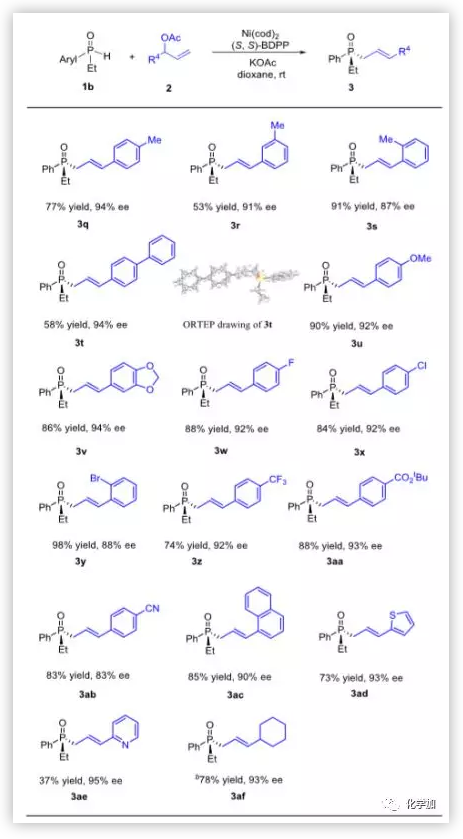
圖4. 烯丙酯底物擴展(圖片來源:J. Am. Chem. Soc.)
接著,作者研究了以1b為反應配偶體的烯丙基酯的范圍(圖4)。一系列含給電子或吸電子基的芳香取代基均具有良好的耐受性,以優良的對映選擇性(83%-94% ee)和中等至良好的產率(53%-98%)得到了目標產物(3q-3ab)。其中,產物3t的絕對構型經單晶分析確定為R。帶有鄰位溴的底物1y在鎳催化條件下仍能共存,產率為98%,ee為88%。該反應還適用于其它芳基/雜芳基取代基,包括1萘基、2-噻吩基和2-吡啶基,可得到3ac、3ad和3ae,具有優秀的對映選擇性(90%-95% ee)。而吡啶基對反應活性不利,3ae的產率37%。帶有環己基的烯丙基酯在高溫(40 ℃)下產率為78%,ee為93%。值得注意的是,所有的產物都具有完全的線性選擇性和E-構型。
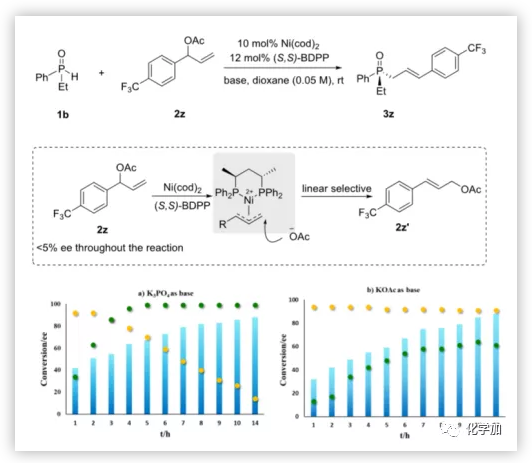
圖5. 機理研究(圖片來源:J. Am. Chem. Soc.)
為了研究KR/ DYKAT的起源,作者分別以KOAc和K3PO4為添加劑,監測了1b與2z的反應(圖5)。在這兩種情況下,未反應2z的ee在整個反應過程中保持在<5%,并且還檢測到了可能由鎳催化的線性選擇性烯丙基取代反應生成的線性區域異構體2z’。相反,1b和3z的ee與添加劑密切相關。當使用K3PO4時,觀察到了動力學拆分反應。產物3z在轉化率低于50%時檢測到高ee,而在高轉化率時檢測到低ee(圖5)。相反,1b的ee在低轉化率時低,而在高轉化率時高。根據一級動力學計算,選擇性因子為37。當使用KOAc時,觀察到了動力學拆分反應。雖然僅實現了剩余1b的部分消旋,但產物3z的ee基本保持不變。在這兩種情況下,剩余1b的絕對構型與已知化合物相類比,經HPLC保留時間確定為RP。
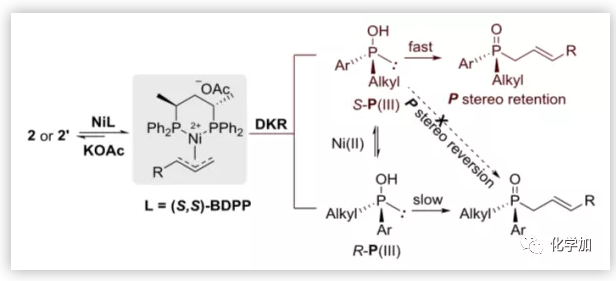
圖6. 可能的反應機理(圖片來源:J. Am. Chem. Soc.)
作者還進行了1a與每個反應組成部分的消旋化研究。結果表明,在KOAc存在下,鎳(Ⅱ)配合物可能是產生消旋的原因之一。但K3PO4對消旋有抑制作用。在此基礎上,作者提出了一種可能動力學拆分起源的機理(圖6)。在鎳配合物的催化下,烯丙基酯2或2’可形成鎳π-烯丙基中間體,再由二級膦氧化物對映選擇性親核加成,當以KOAc為添加劑時,二級膦氧化物可被鎳(Ⅱ)配合物消旋。在反應過程中,P-手性中心的絕對構型保持不變。
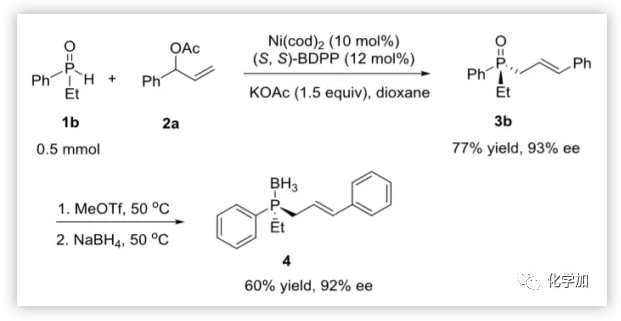
圖7. TPO的衍生化(圖片來源:J. Am. Chem. Soc.)
作者還在0.5 mmol的規模內進行了反應(圖7),在保持對映選擇性(93% ee)的同時,產物3b的收率為77%。在不影響雙鍵構型的情況下,高效得到了手性膦-BH3加成物,一鍋法制得目標產物4,收率為60%,ee值為92%。
總結:中國科學技術大學張清偉特聘研究員課題組報道了首例鎳催化SPO的動態動力學不對稱轉化 (DYKAT)烯丙基化。從外消旋烯丙基酯和二級膦氧化物(SPO)合成了一系列的P-中心的叔膦氧化物。動力學和消旋化研究揭示了DYKAT反應的起源,當KOAc用作添加劑時,Ni(II)-催化了SPO的消旋化。本研究對手性膦化合物的制備及其應用都具有重要意義。
撰稿人:詩路化語
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn