


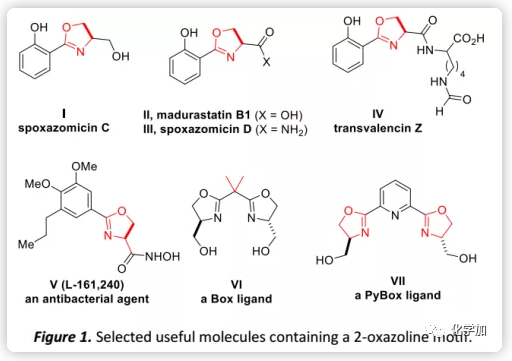
2-噁唑啉不僅廣泛存在于許多天然產物和生物活性分子(如化合物I-V,Figure 1)的雜環亞結構和藥效團,還是有機合成中的通用官能團如基于噁唑啉的配體Box和PyBox(VI-VII)。此外,噁唑啉還常用作保護基、導向基團和合成輔基。基于其廣泛的應用,開發有效的噁唑啉合成方法一直是有機合成的重要課題。目前,通過β-羥基或不飽和酰胺的環化合成噁唑啉是最直接和最常用的方法(Scheme 1a),然而其通常會涉及劇烈條件或腐蝕性試劑(如DAST和氧化劑)的使用,不可避免地導致成本增加或化學廢物產生。因此,開發溫和的催化方法意義重大。
(圖片來源:Chem. Sci.)
氧雜環丁烷是藥物化學和有機合成中常見的結構片段,與其三元環同系物(環氧乙烷)相比,其合成能力尚未得到充分研究。近日,香港科技大學孫建偉團隊開發了一種新的溫和催化方法用于從氧雜環丁烷合成噁唑啉,從而能夠快速獲得多種天然產物。
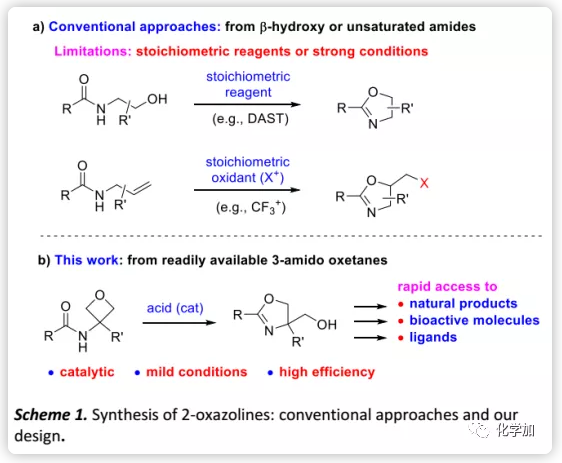
作者設想含有3-酰胺基的氧雜環丁烷經酸活化后會發生分子內氧雜環丁烷開環并自發環化形成噁唑啉環(Scheme 1b),這樣產生的噁唑啉在4-位帶有羥基可供修飾,該取代基的存在與上述重要的分子和配體完全匹配(如Figure 1和Scheme 2),從而對其可以進行快速合成。 而且,這種方法原則上是可以催化的,對傳統方法是一種補充。
(圖片來源:Chem. Sci.)
首先,作者以1a作為模型底物,考察了用于活化氧雜環丁烷片段的各種Lewis酸(Table 1)。雖然大多數均具有催化活性,但Sc(OTf)3和In(OTf)3的催化效率更高且后者略好。因此,在10 mol% In(OTf)3存在下,1a在室溫甲苯中順利反應以75%的收率得到噁唑啉2a。然而,Br?nsted酸如TsOH和HNTf2表現出極低的催化轉化率。接下來,作者對溶劑的考察發現:極性和質子溶劑如MeCN和MeOH導致低反應性,而DCM可以提高反應效率(86%產率)。最后,在40 ℃條件下,反應時間縮短至24 h,產率提高至93%。

(圖片來源:Chem. Sci.)
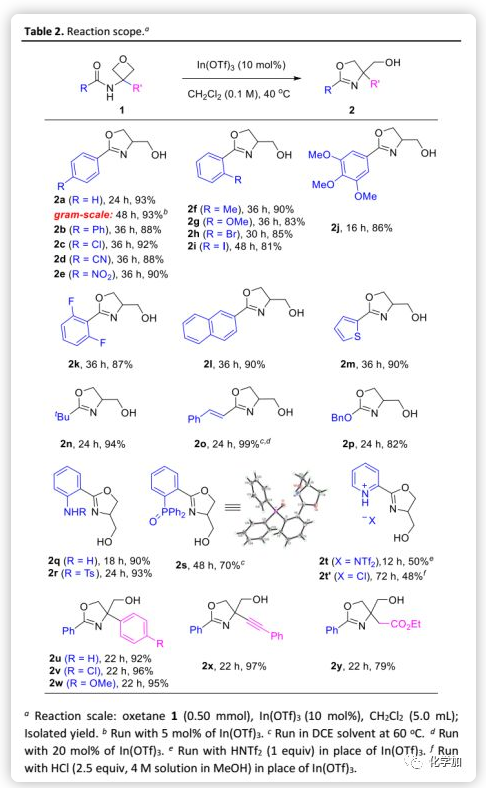
在最佳反應條件下,作者考察了該方法的普適性(Table 2)。含有不同電性的3-酰胺基氧雜環丁烷均可在溫和條件下發生分子內環化得到相應的2-噁唑啉;芳香族和脂肪族酰胺均是合適的底物。此外,α,β-不飽和酰胺和氨基甲酸酯也可以參與反應得到2-位分別含有乙烯基和烷氧基的噁唑啉。該環化基本不受酰胺官能團的空間位阻的影響,從而可以在產物中引入雜環。鑒于噁唑啉作為配體的多功能性,作者還評估了合成雙齒配體的可能性。例如,游離和受保護的氨基與氧化亞磷酸空間很近,雖然后者需要稍高的溫度,但仍能高效地形成相應的噁唑啉產物;其中,2s的結構通過單晶X-射線衍射確證。值得注意的是,In(OTf)3未能催化含吡啶的底物1t的反應,可能是由于吡啶片段與In(OTf)3競爭結合導致催化劑失活。
然而,經過(過量)化學當量的酸如HNTf2和HCl進一步優化后,可以得到預期的噁唑啉鹽產物。3,3-二取代的氧雜環丁烷也可以參與反應得到4,4-二取代的噁唑啉。總之,這種溫和的條件可以耐受各種官能團如醚、硝基、腈、芳基鹵、胺、酯、烯烴和炔基。此外,該方法在克級規模也表現出了高效的反應性。值得注意的是,與抗菌天然產物spoxazomicin C(Figure 1)相比,這些噁唑啉產物還應具有抗菌活性,并可以直接用于“構效關系”研究,進一步突出了的該反應合成效率。
(圖片來源:Chem. Sci.)
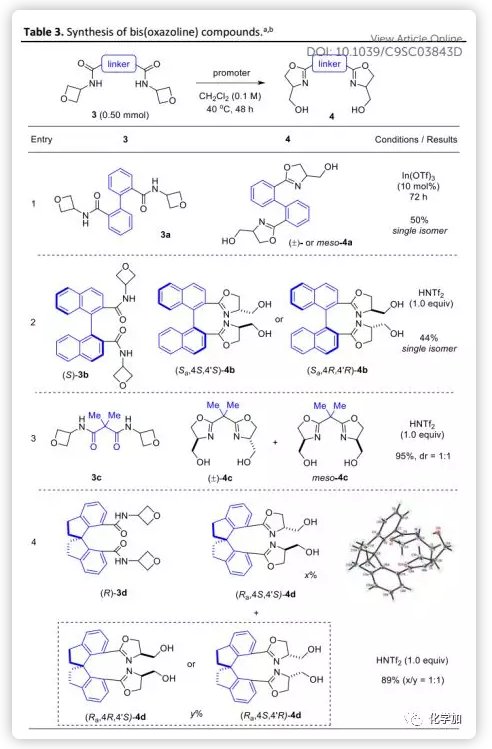
接下來,作者評估了該方法在合成雙(噁唑啉)化合物方面的能力(Table 3)。雙(酰胺)底物3經雙重環化可以得到含不同“Linker”的雙(噁唑啉)產物4。其中,4b和4d是以其對映體形式獲得,而4a和4b是作為單一異構體得到。雖然尚未有明確的解釋,但這很可能是由于最初形成的噁唑啉片段的空間取向影響了后續的環化。產物4b-d是已知的優良二齒配體,證明In(OTf)3不如HNTf2有效。值得注意的是,根據“Linker”的光學純度,這些產物可以對映體的形式生成并直接用作手性配體。
(圖片來源:Chem. Sci.)
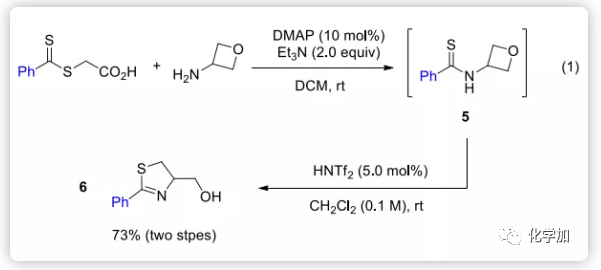
通過將酰胺單元替換為硫代酰胺,作者進一步擴展了該方法用以合成在天然產物、藥物化學和有機合成中常見的雜環:2-噻唑啉環。雖然硫代酰胺5不穩定,但其可以通過2-((苯基硫代甲酰基)硫代)乙酸和3-氨基氧雜環丁烷原位生成,再經HNTf2處理后無需純化即可得到所需的2-噻唑啉6,兩步總收率為73%(Eq 1)。
(圖片來源:Chem. Sci.)
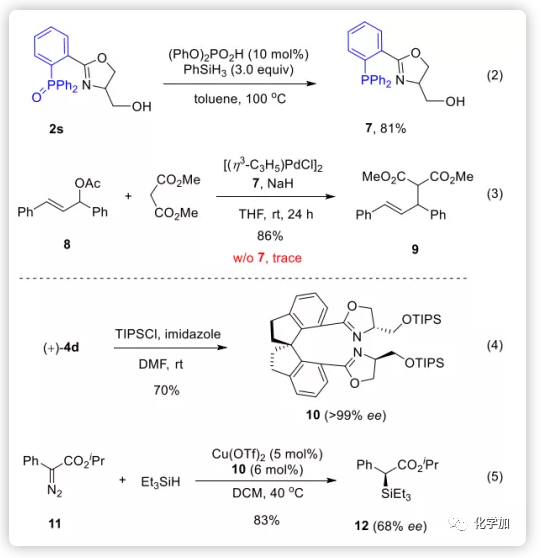
為了證明該反應的實用性,作者將噁唑啉產物用于合成反應的配體。例如,氧化膦2s經簡單還原可以得到P,N-配體7(Eq 2),利用該配體可以實現鈀催化下8的烯丙基取代以86%的收率得到產物9(Eq 3);然而,不加配體時,僅生成痕量產物。在另一個實例中,對映體純的螺環雙(噁唑啉)產物4d經TIPS保護得到的手性配體10可用于將卡賓不對稱插入到三乙基硅烷的Si-H鍵中(Eq 4-5),并且不經條件優化的情況下,可以83%的收率得到α-甲硅烷基酯12(ee,68%)。進一步優化其他反應參數,可能會改善結果。
(圖片來源:Chem. Sci.)
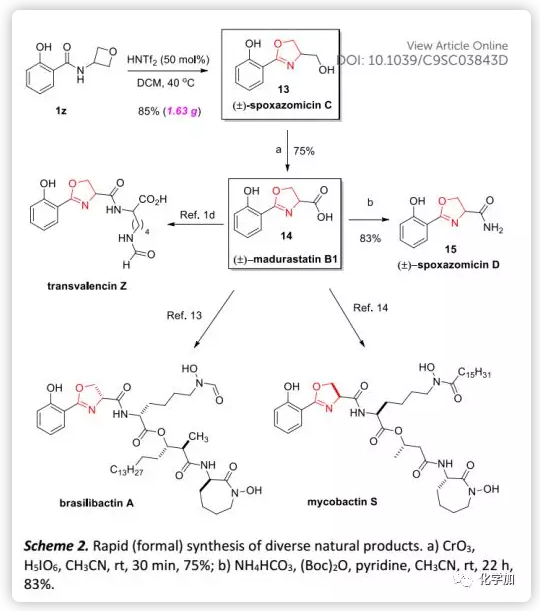
最后,作者通過快速合成各種天然產物進一步證明了該方法的實用性(Scheme 2)。例如,天然產物(±)-spoxazomicin C(13)可以由酰胺1z進行環化直接獲得,再經簡單的氧化得到另一種天然產物(±)-madurastatin B1(14),然后在NH4HCO3存在下再進一步轉化得到另一種天然產物(±)-spoxazomicin D。此外,酸14是其他天然產物如transvalencin Z、brasilibactin A和mycobactin S的已知前體以及oxachelin C的潛在中間體,而上述天然產物均表現出有趣的抗菌活性。因此,作者開發的方法不僅為其集群式合成提供了獨特有效的途徑,而且還可以進行結構修飾用于藥物研究。
(圖片來源:Chem. Sci.)
小結:香港科技大學孫建偉團隊開發了一種新的溫和的催化方法,可以實現由基于β-羥基或不飽和酰胺的氧雜環丁烷通過非催化環化合成噁唑啉,這不僅是對噁唑啉合成策略的有力補充,也是對氧雜環丁烷反應性的擴展,特別是對于雜環的合成。作者篩選的Lewis酸催化劑In(OTf)3可以使各種易得的3-酰胺基氧雜環丁烷在溫和條件下進行環化得到相應的噁唑啉。該方法也適用于各種二齒配體以及具有廣泛應用性的雙(噁唑啉)化合物的合成。此外,通過該方法所得到的產物,通常含有4-羥甲基取代基側鏈,這與許多天然產物和抗菌分子的結構完全一致。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn