



含氟有機(jī)分子在藥物化學(xué),材料化學(xué)等領(lǐng)域中扮演著關(guān)鍵角色。含氟基團(tuán)中,二氟甲基作為羥基、巰基及氨基等基團(tuán)的生物電子等排體,不僅能改變分子脂水分布及代謝性質(zhì),還可作為弱氫鍵供體發(fā)揮作用,因此受到廣泛關(guān)注。傳統(tǒng)構(gòu)建Csp3—CF2H鍵的方法主要分為兩類:分別是二氟甲基自由基對(duì)烯烴的加成與親核/親電二氟甲基物種與預(yù)活化分子的反應(yīng),其條件較劇烈,官能團(tuán)容忍性較差,因此無(wú)法用于復(fù)雜分子的后期修飾。所以,開(kāi)發(fā)溫和的二氟甲基化反應(yīng)并將其用于活性分子后期修飾意義重大。
美國(guó)邁阿密大學(xué)Wei Liu課題組在前期開(kāi)發(fā)銅介導(dǎo)烷基化合物氟官能團(tuán)化反應(yīng)(Chem. Eur. J.2018, 11559-11563.J. Am. Chem. Soc.2019, 141, 3153-3159.)基礎(chǔ)上,考慮以烷基自由基為合成二氟甲基化合物的活性中間體,其可由自然界中廣泛存在的羧酸通過(guò)氧化或還原手段引發(fā)自由基脫羧生成;如果能以羧酸為起點(diǎn),實(shí)現(xiàn)活性分子的二氟甲基化,將極大豐富二氟甲基化合物合成的手段。目前,活化羧酸的主流方法包括可見(jiàn)光催化引發(fā)或過(guò)渡金屬催化的脫羧等。銅元素作為一種常見(jiàn)金屬,廉價(jià)易得;但其穩(wěn)定性和催化性質(zhì)受環(huán)境影響大,作為催化劑的潛力尚待發(fā)掘。由于目前仍未有烷基自由基作為中間體的二氟甲基化反應(yīng)的報(bào)道,作者猜想,能否將銅作為二氟甲基向烷基自由基轉(zhuǎn)移的媒介,結(jié)合羧酸易生成烷基自由基的特點(diǎn),實(shí)現(xiàn)脂肪酸的脫羧二氟甲基化反應(yīng)。最近,他們與中科院山西煤炭所的曹直研究員團(tuán)隊(duì)合作,成功實(shí)現(xiàn)了該轉(zhuǎn)化。
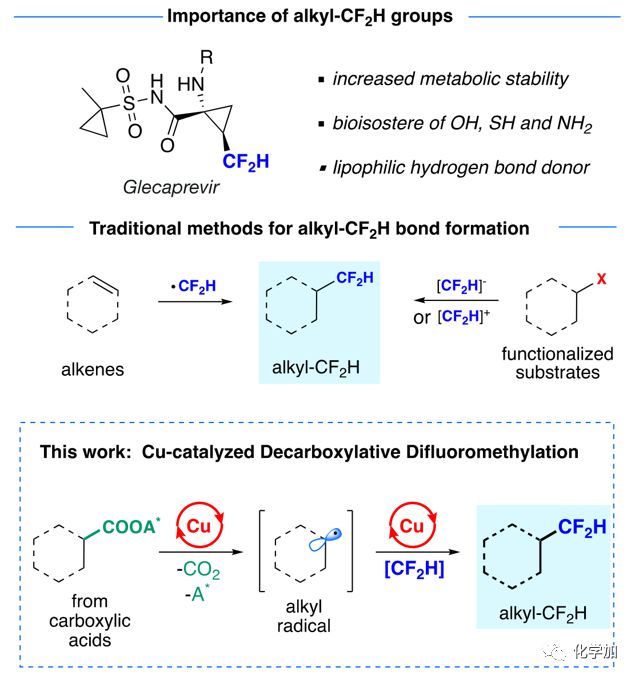
圖1. 先前及新發(fā)展的烷基二氟甲基化方法。來(lái)源:J. Am. Chem. Soc.
作者設(shè)計(jì)了如下催化循環(huán),CuI1與二氟甲基試劑2首先發(fā)生轉(zhuǎn)金屬化得到二氟甲基銅物種[CuI-CF2H]3,經(jīng)計(jì)算,以AgCl為參比電極時(shí),其標(biāo)準(zhǔn)電極電勢(shì)為-1.2 V(E0= –1.2 V vsAg/AgCl),其可能與活化酯5(RAE, E = –1.2 V vs Ag/AgCl)發(fā)生電子轉(zhuǎn)移被氧化為CuII7;5同時(shí)被還原,發(fā)生自由基脫羧得到烷基自由基6;6,7迅速重組得到CuIII8,隨后還原消除得到二氟甲基化產(chǎn)物9并再生催化劑1進(jìn)入新的催化循環(huán)。
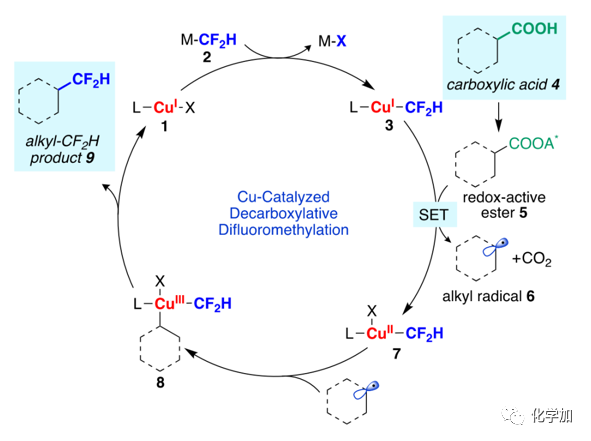
圖2. 設(shè)計(jì)的催化循環(huán)。來(lái)源:J. Am. Chem. Soc.
作者隨后以RAE 10的脫羧二氟甲基化反應(yīng)為模型反應(yīng)對(duì)反應(yīng)條件進(jìn)行探究。其最優(yōu)條件為:以20 mol% CuCl為催化劑,20 mol% bpy為配體,1.3當(dāng)量 (DMPU)2Zn(CF2H)2為二氟甲基化試劑,60 oC下于DMSO中反應(yīng)8小時(shí),能以98%收率得到二氟甲基化產(chǎn)物12(entry 1);經(jīng)驗(yàn)證,不同的NHPI酯(entry 2),溶劑的改變(entry 3-5),催化劑、配體的有無(wú)(entry 8, 12)及反應(yīng)溫度的改變(entry 9)均會(huì)對(duì)反應(yīng)效率產(chǎn)生影響;在其他文獻(xiàn)中能夠用于催化RAE自由基脫羧的NiCl2·DME無(wú)法催化該反應(yīng)(entry 7);反應(yīng)對(duì)銅鹽(entry 6)、空氣(entry 11)及現(xiàn)場(chǎng)生成10時(shí)引進(jìn)的雜質(zhì)(entry 10)不敏感;將二氟甲基試劑降至當(dāng)量,收率有所降低(entry 13);加入過(guò)量二氟甲基試劑時(shí),反應(yīng)中檢測(cè)到1,1,2,2-四氟乙烷(HCF2CF2H)及二氟甲烷(CF2H2)的生成。
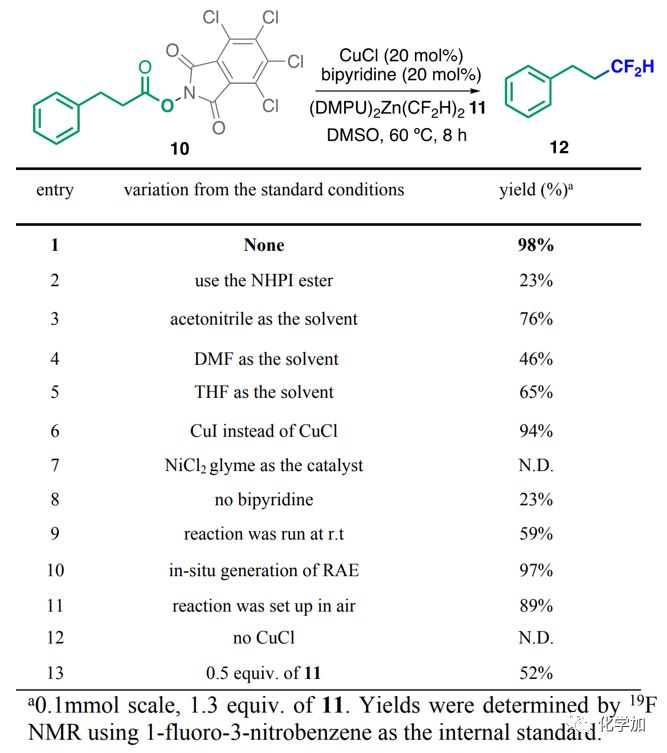
圖3. 銅催化脂肪酸的脫羧二氟甲基化反應(yīng)的條件優(yōu)化。來(lái)源:J. Am. Chem. Soc.
得到最優(yōu)條件后,作者對(duì)脫羧二氟甲基化反應(yīng)的底物適用性進(jìn)行了評(píng)估:其底物適用性廣,一級(jí),二級(jí),三級(jí)羧酸均可發(fā)生反應(yīng)。其中,底物中的溴(15,29),醛基(40),雜芳環(huán)(35, 36, 42, 54),酚羥基(27),末端炔(37)及飽和雜環(huán)(45-54)未受影響;芳香乙酸(32-34)及酚氧乙酸(40-43)脫羧后由于會(huì)生成穩(wěn)定的芐基或α-氧自由基,因此收率較高;底物為二酸時(shí),兩個(gè)羧基都能被轉(zhuǎn)化為二氟甲基(38, 39)。作者還嘗試了一鍋法活化—脫羧的方法,一級(jí)(24)、二級(jí)(53)、三級(jí)(57)羧酸,芳香/酚氧乙酸(32, 41),雜環(huán)羧酸(54)均可順利發(fā)生反應(yīng)。該反應(yīng)還可以進(jìn)行克級(jí)制備,5 mmol規(guī)模下,能以87%的收率得到49。
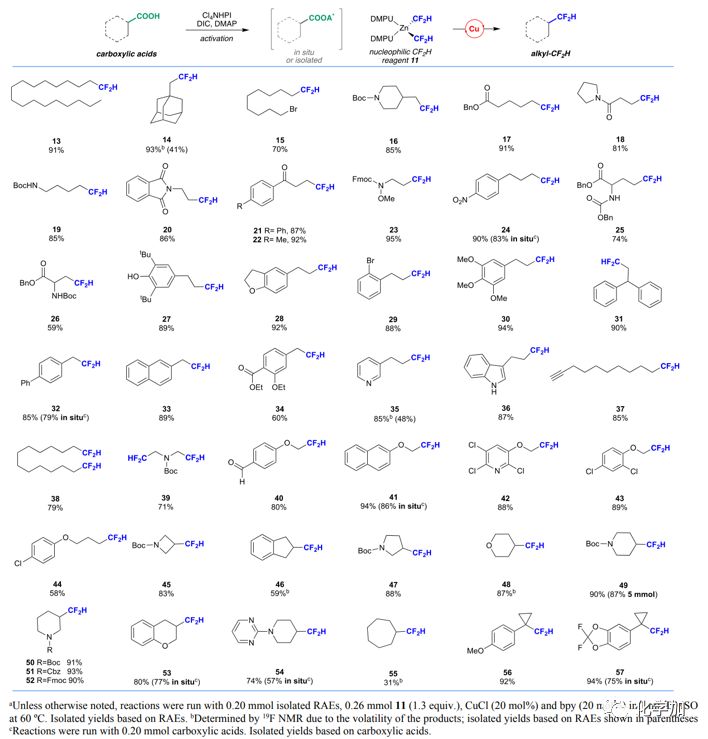
圖4.脫羧二氟甲基化反應(yīng)的底物適用性。來(lái)源:J. Am. Chem. Soc.
作者隨后對(duì)復(fù)雜活性分子進(jìn)行了二氟甲基化修飾。含二氟甲基的加巴噴丁58,巴氯芬59,雙氯酚酸60,醋氯酚酸61能以中等至優(yōu)秀的收率得到。雜環(huán)藥物,包括吲哚美辛62,伊索克酸63,托美汀64和奧沙普秦65也可以順利反應(yīng)。甾體羧酸(68-70),厄多司坦(71)和生物素(72)中的羧基也以中等以上收率被轉(zhuǎn)化為二氟甲基。結(jié)構(gòu)復(fù)雜的霉酚酸(73)和立普妥(74)的脫羧二氟甲基化反應(yīng)結(jié)果也令人滿意。其中,化合物62,66和73可通過(guò)一鍋法得到,證明該方法在藥物改造中同樣奏效,進(jìn)一步降低了復(fù)雜分子二氟甲基化修飾的難度。
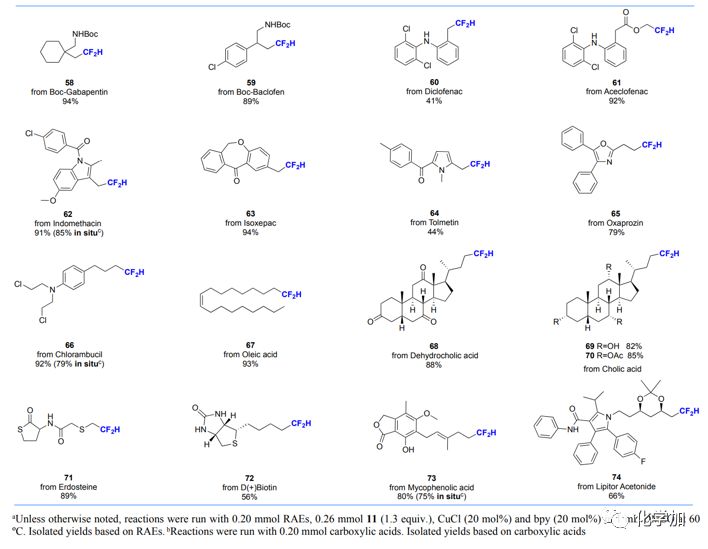
圖5. 復(fù)雜生物分子的改造。來(lái)源:J. Am. Chem. Soc.
為驗(yàn)證反應(yīng)機(jī)理,作者向底物10的脫羧二氟甲基化反應(yīng)體系中加入1.0當(dāng)量的自由基捕獲劑TEMPO,此時(shí)12的收率降低并檢測(cè)到TEMPO捕獲產(chǎn)物75。通過(guò)76的自由基鐘實(shí)驗(yàn),作者以77%收率得到開(kāi)環(huán)產(chǎn)物。這兩項(xiàng)實(shí)驗(yàn)證明反應(yīng)經(jīng)歷了烷基自由基歷程。
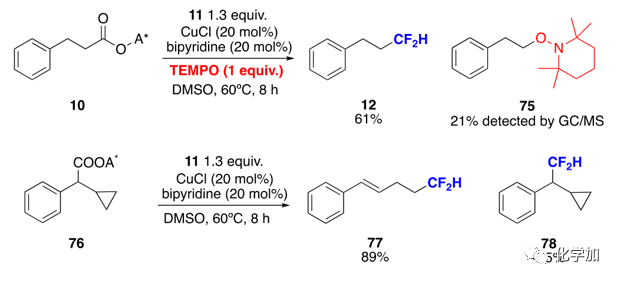
圖6. 機(jī)理驗(yàn)證。來(lái)源:J. Am. Chem. Soc.
總結(jié):邁阿密大學(xué)的Wei Liu課題組和中科院山西煤炭所的曹直課題組開(kāi)發(fā)了首例銅催化脂肪酸的脫羧二氟甲基化反應(yīng),這也是首例非可見(jiàn)光引發(fā)銅催化RAE的C-C鍵生成反應(yīng)。反應(yīng)收率較高,具有優(yōu)良的底物適用性和官能團(tuán)耐受性,在復(fù)雜活性分子的后期修飾中也表現(xiàn)出強(qiáng)大的潛力。更重要的是,該反應(yīng)獨(dú)特的二氟甲基向烷基自由基轉(zhuǎn)移的機(jī)理將為開(kāi)發(fā)新型的二氟甲基化反應(yīng)提供新思路。
撰稿人:H.D.
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn