
圖 1 “長江三鮮”:河豚、刀魚和鰣魚(圖片來源于網(wǎng)絡(luò))
中國民間有“拼死吃河豚”的說法,相傳過去吃河豚時會在餐桌旁準(zhǔn)備好稀釋的糞便,一旦出現(xiàn)中毒癥狀便立即催吐。即便如此,河豚的美味依然讓那些“吃貨”們欲罷不能。相傳蘇軾謫居常州之時,當(dāng)?shù)厥a(chǎn)河豚,有位士大夫烹制河豚手法獨到,蘇學(xué)士品嘗后贊不絕口,發(fā)出“據(jù)其味,真是消得一死!”的感慨。河豚的食用處理需要專業(yè)人士進(jìn)行,因而我國對河豚的銷售并未完全開放,品嘗河豚的美味并非輕而易舉之事。與我們鄰近的日本擁有悠久的“食魚文化”,據(jù)統(tǒng)計日本可食用的魚類超過四百多種,其中的料理方法更是不計其數(shù),在眾多魚類美食中,日本人對河豚的喜愛可以用癡迷來形容,本土的河豚產(chǎn)量早已無法滿足巨大的需求而不得不依賴進(jìn)口。

圖 2 日本河豚廚師與食客之間的完全信任(圖片來源于網(wǎng)絡(luò))
河豚,其實學(xué)名應(yīng)該是河鲀,在中國俗稱氣泡魚、吹肚魚、氣鼓魚等,而之所以獲得這些俗名,是因為它在面對外來危險時會將身體膨脹數(shù)倍同時將皮膚表面的小刺豎起達(dá)到自衛(wèi)目的,許多表情包和影視作品也紛紛借用了河豚這種“萌萌噠”的形象。除了通過膨脹身體“虛張聲勢”,河豚真正防身的武器來源于它的毒素——河豚毒素(tetrodotoxin,TTX),這也正是導(dǎo)致食用河豚中毒的罪魁禍?zhǔn)住?/span>

圖 3 河豚表情包和電影《海底總動員》中的河豚形象(圖片來源于網(wǎng)絡(luò))
植物毒素例如嗎啡(morphine)、阿托品(atropine)和番木鱉堿(strychnine)等早在19世紀(jì)就被分離得到純品,然而多次嘗試后人們依然無法分離得到純凈的河豚毒素更別提揭開它的“廬山真面目”。眾所周知,植物毒素大都屬于生物堿類物質(zhì),微溶于水而易溶于有機(jī)溶劑。遺憾的是,所有適合生物堿的提取方法用在提取河豚毒素時均不奏效。真正的突破發(fā)生在1955年,日本化學(xué)家平田義正(Hirata Yoshimasa)從河豚魚中首次分離出純品TTX并在隨后的幾年中致力于TTX的結(jié)構(gòu)解析,1964年他和同為日本化學(xué)家的津田恭介(Tsuda Kyosuke)以及美國著名化學(xué)家伍德沃德(R. B. Woodward)在京都召開的第3屆IUPAC國際天然產(chǎn)物化學(xué)大會上同時報道了TTX的正確結(jié)構(gòu),震驚世界。

圖 4 左起:平田義正、津田恭介和伍德沃德
TTX的化學(xué)結(jié)構(gòu)解析并非一件易事,雖然化學(xué)家們早已通過化學(xué)反應(yīng)確定了TTX結(jié)構(gòu)中存在的特殊化學(xué)基團(tuán)(官能團(tuán)),但是其精確結(jié)構(gòu)的確定還得依賴X-射線晶體衍射。幸運的是,化學(xué)家們將TTX置于鹽酸和丙酮以及甲醇的混合溶液中得到了非常漂亮的晶體物質(zhì),隨即確定了它的精確結(jié)構(gòu)。對比二者的分子式不難發(fā)現(xiàn),晶體結(jié)構(gòu)中增加的部分正是來自混合溶液(紅框部分),接下來只需要“逆推”就可以獲得TTX的真實結(jié)構(gòu)。可事實真就如此嗎?當(dāng)化學(xué)家們對TTX進(jìn)行紅外光譜測試時竟然沒有觀測到結(jié)構(gòu)中極其特殊的也是唯一的羰基吸收峰,而X-射線晶體衍射又是公認(rèn)的最權(quán)威的結(jié)構(gòu)解析手段,這一相互矛盾的實驗結(jié)果又該如何解釋呢?化學(xué)家們在紅外光譜中發(fā)現(xiàn)了與晶體衍生物相同的胍鹽結(jié)構(gòu)吸收信號,這意味著兩個結(jié)構(gòu)都含有胍鹽結(jié)構(gòu)。又經(jīng)過細(xì)致分析,化學(xué)家們最終確定TTX其實存在兩種平衡態(tài)結(jié)構(gòu),只有在酸性條件下才可能觀察到晶體衍生物中的內(nèi)酯結(jié)構(gòu)。
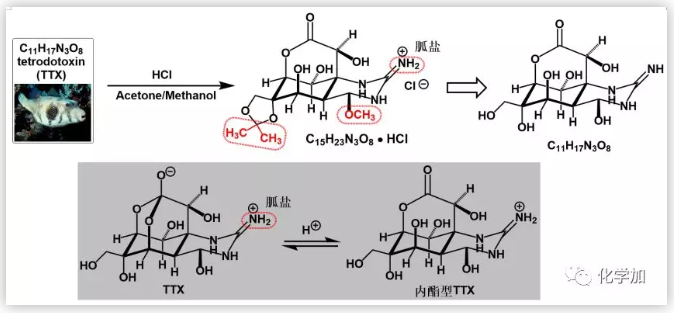
圖 5 TTX的化學(xué)結(jié)構(gòu)及結(jié)構(gòu)解析簡要示意圖
由于TTX結(jié)構(gòu)的特殊性,它在有機(jī)溶劑和水中的溶解性都較差,僅溶于醋酸等弱酸性溶劑,并且在堿性和強(qiáng)酸性溶劑中亦不能穩(wěn)定存在,這也是TTX久久不能被分離得到純品的重要原因。TTX 獨特復(fù)雜的結(jié)構(gòu)和顯著的生物活性吸引了大批有機(jī)合成化學(xué)家的目光,被認(rèn)為是一個極富挑戰(zhàn)性和吸引力的研究課題,同時也是非常令人可畏的全合成目標(biāo)。1972年,時任名古屋大學(xué)的Kishi Yoshito教授與學(xué)生Tohru Fukuyama率先完成了TTX外消旋體的全合成(作者注:Kishi Yoshito教授是世界著名的全合成大師,曾完成海葵毒素的全合成,他的學(xué)生Tohru Fukuyama也是全合成領(lǐng)域的泰山北斗)。他們以對苯二醌取代的乙酮肟和丁二烯為起始原料,采用Diels-Alder [4+2]環(huán)加成反應(yīng)構(gòu)建兩個六元環(huán)骨架,再利用經(jīng)典的Beckmann重排反應(yīng)順利得到乙酰胺產(chǎn)物,被還原后的羰基進(jìn)攻環(huán)氧化的雙鍵得到重要中間體,后續(xù)經(jīng)過數(shù)十步反應(yīng)成功得到外消旋的TTX產(chǎn)物。隨著不對稱合成的迅猛發(fā)展,斯坦福大學(xué)Du Bois教授和名古屋大學(xué)Minoru Isobe教授在2003年同時報道了TTX的不對稱全合成,Du Bois教授利用他們擅長的銠(Rh)催化的C-H鍵胺化反應(yīng),突顯了該策略在天然產(chǎn)物全合成中的巨大優(yōu)勢;Minoru Isobe教授則通過高選擇性的立體反應(yīng),以及模擬生物有機(jī)合成過程中羥基的保護(hù)方式,從而控制TTX 分子中全部的立體中心。隨后,采用不同合成路線的TTX不對稱全合成也相繼得到報道,TTX 的不對稱全合成曾被稱為有機(jī)合成化學(xué)中偉大的突破和成就之一。
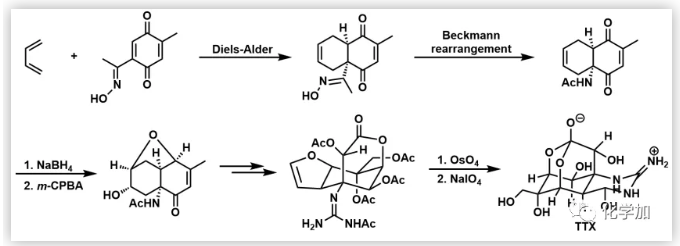
圖 6 Kishi Yoshito教授全合成TTX的簡要路線
TTX是已知的毒性最強(qiáng)的非蛋白類神經(jīng)毒素之一,其毒性是劇毒物氰化鈉(NaCN)的1250倍,幾乎對所有的動物都具有致命毒性。雖然河豚是利用體內(nèi)的TTX來“御敵”或者捕食其他生物,但TTX是如何在其生物體內(nèi)產(chǎn)生或積聚的,目前仍沒有定論。有生物學(xué)家認(rèn)為,TTX并非河豚獨有,在其他生物例如蠑螈、蝦虎魚、甲藻、扁形蟲、章魚等的體內(nèi)也發(fā)現(xiàn)了TTX或TTX類似物,這些生物的進(jìn)化程度差異巨大,其實很難想象這些差異巨大的生物都同時進(jìn)化或保留了合成TTX的功能,因此生物學(xué)家推斷河豚體內(nèi)的TTX 可能是通過食物鏈攝食含有該毒素的魚、蝦、蟹、貝類及藻類等,最終在體內(nèi)富集產(chǎn)生的;顯然這個說法也不能完全令人信服,因為科學(xué)家后來發(fā)現(xiàn)海洋中有些生物也吃和河豚同樣的食物,但它們的體內(nèi)并不含有TTX,所以他們進(jìn)而推斷河豚體內(nèi)可能含有特殊的保留TTX的機(jī)制。目前,大多數(shù)學(xué)者認(rèn)為河豚體內(nèi)的河豚毒素是受食物鏈和微生物雙重影響的結(jié)果。神奇的“造物主”為我們留下了這個懸而未解的謎題,未來是否有更合理的解釋讓我們拭目以待。
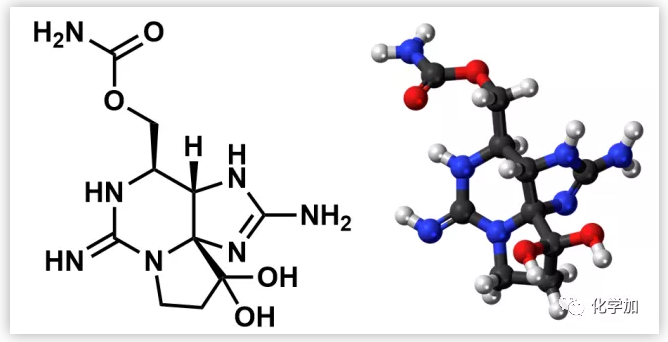
圖 7 與TTX結(jié)構(gòu)及作用機(jī)制相似的石房蛤毒素(Saxitoxin,STX)
河豚毒素雖為劇毒,但其具有潛在的、巨大的醫(yī)藥開發(fā)價值。臨床應(yīng)用研究顯示,河豚毒素可以用作消炎鎮(zhèn)痛藥物,還有局麻、治療肌肉痙攣的功效,既可以治療心血管疾病,又可以作為毒品的戒斷藥物,不得不說,臨床上應(yīng)用的許多藥物都直接或間接來源于天然產(chǎn)物,天然產(chǎn)物已成為發(fā)現(xiàn)治療重大疾病藥物或重要先導(dǎo)化合物的重要源泉。河豚仿佛是大自然刻意留給人類的一座“寶庫”,相信未來我們一定可以從它身上挖掘出更具價值的東西。
參考資料
[1] 郭瑞霞等. 天然藥物化學(xué)史話: 河豚毒素[J]. 中草藥, 2014, 45(9): 1330-1335.
[2] 王麗雅等. 河豚的食用安全性及營養(yǎng)價值研究進(jìn)展[J]. 上海農(nóng)業(yè)學(xué)報, 2012, 123-128.
[3] 張世義, 沈慧. 河豚及其文化[J]. 生物學(xué)通報, 2016, 51(9): 11-13.
[4] Kishi, Y., et al. "Synthetic studies on tetrodotoxin and related compounds. III. Stereospecific synthesis of an equivalent of acetylated tetrodamine." J. Am. Chem. Soc.1972, 94(26), 9217-9219.
[5] Kishi, Y., et al. "Synthetic studies on tetrodotoxin and related compounds. IV. Stereospecific total syntheses of DL-tetrodotoxin." J. Am. Chem. Soc.1972, 94(26), 9219-9221.










