



手性醛催化劑作為一種強有力的有機催化劑廣泛應用在胺化學當中。因此,高效合成多樣性的手性醛催化劑一直是化學家關注的焦點。隨著時間的推移,科學家們合成出了多種類型的手性醛催化劑。從早期的Kuzuhara和Breslow教授等人合成的平面手性的仿生吡哆醛環(huán)芳烴催化劑,再到后來趙寶國教授發(fā)展的脯氨醇衍生的點手性吡哆醛和軸手性吡哆醛催化劑(Scheme 1a)。近期,郭祺祥教授等人發(fā)展了一種新型軸手性醛催化劑的方法,主要從手性BINOL骨架出發(fā),歷經(jīng)8-9步左右的轉化得到,該類催化劑可用于甘氨酸酯的不對稱催化活化反應當中(Scheme 1b)。盡管一些手性醛催化劑的合成已被報道出來,但高效合成雙芳基軸手性醛催化劑仍是一大挑戰(zhàn)。
近日,浙江大學史炳鋒課題組報道了Pd-催化旋轉禁阻選擇性C-H萘基化合成手性醛催化劑的新策略(Scheme 1c)。該方法連續(xù)進行三步C-H鍵官能團化反應,簡單高效構建了軸手性醛催化劑,且產(chǎn)物體現(xiàn)出了優(yōu)秀的催化性能。
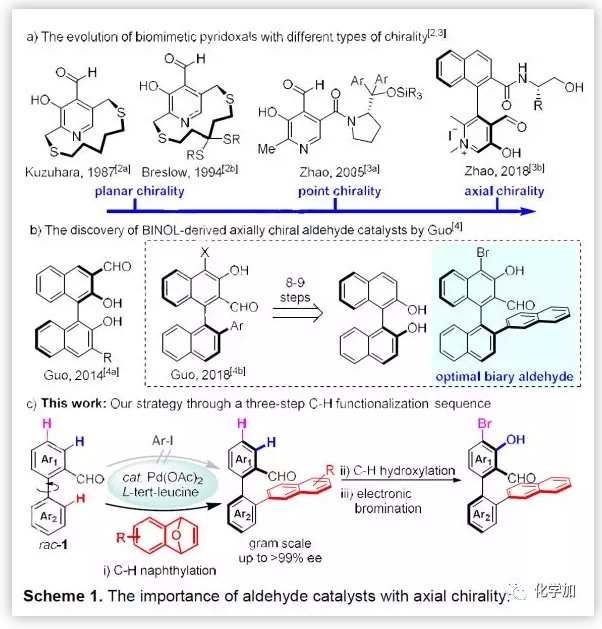
(圖片來源:Angew. Chem. Int. Ed.)
如Scheme 2a所示,對雙芳基軸手性醛催化劑6進行逆合成分析,化合物6可由5經(jīng)過親電溴化得到,5又可以經(jīng)過3的C-H鍵氧化得到,而3可以從外消的醛1經(jīng)過不對稱C-H鍵萘基化得到,共需要三步。但這一方法在優(yōu)化第一步C-H鍵萘基化過程出現(xiàn)問題,當選用萘基碘作為芳基化試劑時,嘗試大量條件都不能得到化合物3(Scheme 2b)。最后,使用7-氧雜苯并降冰片二烯作為萘基化試劑反應順利發(fā)生,作者提出了可能反應機理:首先底物芳基醛1與手性氨基酸縮合得到亞胺中間體A1和B1;然后對B1進行C-H鍵活化得到中間體C1,隨后發(fā)生2a的遷移插入得到中間體D1,b-氧消除得到中間體E1,質子化釋放出催化劑得到F1,最后脫氫芳構化得到目標化合物3(Scheme 2b)。
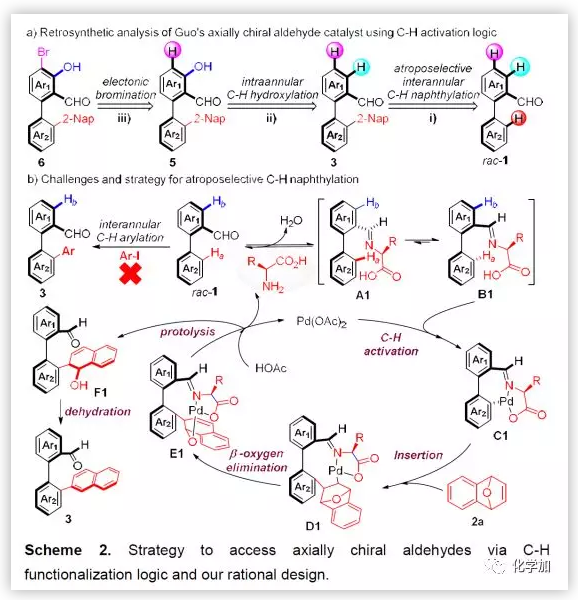
(圖片來源:Angew. Chem. Int. Ed.)
為了驗證以上設想,作者以rac-1a和7-氧雜苯并降冰片二烯為模板底物、Pd(OAc)2為預催化劑,L-叔亮氨酸為手性配體,在60 oC條件下進行條件篩選。首先對常規(guī)的溶劑進行篩選(DCE, THF, Dioxane, Toluene, HFIP, TFE等),發(fā)現(xiàn)單一溶劑能以高達99% ee得到目標化合物,但產(chǎn)率僅為13%(Table S1,entry 5)。隨后當使用TFE/HOAc混合溶劑時,發(fā)現(xiàn)產(chǎn)率提高到32%(Table S1,entry 8)。該現(xiàn)象說明有機酸的加入對反應的活性起到了促進的作用,因此緊接著對一系列的有機酸進行考察。最后發(fā)現(xiàn),當添加金剛烷乙酸和nPrCO2Na時能以71%的產(chǎn)率和>99%的ee值得到3a(Table S1,entry 13)。
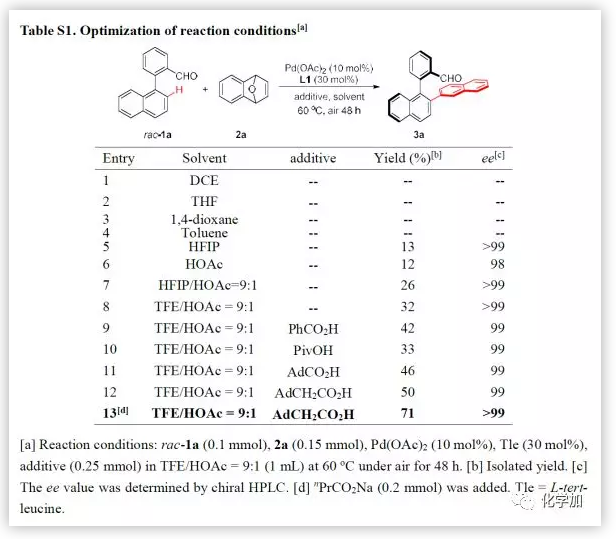
(圖片來源:Angew. Chem. Int. Ed.)
在最佳條件下,作者考察了C-H鍵萘基化反應的底物范圍(Table 1)。結果表明,底物rac-1的聯(lián)芳基片段對吸電子和供電子基團均有良好的兼容性(-OMe, -CF3, -Me,-F, -Cl, and -SPh)(3b-3s)。值得注意的是,當Ar2基團為苯基對位含有取代基時,還可以通過去對稱化的過程實現(xiàn)軸手性雙芳基化合物的合成(3t-3v)。作者還對底物2的普適性進行考察,使用該方法同樣能得到目標化合物3w-3z。其中非芳構化產(chǎn)物3y和3z的產(chǎn)生進一步證實了反應過程可能經(jīng)歷理想模型中F1中間體。
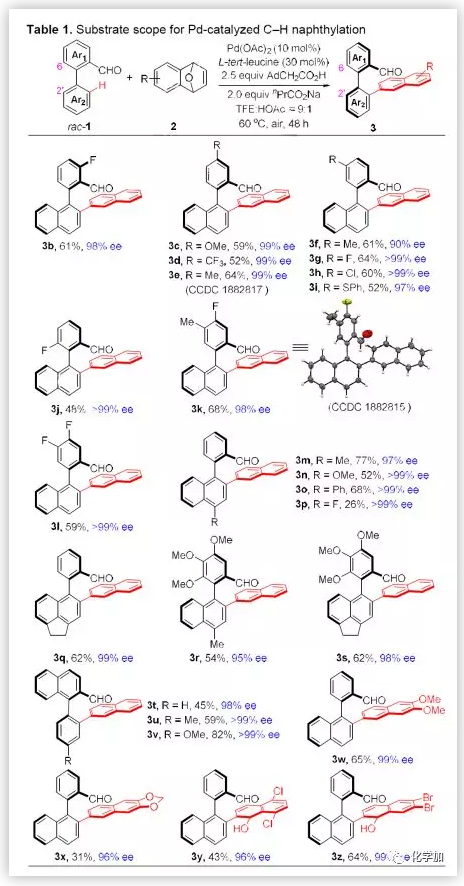
(圖片來源:Angew. Chem. Int. Ed.)
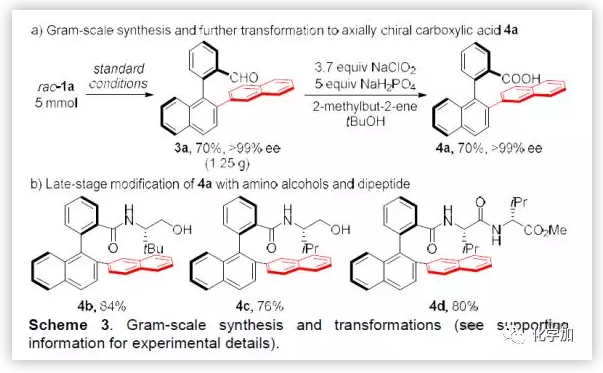
在最優(yōu)條件下,以70%的產(chǎn)率和>99%的ee值完成了3a的克級規(guī)模制備,進一步氧化以對映選擇性保持的結果得到軸手性芳基酸4a(Scheme 3)。隨后,使用氨基醇和二肽類化合物對4a進行修飾,縮合得到一系列的軸手性酰胺類配體4b-4d(Scheme 3)。這種新型手性骨架有望作為肽基催化劑進行催化應用。
(圖片來源:Angew. Chem. Int. Ed.)
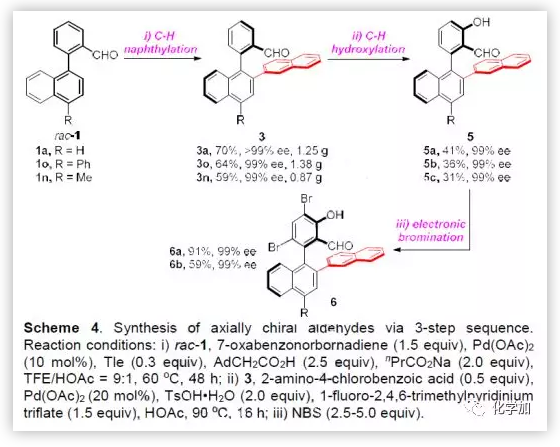
隨后,作者嘗試了連續(xù)的三步C-H鍵官能團化反應,合成軸手性醛催化劑6(Scheme 4)。反應從雙芳基醛底物rac-1出發(fā),經(jīng)由C-H鍵萘基化、C-H鍵羥基化以及親電溴化完成了軸手性醛6a-6c的合成(up to 91%產(chǎn)率,99% ee)。其中,第二步的C-H鍵氧化過程非常關鍵,反復文獻調研發(fā)現(xiàn),當對Sorensen教授所報道的條件進行調整后可以有效避免醛基的轉化,能夠順利得到預期的氧化產(chǎn)物5a-5c,并能完成克級規(guī)模合成。
(圖片來源:Angew. Chem. Int. Ed.)
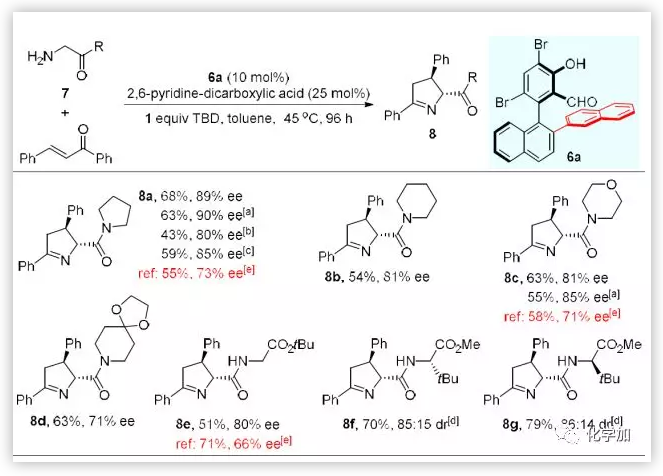
最后,作者將上述合成的軸手性醛催化劑6a運用到查爾酮與甘氨酸衍生的酰胺與二肽類底物7的不對稱反應當中(Scheme 5)。郭祺祥教授所報道過的反應中,這一胺類底物7的反應活性較低,得到的產(chǎn)物的對映選擇性不理想。對比發(fā)現(xiàn),當使用6a為催化劑時,能夠順利發(fā)生反應得到手性吡咯啉衍生物8,且產(chǎn)物8a、8c以及8e都能得到比文獻報道更優(yōu)的產(chǎn)率和對映選擇性,說明作者所合成的這一類新型的手性醛催化劑具有一定的優(yōu)勢。
(圖片來源:Angew. Chem. Int. Ed.)
總結:浙江大學史炳鋒教授課題組報道了Pd-催化旋轉禁阻選擇的C-H萘基化合成手性醛催化劑的新策略(Scheme 1c)。該策略簡單高效,僅需連續(xù)三步C-H鍵官能團化反應即可構建一系列軸手性醛催化劑。進一步的研究表明,該類催化劑在較低活性胺底物中體現(xiàn)出了更優(yōu)的催化性能。
史炳鋒教授課題組:https://person.zju.edu.cn/bfshi/617422.html
撰稿人:莫非
聲明:化學加刊發(fā)或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn