

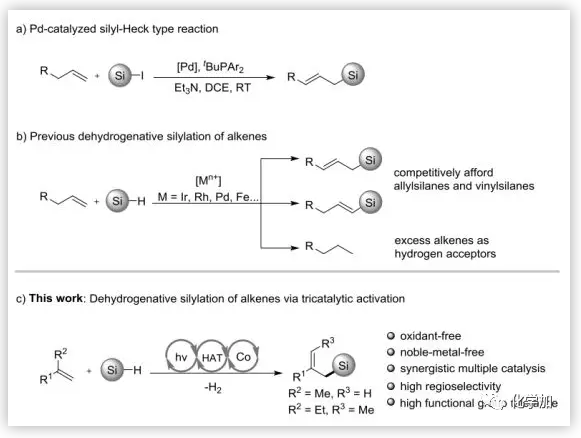
圖1. 合成取代烯丙基硅烷的策略(圖片來源:Angew. Chem. Int. Ed.)
烯烴直接偶聯生成烯丙基硅烷是一種步驟高效、原子經濟的合成方法,例如,Watson報告了Pd-催化硅基Heck反應,利用端烯和TMSI制備烯丙基硅烷(圖1a)。而高選擇性脫氫硅烷化反應合成烯丙基硅烷仍具有挑戰性,這些反應大多需要對水分敏感的貴金屬催化劑或過量的烯烴,并且由于區域選擇性低而得到烯丙基和乙烯基硅烷混合物(圖1b)。因此,更有效和環境友好的合成方法仍然是迫切需要的。
由于條件溫和,可見光在合成領域中的應用受到人們的廣泛關注。將光催化與其它催化方法相結合,可以實現新的光催化轉化。最近,吳驪珠等發展的光氧化還原介導的脫氫交叉偶聯反應就避免了使用任何氧化劑,并提供了一個有效構建C-C,C-X鍵的方法,但反應模式和底物范圍仍然有限。與烯烴和不同親核試劑的交叉偶聯相比,脫氫交叉碳-硅偶聯反應是一種可靠的合成技術。考慮到Si-H和C-H鍵的BDEs相似,親電自由基或自由基陽離子的攫氫過程也能活化Si-H鍵。為實現這一目標,需要解決的主要挑戰是如何避免氫硅化過程和乙烯基硅烷副產物。近日,蘭州大學化學院許鵬飛教授課題組提出了一種新的三催化活化方法,即光氧化還原、氫原子轉移和鈷催化的協同作用,為烯丙基硅烷的選擇性構建提供了一條有效而普適的途徑,文章發表在Angew. Chem. Int. Ed.上(DOI:10.1002/anie.201904707)。
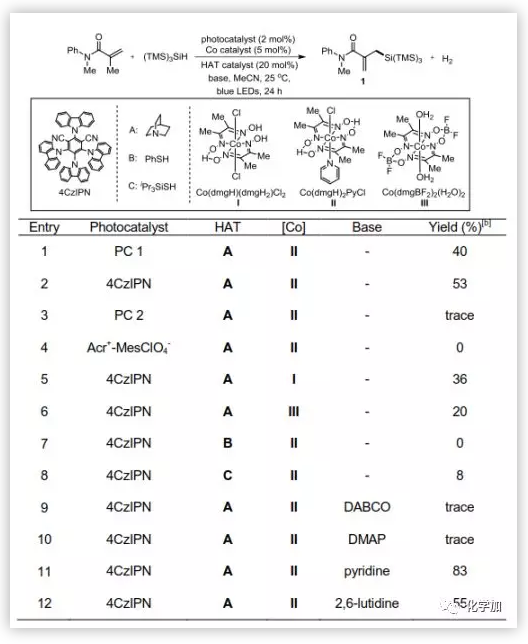
圖2. 反應條件的優化(圖片來源:Angew. Chem. Int. Ed.)
如圖2所示,作者在室溫下以三(三甲基硅基)硅烷(TTMSS)作為硅自由基前體,以Ir[dF(CF3)ppy]2(dtbbpy)PF6為光催化劑,A為HAT催化劑,Co(dmgH)2 PyCl II為質子還原催化劑,N-甲基-N-苯基甲基丙烯酰胺為硅自由基受體,合成了期望的烯丙基硅烷產物1(產率為40%)。當用4CzIPN代替Ir[dF(CF3)ppy]2(dtbbpy)PF6時,產物1的收率提高到53%。當以之前報道的HAT催化劑如噻吩醇(B)和三異丙基硅硫醇(C)代替 (A)時,要么沒有反應,要么產率很低。為了提高反應收率,作者對各種堿進行了考察,當以吡啶為堿時,收率提高到了83%。溶劑篩選表明,MeCN效果最佳。此外,控制實驗表明,光催化劑、鈷催化劑、HAT催化劑和可見光源都是反應的必要條件,在沒有它們的情況下,沒有反應。
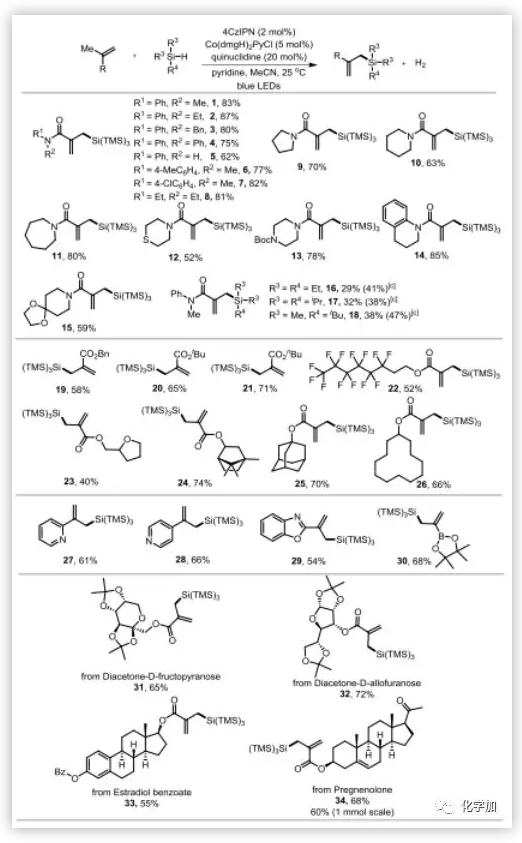
圖3. 底物擴展(圖片來源:Angew. Chem. Int. Ed.)
有了最佳反應條件,作者對各種烯烴的反應性進行了探討。如圖3所示,一系列甲基丙烯酰胺都是合適的底物,包括那些氮核上具有烷基和苯基的底物,并且全部得到良好的產率(1-4,75-87%)。5中存在N-H鍵,產率略低。具有取代苯基的底物也能以中等產率(6和7)得到產物。在這種轉化(8-15)中,非環狀和環狀不飽和二烷基酰胺都具有良好的耐受性。與5-和6-元雜環相比,7-元雜環的產率最高(11,80%)。此外,具有O、S或N原子的其它雜環也可用于該反應(12-15,52-85%)。其它硅烷如三乙基硅烷、三異丙基硅烷和叔丁基二甲基硅烷,也都可以兼容,分別得到產物16-18,但產率降低(29-38%),這可能是由于較高的Si-H BDEs所致。為了解決這一問題,作者對不同的HAT催化劑進行了考察,結果表明,在35 ℃時,奎寧環-3-乙酸酯對烷基硅烷有較好的作用,使產率略有提高(16-18,38%~47%)。接下來,作者探討了α,β-不飽和酯的范圍。2-甲基丙烯酸芐酯具有良好的適應性(19,58%),如預期的那樣,2-甲基丙烯酸叔丁酯和丁酯在此反應中表現出相似的反應性(20和21)。此外,含有大位阻基團的底物也具有良好的耐受性(22-26,40-74%)。其他雜環芳基烯烴也能以中等收率(27-29)成功轉化為預期產物。在優化的反應條件下,2-丙烯基硼酸酯也能反應,得到相應的產物(30,68%)。但烯烴的來源范圍僅限于1,1-二取代烯烴,單取代烯烴和α,β-不飽和酮的不能反應。為了進一步證明該方法的合成用途,作者測試了幾種含有生物相關單元的更復雜的烯烴底物,包括二丙酮-D-果糖(31)、二丙酮-D-呋喃糖(32)和甾體衍生物(33和34)的糖骨架,它們都適用于該反應,并以較好的收率得到了所需產物。1 mmol規模的反應,得到孕烯醇酮衍生物34,收率60%,這些結果表明,該方法對合成過程中的后期功能化具有一定價值。
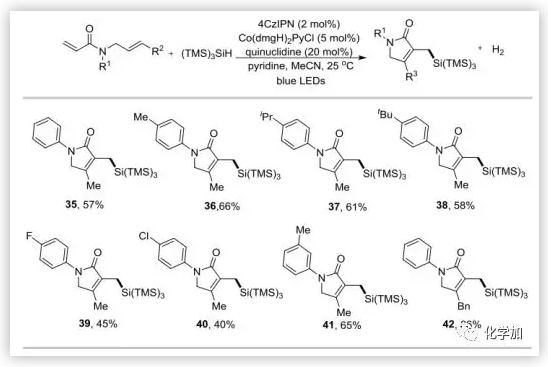
圖4. 脫氫硅化并5-exo-trig環化(圖片來源:Angew. Chem. Int. Ed.)
在此三催化體系中,標準反應條件下,自由基5-exo-trig環化反應可形成5元α,β-不飽和γ-內酰胺(圖4)。首先,作者研究了一系列N-烯丙基-N-芳基丙烯酰胺類化合物,其在芳香環上具有吸電子和給電子取代基的底物都能反應良好。給電子基如甲基(36,41),異丙基(37)和叔丁基(38),產率較高(58-66%)。然而,N-芐基和N-環己基丙烯酰胺等非共軛底物無法得到所需的產物,這可能是由于5-exo-trig環化速率較低所致。用肉桂基代替烯丙基會使產率升高,相應產物為42,收率為86%。
為驗證該工藝的實用性,作者進行了克級規模實驗,得到了相應的烯丙基硅烷1,產率72%。作者還進行了一系列機理實驗,以了解脫氫硅化過程。在2當量自由基清除劑TEMPO的存在下,1的形成被完全抑制,氣相色譜檢測不到H2,這意味著反應是一個自由基過程。當使用N-甲基-N-苯基丙烯酰胺時,未檢測到相應的乙烯基硅烷產物43,表明該反應具有較高的區域選擇性。此外,N-甲基-N-苯基乙基丙烯酰胺也與此反應相容,只得到Z異構體產物。通過分子間競爭同位素效應實驗確定了動力學同位素效應(KIE)值為2.8,表明甲基C-H鍵斷裂可能是該反應中的一個動力學相關步驟。隨后進行了發光淬滅研究,如Stern-Volmer圖所示,Co(dmgH)2PyCl具有更大的淬滅程度,并表現出對激發態4 CzIPN*單電子氧化的動力學偏好。為了揭示自由基的機理,作者設計了電子順磁共振(EPR)實驗,觀察了DMPO作為自旋捕獲劑對自由基中間體的俘獲。EPR信號清楚地指示了自旋加合物的形成,可以得出結論,硅自由基對N-甲基-N-苯基甲基丙烯酰胺中加成后,反應過程中產生了碳中心的自由基。

圖5. 克級規模實驗及機理研究(圖片來源:Angew. Chem. Int. Ed.)
基于上述研究和早期報道,作者提出了一種可能的反應機制,如圖6所示,基態光催化劑4CzIPN在可見光照射下產生激發態光催化劑4CzIPN*,被Co(dmgH)2PyCl 催化劑A氧化生成Co(Ⅱ)物種B。隨著光催化循環的完成,生成的氧化性4CzlPN+物種氧化奎尼丁生成奎尼丁自由基陽離子。高親電性的奎尼丁自由基陽離子選擇性地從TTMSS的氫鍵中攫取氫原子,產生相應的硅自由基。隨后硅自由基對缺電子的烯烴加成,形成以碳中心的自由基中間體。同時,Co(II)物種B可以接受自由基得到加合物C,在輻射下Co-C鍵的斷裂和隨后的β-H的消除得到最終的烯丙基硅烷和氫鈷D,后者可以與另一個質子反應釋放H2。
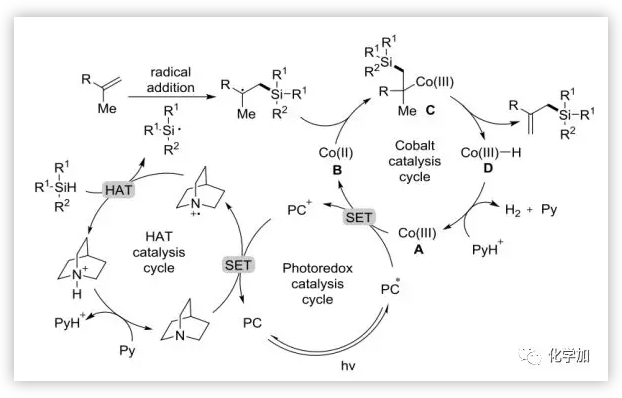
圖6. 可能的反應機理(圖片來源:Angew. Chem. Int. Ed.)
總結:蘭州大學許鵬飛教授課題組開發了光氧化還原催化、氫原子轉移和鈷催化協同合成烯丙基硅烷的方法。該脫氫硅化反應具有區域選擇性高、官能團耐受性好、底物范圍寬、反應條件溫和等特點。此外,這種無氧化劑體系提供了一種比傳統催化更清潔、更有效的方法,不需要使用當量或過量氧化劑。而且,該反應已經成功地應用于在許多生物活性分子骨架中引入硅基團,在有機合成和藥物研發中具有重要應用價值。
撰稿人:詩路化語
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn