



過(guò)渡金屬催化烯烴的雙功能化已成為快速獲得有價(jià)值復(fù)雜分子的基本策略,電子無(wú)偏烯烴的區(qū)域選擇性是這一領(lǐng)域的一大挑戰(zhàn)。化學(xué)家們?yōu)榱私鉀Q這個(gè)問(wèn)題,設(shè)計(jì)了分子內(nèi)體系,或者在烯烴底物上引入配位基團(tuán)。相比之下,完全由催化劑控制的三組分轉(zhuǎn)化仍未得到充分研究。
烯烴的烷基化硼化反應(yīng)在構(gòu)建C(sp3)-C(sp3)化學(xué)鍵的同時(shí)引入了硼基團(tuán),為后續(xù)的多樣化提供了巨大的機(jī)會(huì),特別是在銅催化方面取得了重大進(jìn)展(圖1a)。例如,Sawamura和Ito課題組分別使用分子內(nèi)策略,合成了具有張力的小環(huán)。Yoshida課題組利用苯乙烯和電子偏置烯烴研究了分子間的反應(yīng)。最近,傅堯課題組發(fā)展了在弱配位基團(tuán)的協(xié)助下,未活化端烯的1,2-和2,1-烷基化硼化反應(yīng)(圖1b)。然而,在沒有配位基團(tuán)的情況下,未活化烯烴的區(qū)域選擇性烷基化硼化仍然是一大挑戰(zhàn)。近日,武漢大學(xué)高等研究院陰國(guó)印課題組報(bào)道了無(wú)配位基團(tuán)的鎳催化電子無(wú)偏末端烯烴的1,1-烷基化硼化反應(yīng),以高效和高選擇性的方式得到二官能化產(chǎn)物(圖1c)。在非常溫和的條件下,可利用廉價(jià)硼試劑,從容易獲得的末端烯烴和芐基/烯丙基鹵化物合成有用的二級(jí)脂肪族硼酸酯。
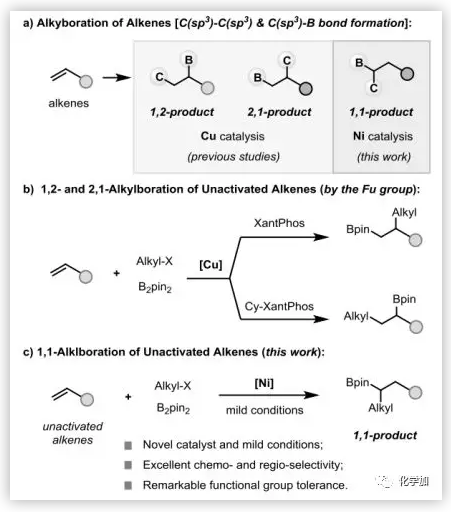
圖1. 過(guò)渡金屬催化的烯烴烷基化硼化反應(yīng)(圖片來(lái)源:Angew. Chem. Int. Ed.)
在銅催化的烷基化硼化反應(yīng)中,從烯烴遷移插入到Cu-B鍵和隨后的鍵形成中產(chǎn)生的瞬時(shí)烷基-Cu中間體主要受益于d10金屬難以進(jìn)行β-H消除。由于一直致力于鎳催化的研究,特別是在鎳催化烯烴遷移芳基化硼化成功后(Angew. Chem. Int. Ed. 2019, 58, 4612-4616),陰國(guó)印課題組推測(cè)如果用鎳代替銅催化劑,快速的β-H消除和遷移插入將生成穩(wěn)定的R-CH(Bpin)Ni(II)物種,隨后與烷基親電試劑形成C(sp3)-C(sp3)鍵,將得到1,1-烷基化硼化產(chǎn)物。
作者首先以端烯1a、芐溴2a和雙(頻哪醇)二硼(B2pin2,3)的三組分反應(yīng)為模型反應(yīng),對(duì)反應(yīng)條件進(jìn)行了考察。如圖2所示,許多在鎳催化中常用的配體都沒有或僅得到了痕量的目標(biāo)產(chǎn)物4a。當(dāng)采用不尋常的吡啶基酰胺L8時(shí),1,1-烷基化硼化產(chǎn)物4a的收率為69%,進(jìn)一步優(yōu)化能使產(chǎn)率提高到91%(L9)。L9和L10的對(duì)比表明,吡啶環(huán)氮原子鄰位的甲基取代基是非常重要的。用L9制備了一種友好、空氣穩(wěn)定的鎳配合物,也得到了類似的分離產(chǎn)率。
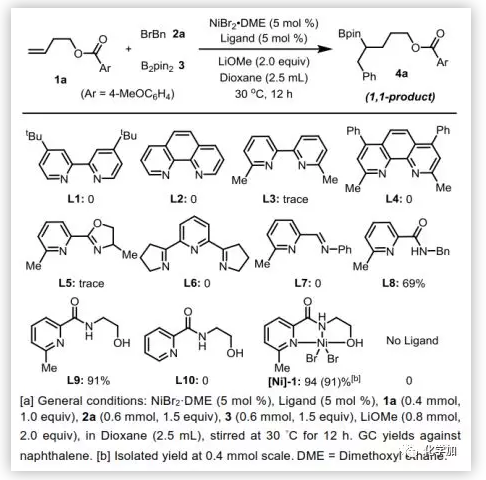
圖2. 反應(yīng)條件篩選(圖片來(lái)源:Angew. Chem. Int. Ed.)
有了最佳反應(yīng)條件,作者對(duì)這種鎳催化反應(yīng)的底物范圍進(jìn)行了考察。如圖3所示,含有多種官能團(tuán)包括酯、醚、酮、酰胺、氰基、醇、對(duì)甲苯磺酸酯、環(huán)氧以及官能化的噻吩、吡咯和吲哚的未活化端烯,均能成功地轉(zhuǎn)化成相應(yīng)的芳基硼化產(chǎn)物,產(chǎn)率良好至優(yōu)秀,且具有優(yōu)異的區(qū)域選擇性(rr>20:1)。以1-庚烯(4b)為原料,合成了1,1-烷基化硼化產(chǎn)物,表明區(qū)域選擇性受催化劑而不是配位基團(tuán)的控制。6-溴己烯(4n)的反應(yīng)中,沒有生成環(huán)化產(chǎn)物。高烯丙基溴的雙鍵也能以良好的收率得到烷基化硼化產(chǎn)物(4e),此外,含有多個(gè)雙鍵的底物中,與單取代烯烴(4s-4v)的選擇性反應(yīng)表明該反應(yīng)在不同類型的雙鍵間具有良好的化學(xué)選擇性。為了進(jìn)一步證明該方法具有良好的相容性,作者還合成了具有生物活性的復(fù)雜分子(4w和4x)。值得注意的是,α,β-不飽和酮在鎳催化體系(4w)中也具有良好的耐受性。
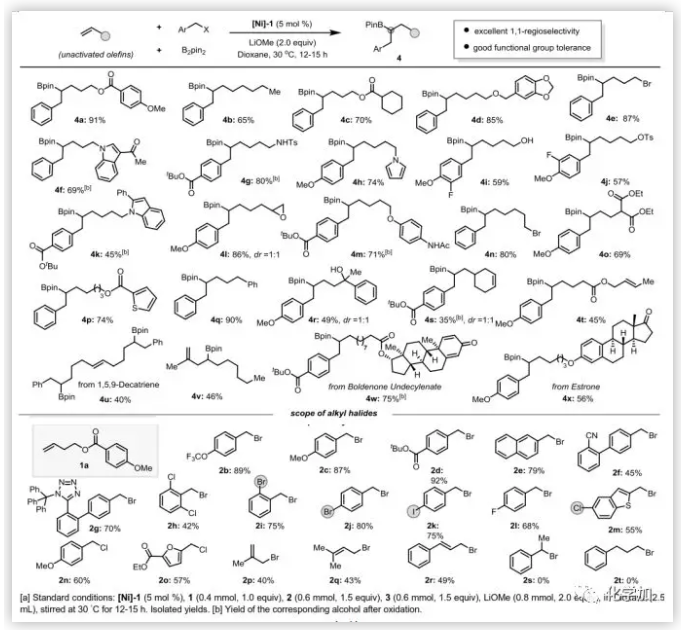
圖3. 底物擴(kuò)展(圖片來(lái)源:Angew. Chem. Int. Ed.)
為了進(jìn)一步評(píng)估這些催化條件的普適性,作者對(duì)一系列取代的芐基溴化物進(jìn)行了研究,富電子取代基和缺電子取代基對(duì)反應(yīng)活性影響不大。在這種溫和的鎳催化條件下,芳基氯、溴甚至碘化物都具有良好的耐受性,為進(jìn)一步的交叉偶聯(lián)做好了準(zhǔn)備。此外,雜環(huán)芐基溴化物和芐基氯化物也是適宜的底物(2m-2o)。烯丙基溴代物雖然比芐基鹵化物的活性稍低,但在相同的反應(yīng)條件下也能生成相應(yīng)的高烯丙基硼酸酯,具有優(yōu)異的1,1-區(qū)域選擇性(2p-2r)。但在這些反應(yīng)條件下,二級(jí)芐基溴代物(2s)和未活的化烷基溴化物(2t)不能得到產(chǎn)物。
除了脂肪族烯烴外,在標(biāo)準(zhǔn)條件下,各種芳基乙烯也可以進(jìn)行烷基化硼化(圖4),但在這些反應(yīng)中只分離出1,2-產(chǎn)物,和Yoshida的銅催化體系結(jié)果一致。這可能是由于芐基鎳中間體的穩(wěn)定性所致。
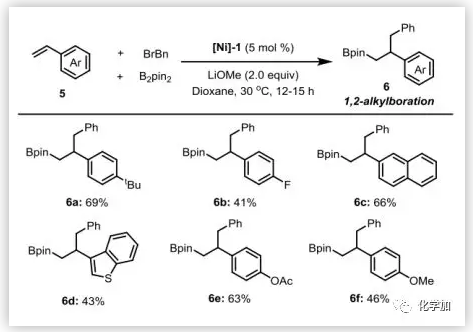
圖4. 乙烯基芳烴的反應(yīng)(圖片來(lái)源:Angew. Chem. Int. Ed.)
為了深入了解該體系的區(qū)域選擇性,如圖5所示,作者對(duì)烯丙基苯和其他幾個(gè)烯丙基取代官能團(tuán)進(jìn)行了研究。烯丙基苯的反應(yīng)中,1,1-產(chǎn)物7仍占主導(dǎo)地位,其區(qū)域異構(gòu)比為6:1。作者進(jìn)一步探討了酯、酰胺和氰基的α-位與硼的α-位之間形成鍵的能力,發(fā)現(xiàn)這三種反應(yīng)都以良好的選擇性得到了1,1-雙官能化產(chǎn)物。這表明良好的區(qū)域選擇性是由新的催化劑決定的。
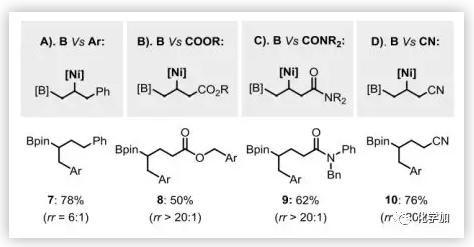
圖5. 區(qū)域選擇性的研究(圖片來(lái)源:Angew. Chem. Int. Ed.)
為了進(jìn)一步探索1,1-烷基化硼化反應(yīng)的潛在范圍,作者還使用了氣體乙烯。如圖6a所示,在氣球壓力下,當(dāng)催化劑負(fù)載量為1 mol%時(shí),在10 mmol的范圍內(nèi),能以61%的收率得到產(chǎn)物11。
最后,作者進(jìn)行了一系列實(shí)驗(yàn)來(lái)闡明這一轉(zhuǎn)化的機(jī)制。首先,用電子順磁共振(EPR)技術(shù)對(duì)反應(yīng)進(jìn)行監(jiān)測(cè)時(shí),未檢測(cè)到任何信號(hào),表明催化劑的靜態(tài)為Ni(0)或Ni(Ⅱ)。在最佳反應(yīng)條件下,1,1-二硼化合物與2a反應(yīng)中未觀察到Suzuki-Miyaura交叉偶聯(lián)產(chǎn)物,這排除了1,1-二硼化合物12作為該烷基化反應(yīng)的中間體的可能性。此外,作者還制備了一種末端氘標(biāo)記的烯烴[d]-1a,并在反應(yīng)中進(jìn)行了考察。產(chǎn)物([d]-4a)的產(chǎn)率為90%,D-原子遷移到β-位的產(chǎn)率為53%。此外,在1a的反應(yīng)中加入乙烯基硼酸酯13,對(duì)反應(yīng)效率沒有影響,也沒有檢測(cè)到氫烷基化產(chǎn)物(14)的形成。這表明,鎳遷移參與了這一轉(zhuǎn)化,在遷移過(guò)程中,鎳氫物種與中間產(chǎn)物不分離。據(jù)此,作者提出了1,2-鎳遷移的催化循環(huán)。如圖6e所示,該反應(yīng)是由Ni(II)物種(I)啟動(dòng)的,它與B2pin2進(jìn)行轉(zhuǎn)金屬化,生成Ni(II)-Bpin物種(II)。隨后烯烴遷移插入生成烷基鎳(II)中間體(III)。β-H消除得到鎳配合物IV,快速遷移插入后得到一個(gè)新的穩(wěn)定的烷基Ni(II)中間體(V),它與活化的烷基鹵化物(2)反應(yīng),產(chǎn)生1,1-雙功能化產(chǎn)物(4)。中間體V與烷基鹵化物的反應(yīng)可能涉及自由基鏈過(guò)程,但在此階段還不能排除另一種可能涉及雙鎳的轉(zhuǎn)金屬化的可能性。
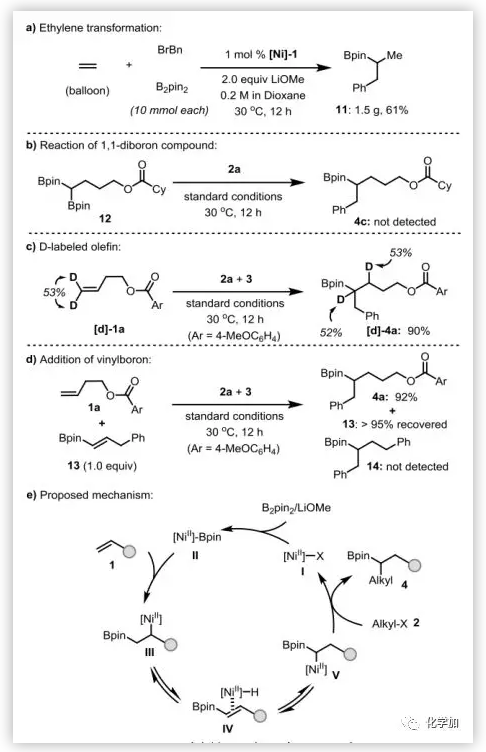
圖6. 乙烯的反應(yīng)及機(jī)理研究(圖片來(lái)源:Angew. Chem. Int. Ed.)
總結(jié):武漢大學(xué)高等研究院陰國(guó)印課題組采用一種不尋常的吡啶酰胺配體,開發(fā)了首例鎳催化烯烴的區(qū)域選擇性1,1-烷基化硼化反應(yīng)。在非常溫和的條件下,以易得的端烯、芐基或烯丙基鹵化物和B2pin2為原料,有效地合成了一系列二級(jí)烷基硼化合物。更重要的是,這種反應(yīng)表現(xiàn)出了極好的區(qū)域選擇性和廣泛的官能團(tuán)相容性,這將大大促進(jìn)烯烴的轉(zhuǎn)化和烷基硼化物的合成,在有機(jī)合成領(lǐng)域具有重要應(yīng)用價(jià)值。
撰稿人:詩(shī)路化語(yǔ)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn