



本文經(jīng)“藥明康德”微信公眾號授權(quán)轉(zhuǎn)載
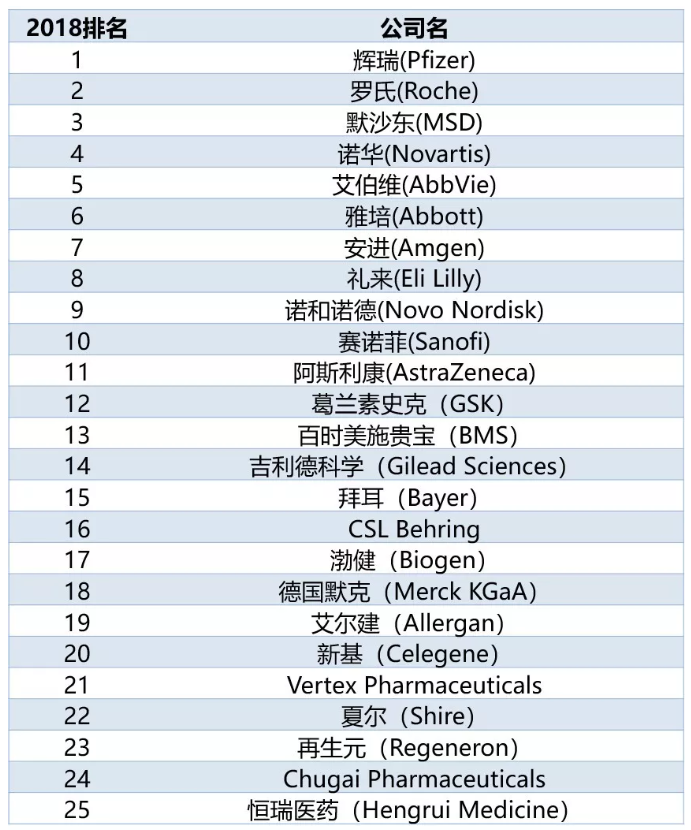
▲數(shù)據(jù)來源:GlobalData 制圖:醫(yī)藥觀瀾
25:恒瑞醫(yī)藥
根據(jù)恒瑞醫(yī)藥2018年年報,該公司在該年度內(nèi)取得創(chuàng)新藥制劑生產(chǎn)批件2個,仿制藥制劑生產(chǎn)批件7個;取得創(chuàng)新藥臨床批件16個。其中SHR0302片、INS068注射液、SHR0410注射液3個產(chǎn)品獲準(zhǔn)在海外開展臨床試驗。目前,恒瑞醫(yī)藥的創(chuàng)新藥艾瑞昔布、阿帕替尼、硫培非格司亭和吡咯替尼均已在國內(nèi)獲批上市。其中,2018年上市的馬來酸吡咯替尼,是基于2期臨床研究獲得中國國家藥監(jiān)局批準(zhǔn)上市的實體瘤新藥,該產(chǎn)品上市為中國HER2陽性晚期乳腺癌患者帶來新的治療選擇。
據(jù)了解,恒瑞醫(yī)藥目前有56個創(chuàng)新藥正在臨床開發(fā)中。其中自主研發(fā)的PD-1抗體卡瑞利珠單抗已經(jīng)申報上市;近期卡瑞利珠單抗聯(lián)合甲磺酸阿帕替尼一線治療肝癌的國際多中心3期臨床試驗,正在美國、歐洲和中國同步開展。
24:Chugai Pharmaceuticals
根據(jù)Chugai官網(wǎng),今年第一個季度該公司取得了不錯的成績。該公司開發(fā)的Actemra靜脈輸液獲得日本厚生勞動省(MHLW)批準(zhǔn)用于細(xì)胞因子釋放綜合征的額外適應(yīng)癥和劑量。抗CD20單克隆抗體Rituxan被MHLW批準(zhǔn)用于CD20陽性的慢性淋巴性白血病。A型血友病治療藥物Hemlibra的上市申請獲得歐盟委員會批準(zhǔn)。
今年3月,該公司脊髓性肌萎縮癥新藥Risdiplam在日本獲得了孤兒藥資格。本月,該公司公布了IL-31受體A靶向阻斷抗體nemolizumab在一項特應(yīng)性皮炎的3期研究中取得陽性結(jié)果。此外,該公司還向MHLW申請ROS1/TRK抑制劑entrectinib治療ROS1融合陽性非小細(xì)胞肺癌的新藥申請。
23:再生元(Regeneron)
2018年9月,再生元宣布FDA批準(zhǔn)了其PD-1抑制劑Libtayo(cemiplimab-rwlc)上市,用于轉(zhuǎn)移性/局部晚期皮膚鱗狀細(xì)胞癌。此前,cemiplimab獲得FDA優(yōu)先審評資格,僅用151天便獲批上市。根據(jù)再生元2018年年報,該公司的血管新生抑制劑Eylea(aflibercept)注射液正在注冊申報階段,主要用于糖尿病黃斑水腫、分支視網(wǎng)膜靜脈阻塞和近視脈絡(luò)膜新生血管(亞洲)。
今年3月,F(xiàn)DA批準(zhǔn)了單抗藥Dupixent(dupilumab),用于治療青少年中度至重度特應(yīng)性皮炎。同期,該公司的PCSK9抑制劑Praluent(alirocumab)獲得歐盟批準(zhǔn)用于降低已確診心血管疾病患者心血管事件的風(fēng)險。臨床開發(fā)管線上的10個產(chǎn)品中,膽固醇新藥alirocumab(PCSK9抗體)和類風(fēng)濕關(guān)節(jié)炎新藥sarilumab(IL-6R抗體)處于臨床3期;IL-4R抗體dupilumab、IL-6R抗體sarilumab、NGF抗體fasinumab、GDF8抗體REGN1033均處于臨床2期;另外還有三款抗腫瘤新藥處于臨床1期。與此同時,再生元還宣布與Alnylam合作,共同開發(fā)RNAi治療藥物。
22:夏爾(Shire)
武田收購夏爾的計劃已在今年1月完成,現(xiàn)在,夏爾已成為武田的一部分。夏爾的研發(fā)方向主要集中在血液學(xué)、免疫學(xué)、遺傳病、神經(jīng)科學(xué)和內(nèi)科醫(yī)學(xué)等核心罕見病領(lǐng)域中,開發(fā)best-in-class的療法,同時擴(kuò)展眼科和腫瘤治療領(lǐng)域。根據(jù)夏爾2018年年報,去年該公司的遺傳性血管性水腫(HAE)新藥Takhzyro已獲得美國、歐洲和加拿大的上市批準(zhǔn),慢性特發(fā)性便秘(CIC)新藥Motegrity在美國獲批上市。
21:Vertex Pharmaceuticals
囊性纖維化的新藥開發(fā)是Vertex的研發(fā)重點。此外,Vertex還有十多個正在進(jìn)行的研究項目,重點關(guān)注其他嚴(yán)重疾病的潛在機(jī)制。去年底,Vertex宣布?xì)W洲委員會批準(zhǔn)Kalydeco(ivacaftor)治療某些CFTR基因突變的囊性纖維化的患者。今年,Vertex的Orkambi(lumacaftor/ivacaftor)和Symdeko(tezacaftor/ivacaftor和ivacaftor)先后在歐洲和澳大利亞獲批上市。
早些時候,Vertex宣布其囊性纖維化三聯(lián)用藥的兩個3期試驗均達(dá)到肺功能改善的主要終點。該公司還宣布tezacaftor/Ivacaftor組合用藥的3期臨床結(jié)果支持其在歐洲的上市申報。另外,Vertex與CRISPR Therapeutics共同開發(fā)的用于治療β地中海貧血癥的新藥CTX001還獲得FDA頒發(fā)的快速通道資格。
20:新基(Celegene)
4月12日,新基和百時美施貴寶(BMS)股東投票批準(zhǔn)了兩家公司于2019年1月3日宣布的合并,預(yù)計將在2019年第三季度完成交易。根據(jù)新基2018年年報,該公司預(yù)計在2020年將上市5款產(chǎn)品。其中,fedratinib應(yīng)用于骨髓纖維化的新藥申請已經(jīng)在去年遞交至FDA,并在今年3月獲得優(yōu)先審評資格。Revlimid與利妥昔單抗(AUGMENT試驗)用于治療患有復(fù)發(fā)和/或難治性惰性非霍奇金淋巴瘤(NHL)患者的補(bǔ)充申請(sNDA)也遞交至FDA,預(yù)計會在今年下半年完成審評。同時,新基還啟動了不少于5項處于不同階段的臨床試驗。不久前,新基公布了Abraxane聯(lián)合療法在轉(zhuǎn)移性三陰性乳腺癌和胰腺癌上的最新進(jìn)展。
19:艾爾建(Allergan)
今年,艾爾建的新藥Avycaz獲得FDA批準(zhǔn)用于兒科患者,Avycaz是一種固定劑量復(fù)方制劑,由ceftazidime(頭孢他啶)和avibactam組成。同時,F(xiàn)DA接受ubrogepant用于急性偏頭痛治療的新藥申請,以及擴(kuò)大Botox(onabotulinumtoxinA)適應(yīng)癥,用于治療患有上肢和下肢痙攣的兒科患者(2歲及以上)。根據(jù)艾爾建2018年年報,艾爾建將在今年繼續(xù)推進(jìn)幾個關(guān)鍵項目的臨床開發(fā),包括用于雙相抑郁癥的cariprazine,用于偏頭痛的ubrogepant,以及用于青光眼的bimatoprost SR。
18:德國默克(Merck KGaA)
2018年,德國默克開發(fā)的抗癌新藥avelumab(Bavencio?)被澳大利亞和巴西在內(nèi)的幾個國家批準(zhǔn)用于Merkel細(xì)胞癌(MCC),在以色列被批用于MCC和尿路上皮癌(UC),同時還在加拿大獲批用于UC。目前,avelumab已在全球46個國家已獲得上市批準(zhǔn)。去年,德國默克還公布了關(guān)鍵的3期JAVELIN Renal 101研究的陽性結(jié)果。根據(jù)德國默克2018年年報,該公司圍繞avelumab的臨床開發(fā)計劃JAVELIN包括30多個,涉及超過15種不同腫瘤類型的9000多名患者。同時,該公司還與Leap Therapeutics、輝瑞等公司達(dá)成新合作。
德國默克在免疫腫瘤領(lǐng)域的另外兩項產(chǎn)品也取得了幾個重要的里程碑,分別是研究性口服MET抑制劑tepotinib和研究性雙功能免疫療法M7824。其中,tepotinib在日本獲得了快速通道資格,M7824分別在美國和歐洲獲得了孤兒藥資格。在多發(fā)性硬化癥(MS)方面,德國默克在去年重新提交了cladribine作為復(fù)發(fā)性MS潛在治療方案的NDA申請。2018年,cladribine以商品名Mavenclad在11個國家獲批。截至目前,該藥已在包括加拿大、澳大利亞在內(nèi)的40多個國家獲批上市。
17:渤健(Biogen)
2019年,渤健雖然在阿茲海默病治療領(lǐng)域臨床上暫時失利,但近兩年其研發(fā)管線上仍然有很多收獲。2018年3月,公司先是收購了輝瑞公司的一款first-in-class新藥PF-04958242。這是一款處于臨床階段的即用型AMPA受體增強(qiáng)劑,用于治療精神分裂癥相關(guān)的認(rèn)知障礙(CIAS)。同年6月,渤健又宣布與TMS簽署了一項獨家選擇協(xié)議,收購其用于急性中風(fēng)的新藥TMS-007和備用化合物。2019年3月,渤健宣布收購基因療法公司Nightstar Therapeutics,獲得了后者的基因療法管線。進(jìn)入2019年,渤健在中國也迎來好消息,其新藥Spinraza在中國獲批上市,用于治療脊髓性肌萎縮癥(spinal muscular atrophy,SMA)。
16:CSL Behring
CSL Behring的研發(fā)主要聚焦血漿療法和重組蛋白,擁有血友病、免疫缺陷疾病以及流感等治療領(lǐng)域的豐富管線,如用于遺傳性血管性水腫病癥的Haegarda和用于B型血友病患者在出血期止血的Idelvion是其代表產(chǎn)品。值得一提的是,2018年,CSL公司的皮下免疫球蛋白產(chǎn)品Hizentra擴(kuò)展了新的適應(yīng)癥——慢性炎癥性脫髓鞘性多發(fā)性神經(jīng)炎(CIDP)。該年3月,Hizentra用于治療CIDP的適應(yīng)癥獲得了歐洲委員會(EC)的上市許可,并于同月在美國獲得批準(zhǔn)。
15. 拜耳(Bayer)

拜耳公司治療A型血友病的新藥Jivi去年8月獲得FDA批準(zhǔn)上市,這是一款長效重組凝血因子VIII。通過對凝血因子VIII重組蛋白進(jìn)行聚乙二醇修飾(PEGlaytion),讓它的半衰期延長到17.9個小時,從而讓患者在減少注射次數(shù)的情況下仍然能夠維持正常凝血功能。在中國拜耳的非修飾型重組凝血因子VIII(商品名為科躍奇)也在去年獲批之后,今年正式上市,有望為A型血友病患者造福。
拜耳開發(fā)“不限癌種”抗癌藥的合作伙伴Loxo Oncology公司雖然被禮來公司收購,但是拜耳獲得了獲批TRK抑制劑Vitrakvi和下一代TRK抑制劑BAY 2731954(LOXO-195)的研發(fā)和推廣權(quán)益。這兩款“廣譜”抗癌藥在治療攜帶NTRK基因融合的實體瘤患者方面顯示出優(yōu)異的療效。而且BAY 2731954還能夠治療對Vitrakvi產(chǎn)生抗性的實體瘤患者。今年,Vitrakvi也已經(jīng)在中國申報臨床試驗,并且獲得臨床默示許可,有望早日為中國癌癥患者造福。
14. 吉利德科學(xué)(Gilead Sciences)

吉利德科學(xué)公司的主要研發(fā)領(lǐng)域包括非酒精性脂肪性肝炎(NASH),艾滋病,炎癥性疾病和癌癥。在治療NASH方面,雖然吉利德科學(xué)靶向細(xì)胞凋亡信號調(diào)節(jié)激酶1(ASK1)的selonsertib作為單藥在3期臨床試驗中表現(xiàn)不佳,但是吉利德科學(xué)并沒有放棄研發(fā)NASH療法的努力。它已經(jīng)與諾和諾德達(dá)成合作,探索聯(lián)合索馬魯肽(semaglutide)治療NASH的組合療法。同時它還與使用機(jī)器學(xué)習(xí)加速藥物研發(fā)的新銳公司insitro合作,使用機(jī)器學(xué)習(xí)發(fā)現(xiàn)治療NASH的新靶標(biāo)。
在預(yù)防艾滋病方面,吉利德科學(xué)使用優(yōu)先審評券,向FDA遞交了使用該公司的新一代艾滋病組合療法Descovy作為暴露前預(yù)防療法(PrEP)的監(jiān)管申請,致力于盡快將這款新藥交到有風(fēng)險受到HIV病毒感染的人群手中。
吉利德科學(xué)與Galapagos公司聯(lián)合開發(fā)的JAK1抑制劑filgotinib在兩項臨床試驗中達(dá)到主要終點。這款治療類風(fēng)濕性關(guān)節(jié)炎的潛在重磅新藥有望在今年年底之前遞交新藥申請。
13. 百時美施貴寶(BMS)

百時美施貴寶公司今年的重大舉措是斥資約740億美元收購新基(Celgene)公司及其豐富的藥物研發(fā)管線。日前,BMS和新基的股東投票批準(zhǔn)了這一收購,這一交易有望在今年第三季度完成。
除此以外,BMS與艾伯維(AbbVie)公司聯(lián)合開發(fā)的Empliciti(elotuzumab)去年11月獲得FDA批準(zhǔn)擴(kuò)展適應(yīng)癥,作為組合療法的一員治療特定復(fù)發(fā)/難治性多發(fā)性骨髓瘤(MM)患者。Empliciti是一款靶向SLAMF7糖蛋白的創(chuàng)新免疫刺激抗體,它不但可以激活先天殺傷細(xì)胞,還可以標(biāo)注腫瘤細(xì)胞,介導(dǎo)基于抗體的細(xì)胞毒性作用。
在癌癥領(lǐng)域,BMS的免疫檢查點抑制劑Opdivo(抗PD-1療法)是多項組合療法的基石。BMS也在與多家公司合作,擴(kuò)展基于Opdivo的組合療法,其中包括Nektar Therapeutics和Compugen。
12. 葛蘭素史克(GSK)

葛蘭素史克在該公司首席科學(xué)官Hal Barron博士的領(lǐng)導(dǎo)下,將開發(fā)癌癥療法作為研發(fā)的重心之一。去年12月該公司與TESARO達(dá)成協(xié)議,以51億美元的金額收購TESARO。這項交易已于今年初完成。GSK收獲的重要療法包括TESARO公司開發(fā)的PARP抑制劑Zejula(niraparib)。這款“合成致死”原理治療攜帶BCRA基因突變癌癥的療法已經(jīng)在治療具有同源重組缺陷的癌癥方面顯示出潛力,GSK將開展臨床試驗進(jìn)一步拓寬niraparib的適用范圍。
GSK還與德國默克(Merck KGaA)達(dá)成協(xié)議,共同開發(fā)德國默克的雙功能免疫療法M7824。這款療法是一種“first-in-class”同時靶向TGF-β和PD-L1信號通路的融合蛋白,在2線治療非小細(xì)胞肺癌(NSCLC)的2期臨床試驗中已經(jīng)表現(xiàn)出卓越療效。
GSK自主開發(fā)的靶向B細(xì)胞成熟抗原(BCMA)的抗體偶聯(lián)療法GSK2857916也在治療MM患者的臨床試驗中表現(xiàn)出積極結(jié)果,GSK公司致力于迅速推送這款在研新藥的臨床開發(fā),今年預(yù)計將開展4項關(guān)鍵性臨床試驗,治療不同類型的MM患者。
11. 阿斯利康(AstraZeneca)

阿斯利康在2018年進(jìn)行了公司結(jié)構(gòu)重組,將MedImmune公司并入阿斯利康。中國地區(qū)始終是阿斯利康公司發(fā)展的重心之一,中國地區(qū)2018年全年增長率達(dá)到25%,遠(yuǎn)遠(yuǎn)超過了阿斯利康在其它新興市場的發(fā)展速度。而在最新公布的2019年第一季度報告中,中國地區(qū)的2019第一季度增長率更達(dá)到28%的高水平。該公司于FirbroGen公司合作開發(fā)的羅沙司他(roxadustat,商品名愛瑞卓)是在中國首先獲批上市的一款新藥。這款治療透析依賴性慢性腎病患者的腎性貧血的“first-in-class”新藥目前還沒有在其它任何國家上市。
今年,阿斯利康還與第一三共(Daiichi-Sankyo)達(dá)成合作,共同開發(fā)創(chuàng)新靶向HER2的抗體偶聯(lián)藥物(ADC)trastuzumab deruxtecan(DS-8201)。這款創(chuàng)新ADC在靶向HER2的單克隆抗體上連接和更多的細(xì)胞毒性藥物,而且對HER2表達(dá)量低的腫瘤也表現(xiàn)出良好的療效。它將成為阿斯利康治療乳腺癌療法的基石之一,預(yù)計在今年下半年將第一次遞交監(jiān)管申請。
10. 賽諾菲(Sanofi)

賽諾菲公司在治療專科疾病的“first-in-class”療法研發(fā)方面取得了顯著進(jìn)展。該公司開發(fā)的Cablivi(caplacizumab)今年2月獲得FDA批準(zhǔn)上市,用于治療獲得性血栓性血小板減少性紫癜(aTTP)的成人患者。這款新藥是賽諾菲旗下Ablynx公司開發(fā)的一種二價抗血管性血友病因子(vWF)的納米抗體(Nanobody)。它能夠阻斷超大vWF多聚體與血小板的相互作用,從而防止血小板聚集和微小血凝塊的形成,避免血栓發(fā)生,同時治療aTTP患者的血小板減少癥、組織缺血和器官功能失常。根據(jù)賽諾菲今日發(fā)布的季報,這款新藥在今年4月正式在美國推出。
而與再生元(Regeneron)聯(lián)合開發(fā)的抗PD-1療法Libtayo(cemiplimab-rwlc)獲得FDA批準(zhǔn)治療轉(zhuǎn)移性皮膚鱗狀細(xì)胞癌(CSCC)或不能接受治愈性手術(shù)或放療的局部晚期CSCC患者。這是FDA批準(zhǔn)的第一例針對晚期CSCC的療法,也是FDA批準(zhǔn)的第三款抗PD-1抗體。今日,歐盟人用醫(yī)藥產(chǎn)品委員會(CHMP)宣布支持Libtayo在歐洲上市,治療CSCC患者。CSCC是世界上最為常見的皮膚癌之一。
9. 諾和諾德( Novo Nordisk)

提到諾和諾德,我們首先想到的可能是該公司開發(fā)的治療糖尿病的多種療法。該公司治療糖尿病的新藥索馬魯肽(semaglutide)是一款胰高血糖樣肽-1(GLP-1)類似物,是一種誘導(dǎo)胰島素分泌的激素。其注射劑型已經(jīng)在2017年獲得批準(zhǔn)治療2型糖尿病。而且諾和諾德還開發(fā)了口服劑型的索馬魯肽,并且在近日向美國FDA遞交了監(jiān)管申請。
這一創(chuàng)新療法不但能夠幫助糖尿病患者控制血糖,而且能夠降低患者主要心血管不良事件的風(fēng)險。它在治療肥胖癥和NASH方面顯示出療效,目前在3期臨床試驗中治療肥胖癥,在2期臨床試驗中治療NASH。這款新藥在諾和諾德與吉利德公司研發(fā)NASH組合療法的合作中也將起到重要作用。
此外,諾和諾德研發(fā)的長效重組凝血因子VIII獲得美國FDA批準(zhǔn)上市,用于治療A型血友病患者。這款名為Esperoct的聚乙二醇化凝血因子VIII的半衰期是標(biāo)準(zhǔn)因子VIII產(chǎn)品的1.6倍。今日,它獲得歐盟CHMP的支持,有望近期在歐盟獲批上市,進(jìn)一步造福更多A型血友病患者。
8. 禮來(Eli Lilly)

禮來公司今年年初宣布將以約80億美元的數(shù)額收購開發(fā)“不限癌種”抗癌療法的Loxo Oncology公司,進(jìn)一步拓寬了該公司的藥物研發(fā)管線。除了收購Loxo Oncology以外,禮來公司還與多家生物醫(yī)藥公司達(dá)成合作協(xié)議,開發(fā)治療多種疾病的創(chuàng)新療法。其中包括:與AC Immune公司達(dá)成合作,開發(fā)抑制tau蛋白聚集的小分子抑制劑,治療阿爾茨海默病和其它神經(jīng)退行性疾病;與陳列平教授創(chuàng)建的NextCure公司合作,開發(fā)創(chuàng)新癌癥免疫療法;與Avidity Biosciences公司合作,利用該公司的抗體偶聯(lián)寡核苷酸(AOC)技術(shù)平臺發(fā)現(xiàn)創(chuàng)新療法。
該公司達(dá)成的合作還包括獲得Hydra Biosciences開發(fā)的臨床前TRPA1拮抗劑,用于治療慢性疼痛;與Aduro Biotech公司合作開發(fā)cGAS-STING信號通路抑制劑,構(gòu)建治療自身免疫疾病和炎癥性疾病的創(chuàng)新免疫調(diào)節(jié)療法。
日前,該公司開發(fā)的重磅藥Taltz(ixekizumab)在治療治療非放射性軸性脊柱關(guān)節(jié)炎(nr-axSpA)的3期臨床試驗中也表現(xiàn)出積極療效。這款已經(jīng)獲批治療銀屑病的IL-17A抑制劑,有望治療多種類型的脊柱關(guān)節(jié)炎患者。
7. 安進(jìn)(Amgen)

安進(jìn)公司開發(fā)的雙特異性抗體技術(shù)平臺為該公司帶來了目前唯一獲批的雙特異性T細(xì)胞接合器(BiTE)Blincyto。雙特異性抗體技術(shù)已經(jīng)成為多家醫(yī)藥公司開發(fā)的重要癌癥免疫療法方向。安進(jìn)公司在這一領(lǐng)域也獲得了積極進(jìn)展。該公司開發(fā)的AMG 420和AMG 330分別靶向BCMA抗原和CD33抗原。它們的一端與腫瘤細(xì)胞表面的抗原相結(jié)合,另一端與T細(xì)胞表面的受體相結(jié)合,從而在腫瘤附近特異性激活T細(xì)胞。在去年美國血液學(xué)會上公布的初步臨床結(jié)果表明,這兩款BiTE分別在治療MM和急性骨髓性白血病患者的臨床試驗中顯示出可喜的療效。
本月初,安進(jìn)和優(yōu)時比公司聯(lián)合開發(fā)的Evenity(romosozumab-aqqg)獲得FDA批準(zhǔn)上市,治療具有高骨折風(fēng)險的絕經(jīng)后婦女的骨質(zhì)疏松癥。這款新藥靶向骨硬化蛋白(sclerostin),是一款同時具有提高骨形成和降低骨吸收雙重作用的構(gòu)建骨質(zhì)療法。
6. 雅培(Abbott Laboratories)

雅培是一家主要開發(fā)醫(yī)療器械的生物醫(yī)藥公司。今年初,該公司開發(fā)的Amplatzer Piccolo 封堵器(occluder)獲得FDA批準(zhǔn)上市,用于治療出現(xiàn)在早產(chǎn)兒或新生兒中的動脈導(dǎo)管未閉(patent ductus arteriosus, PDA)。這是一種先天性心臟畸形。Amplatzer Piccolo封堵器只有不到一粒豌豆大,它是世界上第一款通過微創(chuàng)手術(shù),能夠植入到最小的嬰兒心臟中治療PDA的醫(yī)療器械。
該公司開發(fā)的Mitraclip系統(tǒng)獲得FDA批準(zhǔn)治療具有嚴(yán)重二尖瓣關(guān)閉不全的心衰患者。Mitraclip系統(tǒng)是一款通過微創(chuàng)手術(shù)修復(fù)二尖瓣的療法。根據(jù)雅培的新聞稿,它是第一款獲批治療這類心衰患者的經(jīng)導(dǎo)管二尖瓣介入治療手段。
5. 艾伯維(AbbVie)

艾伯維寄予厚望的抗IL-23抗體Skyrizi本周獲得FDA批準(zhǔn),治療中重度銀屑病患者。這款新藥在清除患者皮膚癥狀方面表現(xiàn)非常優(yōu)異,超過半數(shù)患者皮膚癥狀得到完全清除(PASI 100)。艾伯維公司同時在開展多項臨床試驗,檢驗這款新藥在治療多種炎癥性疾病方面的療效。而該公司開發(fā)的另一款治療炎癥性疾病的在研療法upadacitinib獲得FDA授予的優(yōu)先審評資格,用于治療中重度類風(fēng)濕性關(guān)節(jié)炎。Upadacitinib是一款口服JAK1特異性抑制劑。
在治療血液癌癥方面,艾伯維和楊森公司共同開發(fā)的重磅療法Imbruvica獲得FDA批準(zhǔn),與obinutuzumab聯(lián)用,一線治療初治慢性淋巴性白血病/小淋巴細(xì)胞淋巴瘤(CLL/SLL)患者。這是第一款獲得FDA批準(zhǔn)治療CLL/SLL初治患者的一線非化療組合療法,也是自2013年Imbruvica獲批以來第10次FDA批準(zhǔn),將其適應(yīng)癥擴(kuò)展到6個不同的疾病領(lǐng)域。而該公司和羅氏共同開發(fā)的Venclexta(venetoclax)也獲得了FDA授予的第5個突破性療法認(rèn)定,與obinutuzumab聯(lián)用,治療初治CLL患者。這是一款BCL-2抑制劑。
艾伯維公司還與多家公司達(dá)成研發(fā)合作協(xié)議,開發(fā)創(chuàng)新療法,其中包括與Tenebio公司合作開發(fā)靶向BCMA的雙特異性T細(xì)胞接合器,與Voyager Therapeutics公司合作開發(fā)治療帕金森病等神經(jīng)退行性疾病的創(chuàng)新療法。
4. 諾華(Novartis)

在今年年初發(fā)布的2018年年度報告中,諾華表示2019年至2021年該公司將有超過10款重磅藥物上市。如今2019年已經(jīng)過去了4個月,諾華公司治療多發(fā)性硬化癥(MS)的Mayzent(siponimod)成功獲得FDA批準(zhǔn)上市,成為15年來第一款針對活躍的繼發(fā)進(jìn)展型MS的獲批口服療法。Mayzent通過與淋巴細(xì)胞和中樞神經(jīng)系統(tǒng)膠質(zhì)細(xì)胞表面的S1P5和S1P1受體結(jié)合,抑制淋巴細(xì)胞進(jìn)入MS患者的中樞神經(jīng)系統(tǒng),并且有促進(jìn)髓鞘再生的功能。
該公司開發(fā)的治療1型脊髓性肌萎縮癥(SMA)的基因療法Zolgensma在3期臨床試驗中也獲得了積極的中期結(jié)果。這款基因療法有望在今年5月獲得FDA的批準(zhǔn),它通過AAV病毒載體將表達(dá)運動神經(jīng)元生存蛋白(SMN)的基因?qū)牖颊呒?xì)胞中,可能成為潛在的治愈性療法。
在治療被忽視疾病方面,諾華公司也取得了顯著進(jìn)展,該公司的Egaten(triclabendazole)獲得FDA批準(zhǔn),治療6歲以上片形吸蟲病(fascioliasis)患者。這是目前治療這一疾病的唯一FDA獲批療法,也是世界衛(wèi)生組織(WHO)唯一推薦用于治療片形吸蟲病的療法。
今年四月,諾華公司治療銀屑病的重磅IL17A抑制劑可善挺(司庫奇尤單抗,俗稱“蘇金單抗”)在中國獲批上市,成為首個獲批治療銀屑病的生物制劑。它將開啟中國銀屑病治療的新時代。
3. 默沙東(MSD)

提到默沙東,可能我們都會想到該公司開發(fā)的重磅抗癌藥物Keytruda。這款被稱為“K藥”的抗PD-1療法自問世以來不斷擴(kuò)展適用范圍,凸顯了免疫檢查點抑制劑在治療癌癥方面的卓越療效。
Keytruda在2019年斬獲頗豐,本月11日,它獲得FDA批準(zhǔn)單藥一線治療非小細(xì)胞肺癌患者,患者腫瘤PD-L1表達(dá)腫瘤比例評分(TPS)只要超過1%就可以接受治療。這一批準(zhǔn)大幅度擴(kuò)展了適于適用Keytruda單藥治療的NSCLC患者數(shù)量。而在上周,F(xiàn)DA又批準(zhǔn)Keytruda與Inlyta聯(lián)用,一線治療晚期腎細(xì)胞癌患者。Keytruda在中國大陸也獲批與化療聯(lián)用,一線治療轉(zhuǎn)移性非鱗狀NSCLC,有望為更多中國肺癌患者造福。
醫(yī)藥觀瀾相關(guān)閱讀:群星閃耀的中國免疫療法時代:從Keytruda獲批治療肺癌說起
默沙東公司以Keytruda為基石,正在努力開發(fā)多種免疫組合療法,力圖在擴(kuò)展Keytruda適用范圍的同時,進(jìn)一步提高免疫檢查點抑制劑的治療效果。它也在通過達(dá)成研發(fā)協(xié)議,開發(fā)能夠與免疫檢查點抑制劑產(chǎn)生協(xié)同作用的免疫療法。例如,默沙東近日以3億美元收購了Immune Design公司。
除了癌癥領(lǐng)域,默沙東還布局NASH療法的研發(fā),通過與NGM Biopharmaceuticals的合作囊獲一款即將進(jìn)入2期臨床試驗的NASH在研療法。該公司開發(fā)的創(chuàng)新15價肺炎疫苗也獲得了FDA授予的突破性療法認(rèn)定,能夠覆蓋更多血清型,起到更好的預(yù)防肺炎效果。
2. 羅氏(Roche)

羅氏今年2月斥資43億美元,擬收購明星基因療法公司Spark Therapeutics,顯示了該公司開發(fā)基因療法的決心。
羅氏與旗下的基因泰克公司在新藥研發(fā)方面成績卓越,根據(jù)近日羅氏2019第一季度季報,自2013年以來,羅氏的在研療法總計獲得了26項FDA授予的突破性療法認(rèn)定。在2019年,該公司與艾伯維聯(lián)合開發(fā)的Venclexta第五次獲得突破性療法認(rèn)定,與obinutuzumab聯(lián)用一線治療CLL。而該公司最新一代的靶向HER2的乳腺癌療法Kadcyla也獲得突破性療法認(rèn)定,作為輔助療法治療接受過手術(shù)治療的HER2+早期乳腺癌患者。這是一款靶向HER2的抗體偶聯(lián)藥物。
該公司開發(fā)的抗PD-L1重磅抗癌藥Tecentriq今年獲批結(jié)合化療,一線治療廣泛期小細(xì)胞肺癌(ES-SCLC)。這是20多年來ES-SCLC患者首次獲得新的一線治療選擇。Tecentriq還獲得加速批準(zhǔn),與化療聯(lián)用治療三陰性乳腺癌患者。這是第一款用于治療乳腺癌的免疫組合療法。Tecentriq組合療法今年還有望獲得批準(zhǔn),一線治療轉(zhuǎn)移性非鱗狀NSCLC患者。
1. 輝瑞(Pfizer)

輝瑞公司在2018年進(jìn)行了公司結(jié)構(gòu)的重組。調(diào)整之后,將專注于創(chuàng)新藥,仿制藥和消費者保健三大領(lǐng)域。而在2018年年末,輝瑞和GSK宣布合并消費者保健業(yè)務(wù),建立一家擁有強(qiáng)大標(biāo)志性品牌的全球性消費者保健公司。
在新藥研發(fā)方面,輝瑞與德國默克聯(lián)合開發(fā)的Bavencio/Inlyta組合療法獲得FDA授予的優(yōu)先審評資格,有望今年獲批一線治療腎細(xì)胞癌。這是一款PD-L1抗體和酪氨酸激酶抑制劑構(gòu)成的免疫組合療法。
該公司治療轉(zhuǎn)甲狀腺素蛋白淀粉樣變性心肌病的在研新藥tafamidis的新藥申請也獲得了FDA授予的優(yōu)先審評資格,有望在今年7月獲得批準(zhǔn)。這款小分子口服藥物通過與轉(zhuǎn)甲狀腺素蛋白結(jié)合,提高它的穩(wěn)定性,防止淀粉樣蛋白的形成。
輝瑞與禮來公司聯(lián)合開發(fā)的在研止痛藥tanezumab在治療骨性關(guān)節(jié)炎和中重度慢性腰痛患者的3期試驗中均達(dá)到積極頂線結(jié)果。這是一款靶向神經(jīng)生長因子(NGF)的單克隆抗體。
在仿制藥方面,輝瑞開發(fā)的生物類似藥Trazimera(trastuzumab-qyyp)今年3月獲得了FDA的批準(zhǔn),用于治療HER2陽性乳腺癌和胃癌。這是一款赫賽汀(Herceptin)的生物類似藥,為靶向HER2的單克隆抗體。今年,輝瑞還有三款生物類似藥可能獲得批準(zhǔn)。
GlobalData組織的分析師表明,雖然全球25大醫(yī)藥公司的名次有所變動,但是這些公司的一個特點是它們都對創(chuàng)新研發(fā)進(jìn)行大量的投資。平均來看,25大醫(yī)藥公司研發(fā)投入金額占銷售額的19.5%。而Vertex,新基和再生元公司研發(fā)投入比例達(dá)到46.5%、37.1%和32.6%。
研發(fā)創(chuàng)新是開發(fā)治療疾病的新療法的引擎,我們期待諸多醫(yī)藥企業(yè)能夠不斷推動創(chuàng)新,積極進(jìn)取,為全球患者帶來更多新藥好藥!
參考資料:
[1] The top 25 pharmaceutical companies by market cap. Retrieved April 25, 2019, from https://endpts.com/the-top-25-pharmaceutical-companies-by-market-cap/
[2] Pfizer Takes Top Spot in Pharma Market Cap for 2018, Analysis Shows. Retrieved April 26, 2019, from https://www.biospace.com/article/pfizer-takes-top-spot-in-pharma-market-cap-for-2018-analysis-shows/
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點或證實其描述。若有來源標(biāo)注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn