


銠催化的有機硼試劑與缺電子雙鍵的對映選擇性加成是構建不對稱C-C鍵的重要方法。與芳基硼酸鹽相比,乙烯基硼酸鹽的研究鮮有報道。合成雙鍵含多取代基的乙烯基硼酸鹽時,烯烴的立體選擇性問題成為一大挑戰。在銠催化中,通過銠遷移可以使有機硼酸鹽產生新的反應性,實現常規方法難以達到的轉化。近年來,Hayashi課題組報道了乙烯基硼酸中乙烯基至芳基的1,4-銠遷移實現了鄰乙烯基取代的苯環與烯酮加成(Scheme 1a);Lam課題組報道了烯丙基至烯丙基的1,4-銠遷移實現了環亞胺與烯丙基硼酸酯的烯丙基化(Scheme 1b)。乙烯基至芳基的1,4-銠遷移已在有機轉化中得到應用,反過來芳基至乙烯基的1,4-銠遷移尚未報道。中國科學院上海有機所林國強院士和上海中醫藥大學馮陳國課題組通過芳基至乙烯基的1,4-銠遷移實現了烯酮和亞胺的不對稱烯基化(Scheme 1c)。
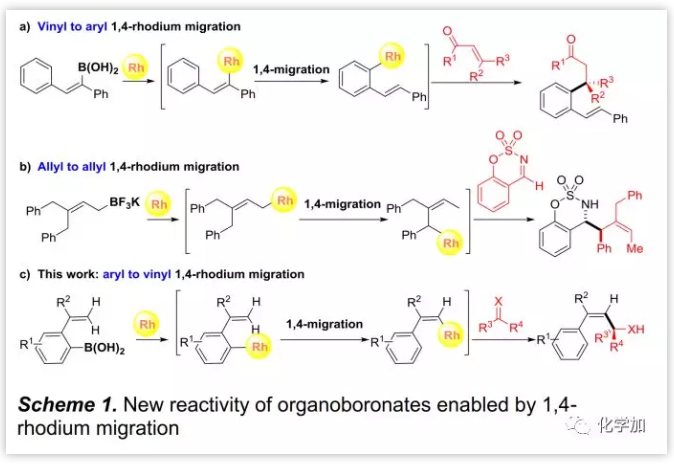
(圖片來源:Angew. Chem. Int. Ed.)
最近,作者報道了芳基至乙烯基的1,4-鈀遷移用于乙烯基硼酸酯和1,3-二烯的立體選擇性合成,其關鍵在于末端烯烴的應用以及小位阻乙烯基鈀的快速交叉偶聯對此遷移產生的推動力。作者認為類似的策略也適用于芳基至乙烯基1,4-銠遷移(Scheme 2)。當硼酸芳基酯1通過金屬轉移產生芳基銠化物2后,與缺電子雙鍵直接加成可能會受到鄰位乙烯基的影響。因此,可以先將2中鄰位乙烯基C-H鍵進行氧化加成產生4,再經H-遷移完成1,4-銠遷移。雖然乙烯基銠3不穩定,但與缺電子雙鍵的快速加成將促使反應沿遷移路徑推進。
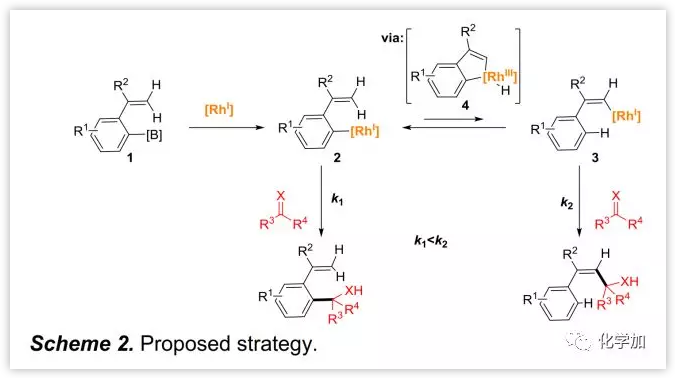
(圖片來源:Angew. Chem. Int. Ed.)
首先,作者利用芳基硼酸6a與2-環己烯酮5a作為模型反應進行了研究,并篩選了銠催化劑(Table 1)。當用[RhCl(COD)]2作為催化劑時,以優異的產率得到1,4-銠遷移/加成產物7a;當用[RhCl(C2H4)2]2和二烯L1原位生成的手性銠催化劑時,反應具有良好的對映選擇性,但由于空間位阻影響導致產率較低;當用二烯L2和L3時,反應性提高,并且L3參與的反應具有優異的對映選擇性。此外,Rh/BINAP及其衍生物催化的芳基至乙烯基1,4-銠遷移反應,具有幾乎定量的產率和完美的對映選擇性。將催化劑負載量降低(3 mol%),導致反應產率下降。在該遷移/加成過程中,產物均為單一E-異構體。
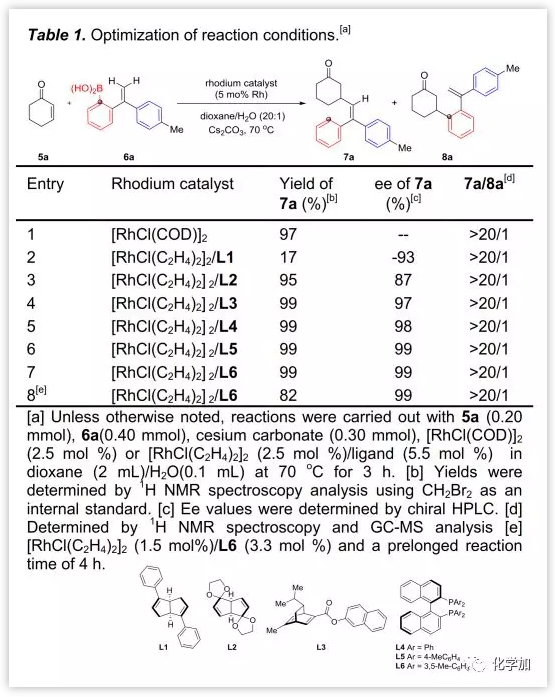
(圖片來源:Angew. Chem. Int. Ed.)
接下來,作者考察了該銠遷移/加成的底物適用范圍(Scheme 3)。通過實驗發現,所有測試的底物均可以進行1,4-銠遷移/加成反應。將苯環A中的對位甲基移至間位或鄰位增加空間位阻后,對反應產率和對映選擇性沒有影響(7a與7c和7d對比)。在對位無論引入給電子基團還是吸電子基團,都具有優異的產率和對映選擇性。當苯環A被萘基、噻吩基或吡啶基取代后,不影響反應結果;當苯環A被烷基取代后,對映選擇性保持但產率較低。相比之下,苯環B上的取代基對反應活性具有顯著影響,引入取代基特別是吸電子基團通常導致產率降低,但對映選擇性保持。這可能是由于苯環B上的取代基改變了C-B/C-Rh鍵的電性,增加了銠遷移的難度,并加速芳基硼酸酯的水解。其他環烯酮也是很好的偶聯配偶體,但更具柔性的線性烯酮反應性較低。通過單晶X-射線衍射確定7c的絕對構型為R(Figure 1),與Hayashi課題組提出的環己烯酮芳基化的立體化學一致。其他產物的構型通過假定類似的反應途徑也被推定為R。

(圖片來源:Angew. Chem. Int. Ed.)
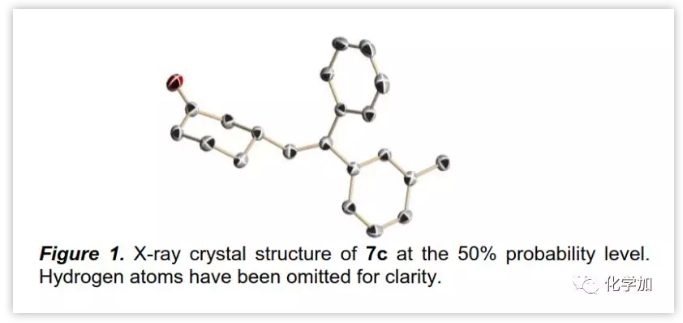
(圖片來源:Angew. Chem. Int. Ed.)
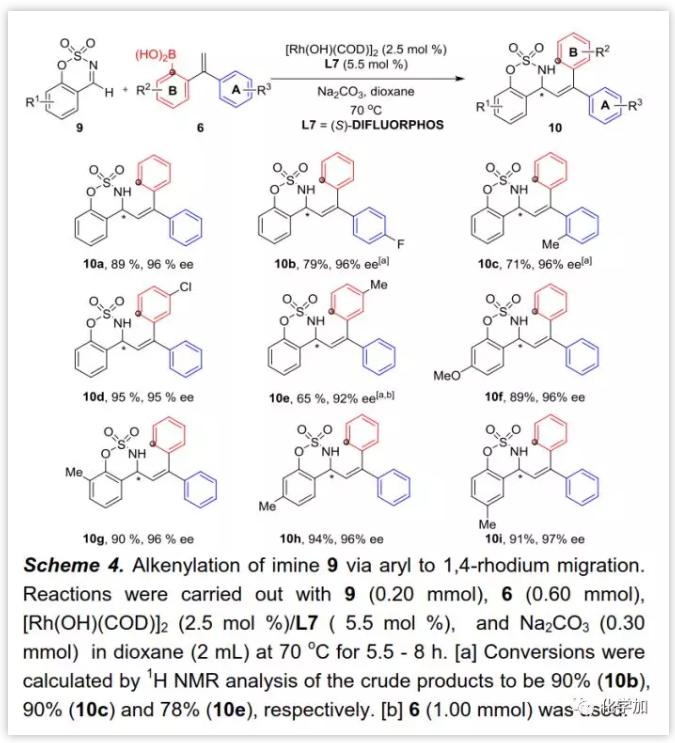
此外,作者還研究了與活性較低的亞胺的加成(Scheme 4)。其中,[Rh(OH)(COD)]2是最佳預催化劑,DIFLUORPHOS對反應至關重要。在新優化的反應條件下,作者測試了幾種芳基硼酸與環亞胺9的加成。大多數底物經過1,4-銠遷移/加成得到加成產物10,反應具有良好的產率和優異的對映選擇性。然而,苯環B被甲基取代后,反應性顯著降低;增加硼酸6用量(5 eq.)后,才能得到適當的產率。
(圖片來源:Angew. Chem. Int. Ed.)
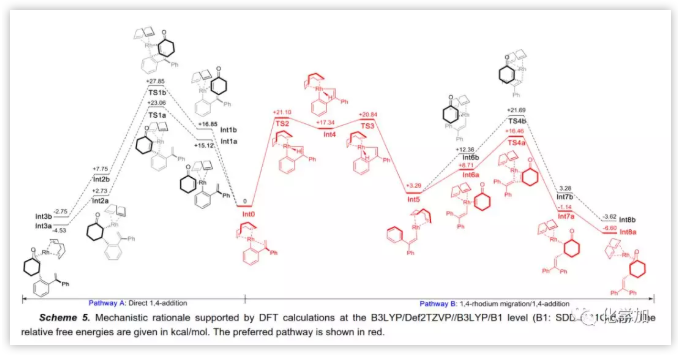
最后,作者通過DFT計算研究了1,4-銠遷移的機理(Scheme 5)。首先,構建了以COD為配體的模型系統。從銠催化劑和芳基硼酸6a通過金屬轉移產生的芳基銠Int0開始,分別通過途徑A和B得到1,4-加成產物8a和1,4-銠遷移/1,4-加成產物7a。在途徑A中,將2-環己烯酮直接插入C-Rh鍵的總能壘為23.1 kcal/mol。在途徑B中,Int0的1,4-銠遷移包括C-H氧化加成和H-遷移過程得到的乙烯基銠Int5(總能壘21.1 kcal/mol)不如芳基銠Int0穩定(+3.3 kcal/mol vs 0 kcal/mol),主要是因為苯基具有很強穩定作用以及Int0中乙烯基配位產生的額外穩定作用。雖然逆向遷移(Int5→Int0)更具能量優勢,但后續Int5與2-環己酮的加成能壘更低(+13.2 kcal/mol),導致Int5快速轉化為烯基化產物。與乙烯基至芳基的1,4-銠遷移受熱力學控制不同,芳基至乙烯基的1,4-銠遷移是動力學控制的。此外,該機理還闡明了類似的芳基至乙烯基1,4-鈀遷移/交叉偶聯過程。
(圖片來源:Angew. Chem. Int. Ed.)
小結:林國強院士和馮陳國課題組通過高效的芳基至乙烯基的1,4-銠遷移立體選擇性得到了乙烯基-銠中間體,從而實現了銠催化的烯酮和亞胺與芳基硼酸之間的不對稱烯基化。證明二烯和雙膦配體都可以催化這種銠遷移過程,并且產生優異的對映選擇性。通過DFT計算可以看出,這種遷移是動力學控制過程。
撰稿人:爽爽的朝陽
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn