



正文
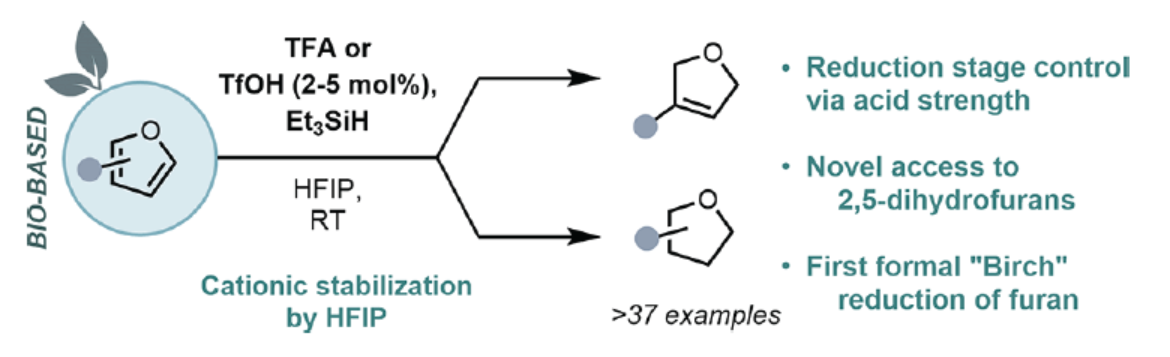
呋喃是將基于化石的化學(xué)工業(yè)轉(zhuǎn)變?yōu)榛谏锖涂沙掷m(xù)的精細(xì)化學(xué)品生產(chǎn)途徑的關(guān)鍵(Figure 1A)。目前,通過去飽和的位點(diǎn)選擇性控制,可將呋喃轉(zhuǎn)化為二氫呋喃,其在香料行業(yè)等行業(yè)備受關(guān)注(Figure 1B)。近年來,化學(xué)家們采用高壓H2和Rh-、Ir-或Ru-催化劑,通過均相和非均相金屬催化體系,實(shí)現(xiàn)了將呋喃還原為四氫呋喃,但對(duì)于呋喃骨架的直接去芳構(gòu)化策略,卻較少有相關(guān)的研究報(bào)道。其中,將呋喃轉(zhuǎn)化為二氫呋喃的Birch還原反應(yīng),僅限于少數(shù)缺電子或羧酸酯取代的底物。同時(shí),由于呋喃骨架易發(fā)生不受控制的二聚和開環(huán)反應(yīng),導(dǎo)致此類去芳構(gòu)化策略極具難度。近日,Benjamin List團(tuán)隊(duì)報(bào)道了一種溫和的Br?nsted酸催化呋喃的還原反應(yīng),合成了一系列形式Birch-還原產(chǎn)物2,5-二氫呋喃衍生物。同時(shí),當(dāng)采用硅烷作為還原劑,還可實(shí)現(xiàn)相應(yīng)的全還原反應(yīng),獲得相應(yīng)的四氫呋喃衍生物(Figure 1C)。歡迎下載化學(xué)加APP到手機(jī)桌面,合成化學(xué)產(chǎn)業(yè)資源聚合服務(wù)平臺(tái)。

(圖片來源:J. Am. Chem. Soc.)
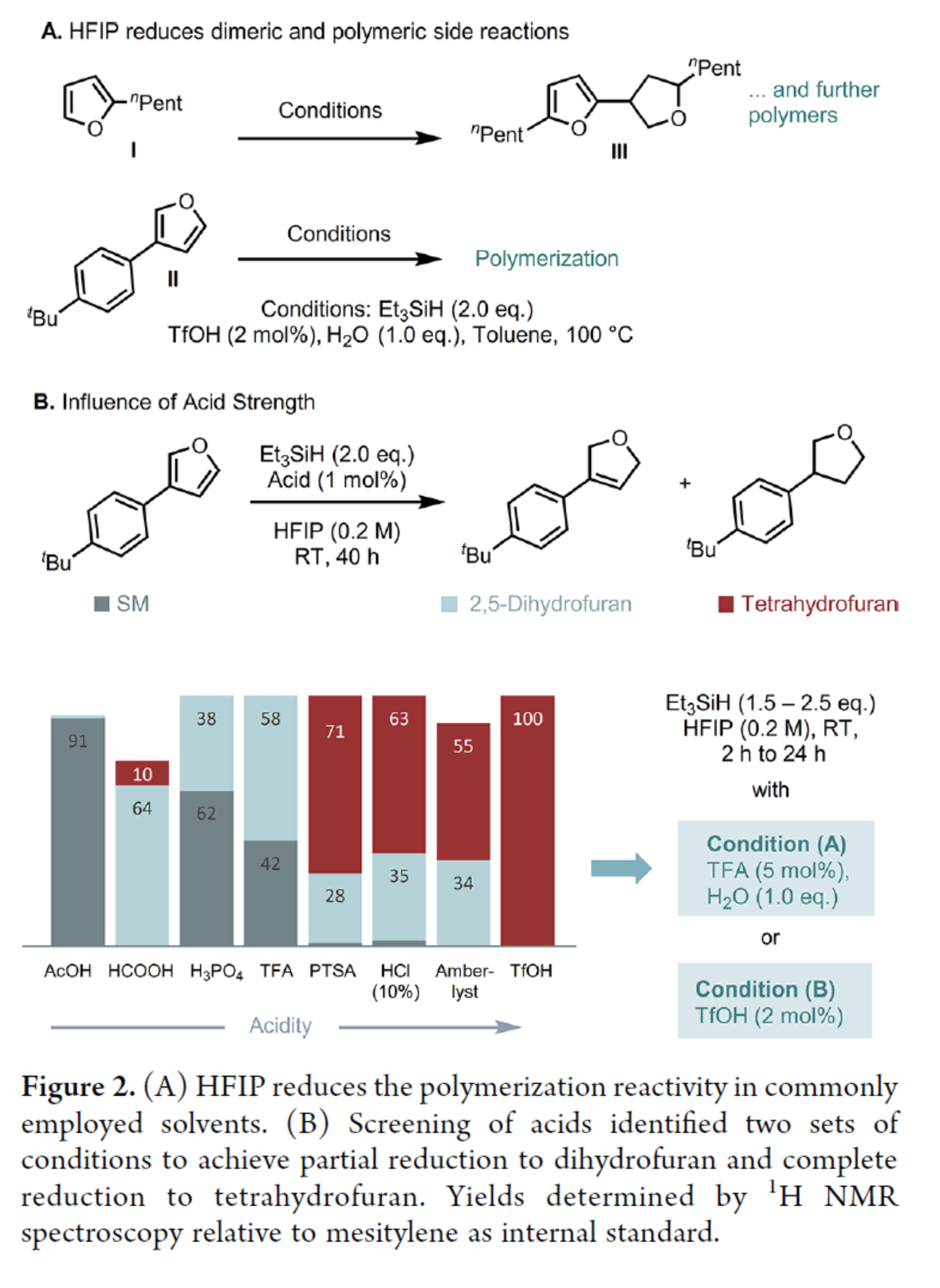
其次,作者以2-戊基呋喃(I)或3-芳基呋喃(II)作為模型底物,進(jìn)行了相關(guān)反應(yīng)條件的篩選(Figure 2)。篩選結(jié)果表明,當(dāng)以Et3SiH作為還原劑,在TFA或TfOH催化下,均未發(fā)生反應(yīng),或者進(jìn)行二聚反應(yīng)(如III)(Figure 2A)。進(jìn)一步的優(yōu)化后發(fā)現(xiàn),HFIP能夠降低常用溶劑中的聚合反應(yīng)性。同時(shí),H2O的添加對(duì)于實(shí)現(xiàn)完全轉(zhuǎn)化也至關(guān)重要。并且,酸的強(qiáng)度也影響還原的程度(Figure 2B)。因此,作者確定了兩種最佳的反應(yīng)條件,即在Condition A條件下,以TFA(5 mol %)作為催化劑,H2O(1.0 equiv)作為添加劑,Et3SiH(1.5 equiv)作為還原劑,在HFIP溶劑中室溫反應(yīng),可以58%的收率得到2,5-二氫呋喃產(chǎn)物。在Condition B條件下,以TfOH(2 mol %)作為催化劑,Et3SiH(2.5 equiv)作為還原劑,在HFIP溶劑中室溫反應(yīng),可以100%的收率得到四氫呋喃產(chǎn)物。
(圖片來源:J. Am. Chem. Soc.)
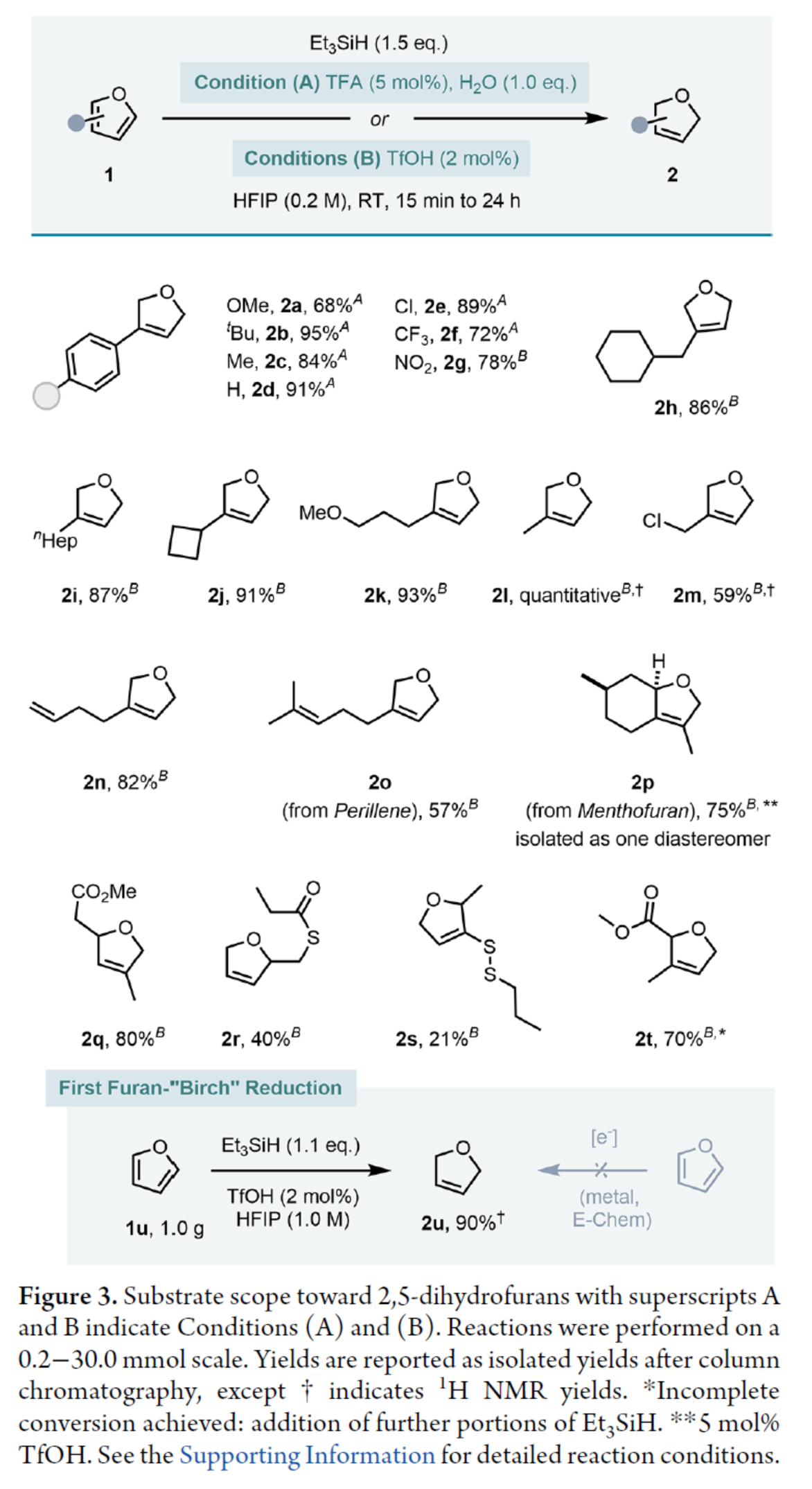
在獲得上述最佳反應(yīng)條件后,作者對(duì)合成2,5-二氫呋喃產(chǎn)物的底物范圍進(jìn)行了擴(kuò)展(Figure 3)。首先,各種3-芳基取代的呋喃衍生物,均可順利進(jìn)行反應(yīng),獲得相應(yīng)的產(chǎn)物2a-2g,收率為68-95%。其中,對(duì)于含有強(qiáng)吸電子基的底物,則需在酸性更強(qiáng)的條件(即Condition B)下才能反應(yīng),如2g。其次,對(duì)于3-烷基取代的呋喃,也需在酸性更強(qiáng)的條件(即Condition B)下反應(yīng),獲得相應(yīng)的產(chǎn)物2h-2l,收率為86-100%。令人驚訝的是,含有氯甲烷(2m,59%)和末端烯基(2n,82%)取代的底物,也與體系兼容,由于其在離子硅烷還原過程中也會(huì)被還原。此外,紫蘇精油中的天然單萜紫蘇烯,可以57%的收率得到部分還原產(chǎn)物2o。調(diào)味劑薄荷呋喃,可以75%的收率得到產(chǎn)物2p。2,4-取代呋喃,可以80%的收率得到產(chǎn)物2q。含有(硫代)酯的呋喃,可以40%的收率得到產(chǎn)物2r。含有雙硫鍵的底物,僅以21%的收率得到產(chǎn)物2s。含有烷氧羰基取代的底物,可以70%的的收率得到產(chǎn)物2t。然而,2-羧基呋喃或3-羧基呋喃,未能有效的進(jìn)行反應(yīng)。值得注意的是,呋喃本身(1u)也是一種合適的底物,可以90%的收率轉(zhuǎn)化為2,5-二氫呋喃(2u),這是呋喃首次形式Birch還原的例子。
(圖片來源:J. Am. Chem. Soc.)
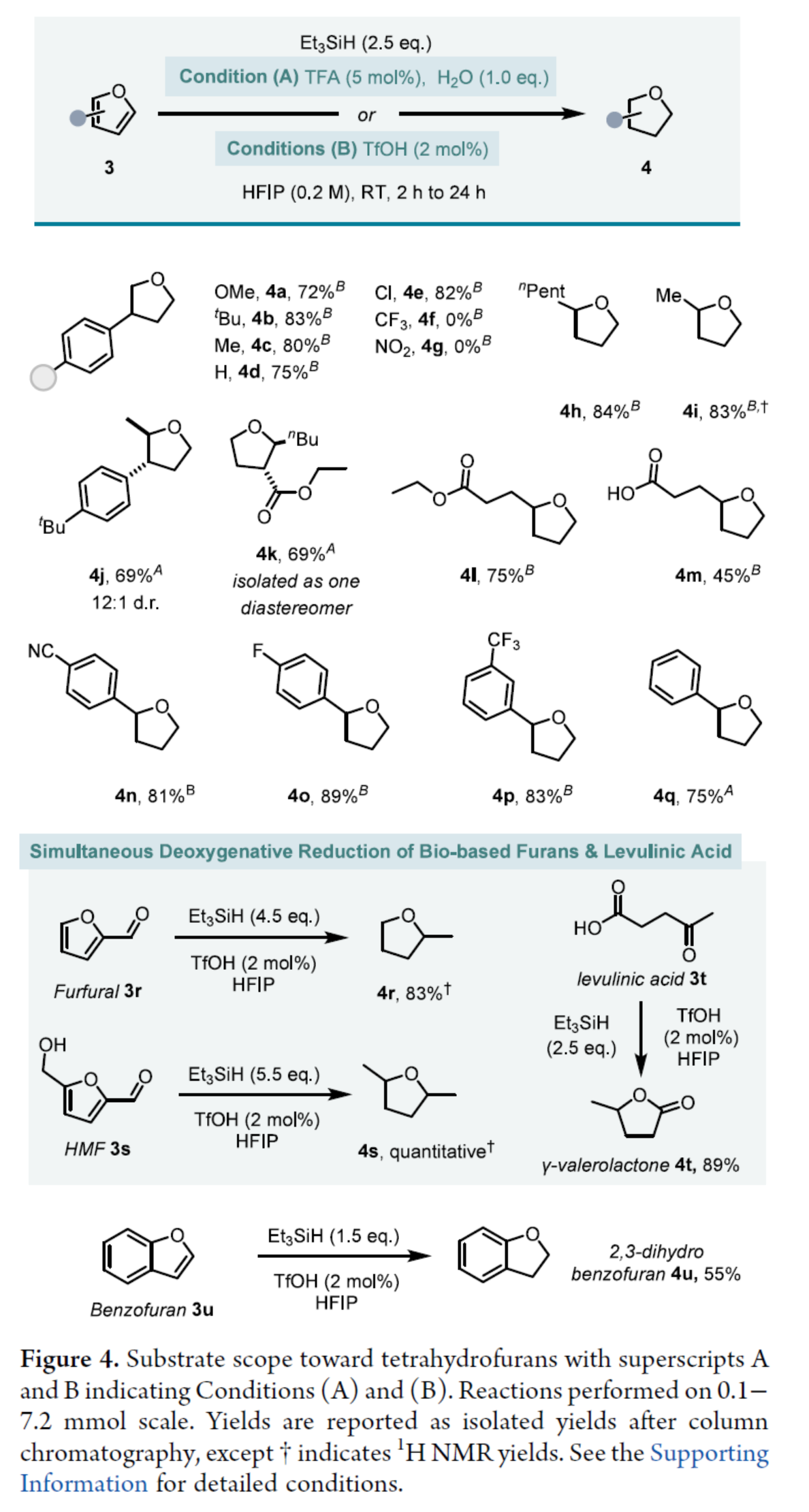
緊接著,作者對(duì)合成四氫呋喃產(chǎn)物的底物范圍進(jìn)行了擴(kuò)展(Figure 4)。首先,各種3-芳基取代的呋喃衍生物,均可順利進(jìn)行反應(yīng),獲得相應(yīng)的產(chǎn)物4a-4e,收率為72-83%。然而,芳基上含有強(qiáng)吸電子基的呋喃衍生物,未能有效的進(jìn)行反應(yīng),如4f和4g。其次,2-烷基與2-芳基取代的呋喃衍生物,也與體系兼容,獲得相應(yīng)的產(chǎn)物4h-4q,收率為45-89%。此外,糠醛和4-羥甲基糠醛(HMF),也是合適的底物,獲得相應(yīng)的產(chǎn)物4r(83%)和4s(定量)。同時(shí),乙酰丙酸3t經(jīng)還原環(huán)化,可以89%的收率得到γ-戊內(nèi)酯產(chǎn)物4t。苯并呋喃,也可以55%的收率轉(zhuǎn)化為2,3-二氫苯并呋喃產(chǎn)物4u。
(圖片來源:J. Am. Chem. Soc.)
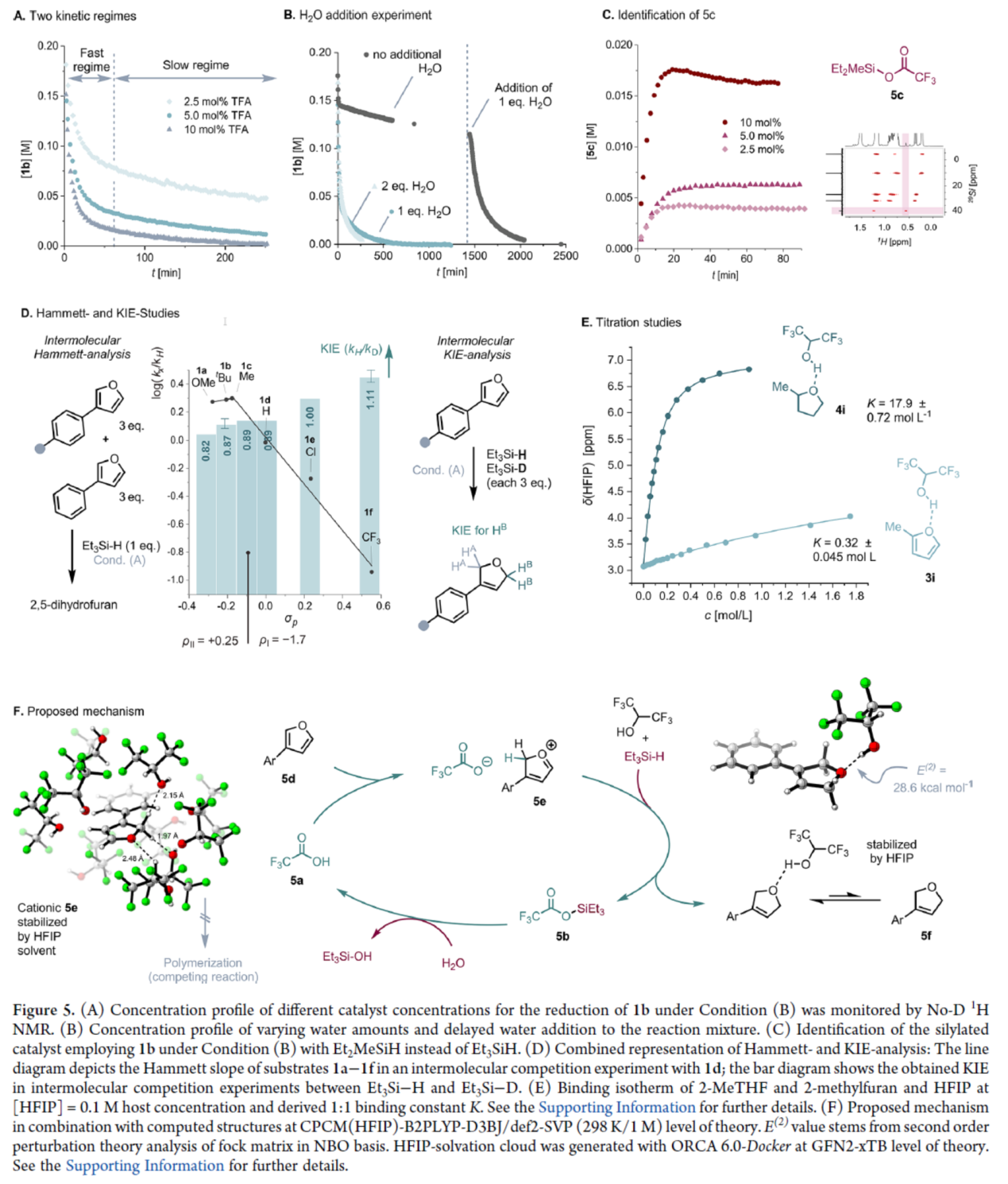
隨后,作者對(duì)反應(yīng)機(jī)理進(jìn)行了研究(Figure 5)。首先,反應(yīng)動(dòng)力學(xué)不受Et3SiH當(dāng)量的影響,表明了對(duì)Et3SiH的零級(jí)依賴性。其次,研究了TFA催化劑的負(fù)載量,可以確定動(dòng)力學(xué)時(shí)間過程中的兩種狀態(tài),并且催化劑負(fù)載量越高,反應(yīng)速度越快(Figure 5A)。通過水添加的對(duì)照實(shí)驗(yàn)發(fā)現(xiàn),體系無水時(shí)僅有25%的轉(zhuǎn)化率,加入1.0當(dāng)量水后,反應(yīng)可繼續(xù)進(jìn)行(Figure 5B)。通過在不同濃度下使用Et2MeSiH代替Et3SiH的實(shí)驗(yàn)表明,反應(yīng)形成了硅烷化催化劑Et2MeSi-TFA 5c(Figure 5C)。Hammett與KIE研究結(jié)果表明,對(duì)于缺電子的呋喃1e和1f,呋喃的質(zhì)子化為決速步。而對(duì)于富電子的呋喃1a-1c,還原過程為決速步(Figure 5D)。滴定研究結(jié)果表明,HFIP和5f之間存在強(qiáng)氫鍵。乙醚氧的HFIP配合物為還原反應(yīng)增加了額外的驅(qū)動(dòng)力(Figure 5E)。
基于上述的討論,作者提出了一種合理的反應(yīng)機(jī)理(Figure 5F)。首先,在呋喃5d質(zhì)子化后,氧雜卡賓陽離子5e在2-位被Et3SiH還原,生成2,5-二氫呋喃產(chǎn)物5f。催化三氟乙酸根陰離子與剩余的硅陽離子(silylium)配位,生成穩(wěn)定的中間體5b。然后,5b與H2O經(jīng)加氫去硅化(hydrodesilylation),可再生成活性催化劑。
(圖片來源:J. Am. Chem. Soc.)
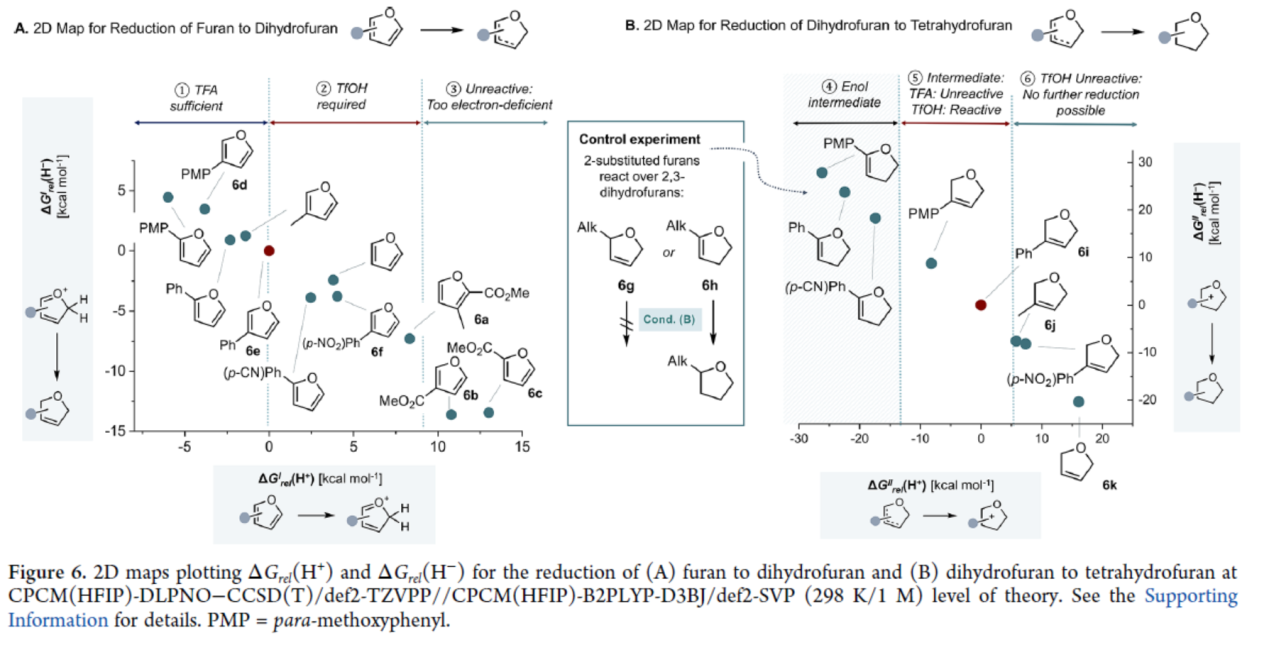
此外,作者還通過二維圖對(duì)呋喃還原過程中的反應(yīng)性差異進(jìn)行了研究(Figure 6)。在呋喃還原為二氫呋喃的過程中,6d可被TFA進(jìn)行充分質(zhì)子化(①)。對(duì)于6f,使用TfOH可以有效促進(jìn)質(zhì)子化(②)。對(duì)于6b或6c,反應(yīng)需使用比TfOH更強(qiáng)的酸(③)。其次,由于相對(duì)高的質(zhì)子親和力,導(dǎo)致2-取代呋喃總是還原為四氫呋喃(④)。3-烷基取代的呋喃6j以及2,5-二氫呋喃6k的質(zhì)子化太不利,無法進(jìn)一步轉(zhuǎn)化為四氫呋喃(⑥),僅進(jìn)行部分還原。對(duì)于其他的中間體,可以通過酸強(qiáng)度實(shí)現(xiàn)選擇性控制(⑤)。
(圖片來源:J. Am. Chem. Soc.)
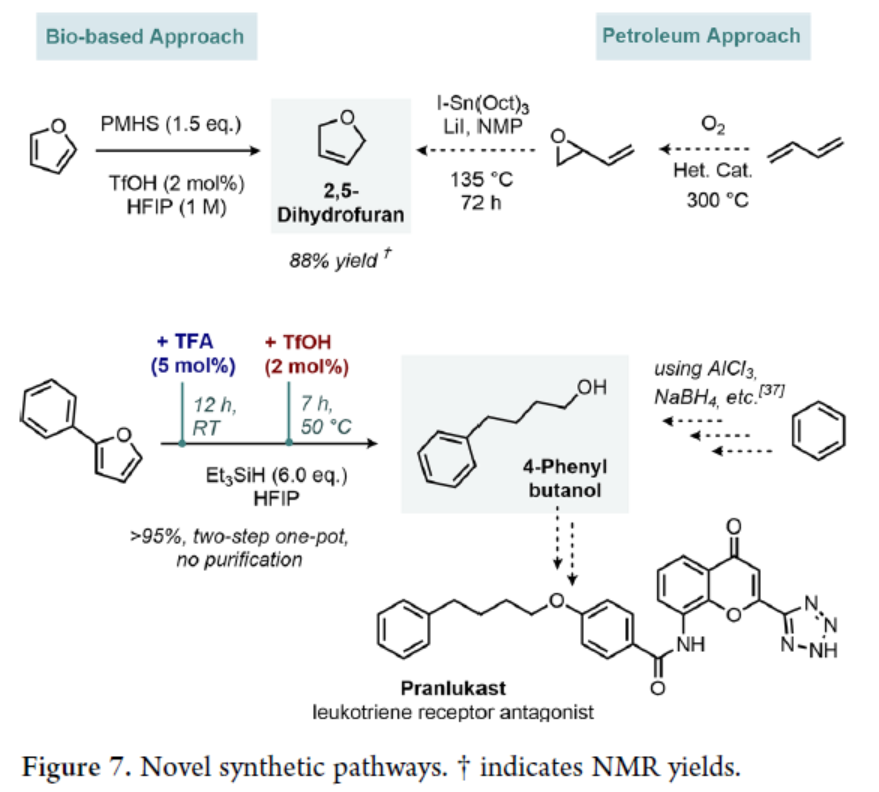
最后,基于工業(yè)方法與生物基方法相比,該策略可作為一種新型的合成途徑(Figure 7)。例如,呋喃可一步轉(zhuǎn)化為2,5-二氫呋喃,避免了工業(yè)上的環(huán)氧化和熱重排的過程。2-苯基呋喃在TFA/TfOH條件下可轉(zhuǎn)化為4-苯基丁醇,其作為合成白三烯受體拮抗劑(Pranlukast)的關(guān)鍵中間體,避免了工業(yè)上使用AlCl3、NaBH4等危險(xiǎn)性試劑。
(圖片來源:J. Am. Chem. Soc.)
總結(jié)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn