

近期,加利福尼亞大學伯克利分校(UC-Berkeley)化學系的助理教授Thomas J. Maimone就在Science上發表了一篇關于二倍半萜的簡捷高效全合成的文章,題目為“Enantioselective synthesis of an ophiobolin sesterterpene via a programmed radical cascade”,文章鏈接為10.1126/science.aaf6742。
作者以程序化的自由基串聯環化反應為關鍵步驟總共9步就完成了復雜二倍半萜 (–)-6-epi-ophiobolin N的全合成,堪稱全合成里面的經典牛文,簡捷、快速、高效、精彩!閑話少敘,咱們也從Who、What、How、Why四個方面欣賞一下這篇全合成佳作,一睹牛人牛作的風采。
Who 本文作者Thomas J. Maimone系UC-Berkeley化學系的本科,師從Dirk Trauner,Scripps的博士,師從當代合成超級新星Phil Baran,MIT的博士后,師從Buchwald,2012年回到UC-Berkeley開始獨立工作,主攻方向為天然產物全合成。值得一提的是,陜西師范大學的趙玉明副教授(蘭州大學化學系本科,博士,涂永強院士的弟子)曾師從Thomas J. Maimone進行過博士后研究。
What 本文的目標分子為蛇孢菌素家族類天然產物二倍半萜 (–)-6-epi-ophiobolin N,如圖1所示,從結構上看,似乎并不復雜,但其核心骨架5-8-5并環體系以及上面豐富的手性中心正是全合成的挑戰,眾所周知,由于八元環合成中熵效應和焓效應都不利,加之跨環相互作用,使得八元環的合成異常艱難,比如紫杉醇Taxol中八元環的構建。蛇孢菌素家族類天然產物由于新穎的化學骨架和顯著的生物活性,吸引了眾多的有機合成化學家進行全合成研究,但到目前為止,只有兩篇全合成報道,且分別用了38步和47步。(分別發表在JACS和Angew上,該類分子的重要性和合成挑戰可見一斑。)

How 那本文的作者是如何進行全合成的呢。一般來說,自然界中,萜類都是由聚異戊烯在酶催化下經由多烯環化合成的,Thomas J. Maimone也從生源合成中得到啟發,希望通過8-endo/5-exo程序化可控的自由基串聯環化反應一步構建5-8-5核心碳環骨架,前體可以逆推至已知原料芳樟醇linalool和金合歡醇 farnesol。
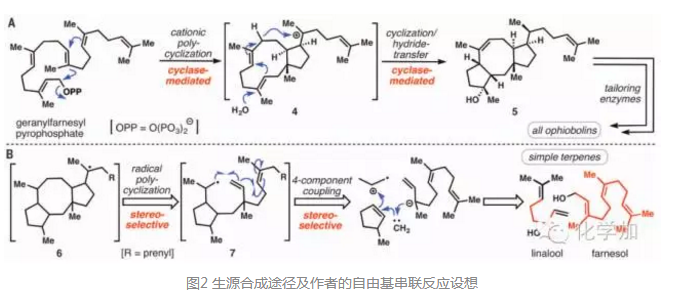
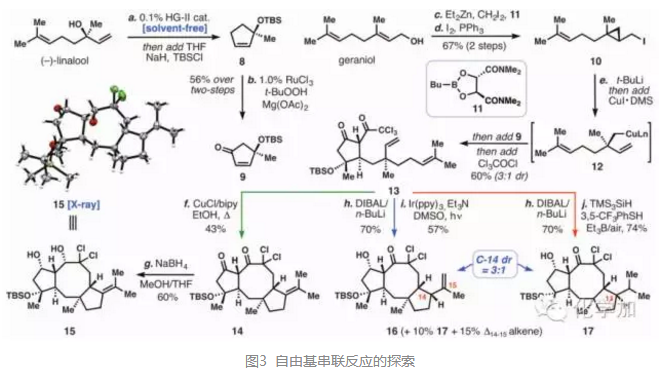
從10個碳單位的芳樟醇出發,無溶劑條件下RCM反應后保護三級羥基得到環戊烯化合物8,再在烯丙位氧化出羰基得到環戊烯酮9。另一方面,從香葉醇geraniol出發,環丙烷化后再經Appel反應得到碘代物10,加入t-BuLi鋰鹵交換后打開環丙烷并和銅發生轉金屬化得到中間體12,再和環戊烯酮9以及三氯乙酰氯發生三組分反應,Michael后羰基α-位親核取代得到化合物13,即自由基關環前體,再在自由基引發條件下順利關環得到5-8-5環系,其結構和立體化學由單晶予以確證。
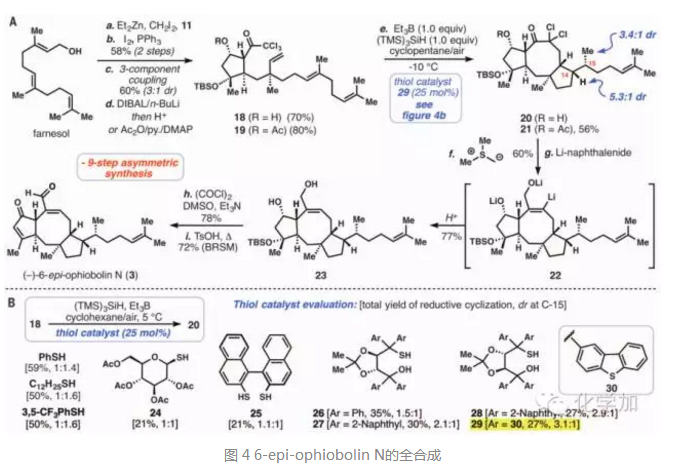
有了這些成功的探索,作者嘗試了將這一串聯的自由基環化策略用于蛇孢菌素類天然產物真實體系的全合成中,從15個碳單位的金合歡醇 farnesol出發,經由環丙烷化后Appel反應得到碘代物,再和環戊烯酮9以及三氯乙酰氯發生三組分反應并還原五元環上酮羰基得到化合物18或者乙酰基保護得到化合物19,即自由基關環前體,在Et3B、(TMS)3SiH條件下,發生串聯的自由基環化反應得到化合物20或者21,并通過硫醇催化劑的篩選,催化劑29給出了最優的非對映選擇性。
化合物20或者21發生Corey-Chaykovsky反應得到環氧,同時脫去乙酰基保護基,再在過量鋰萘的還原下,打開環氧,質子化后得到二醇化合物23,最后Swern氧化兩個羥基分別得到酮和醛,酸性條件下脫去TBS保護并脫水形成烯酮,僅僅用了9步就簡捷高效地完成了6-epi-ophiobolin N的全合成,總產率2%,作者也得到了15 mg目標產物。
Why 這篇文章為什么發在了Science,亮點在哪里?欣賞了全文,我們可以看出Thomas J. Maimone團隊仿照生源合成途徑,提出了一種全新的程序化可控的自由基串聯環化反應的策略,一步構建了具有挑戰性的核心5-8-5環系,碳環骨架構建以后只需幾步簡單轉化就可以實現天然產物的全合成,僅僅用了9步就完成了全合成,非常簡捷高效,符合原子經濟性和步驟經濟性的要求,這對于其它蛇孢菌素類天然產物以及萜類天然產物的全合成都有重要意義。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn