(圖片來源:Nature)
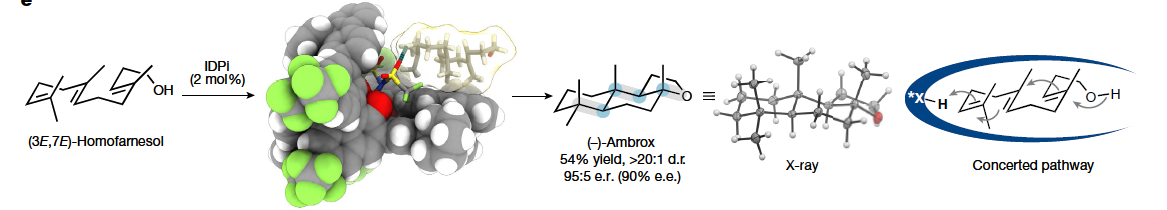
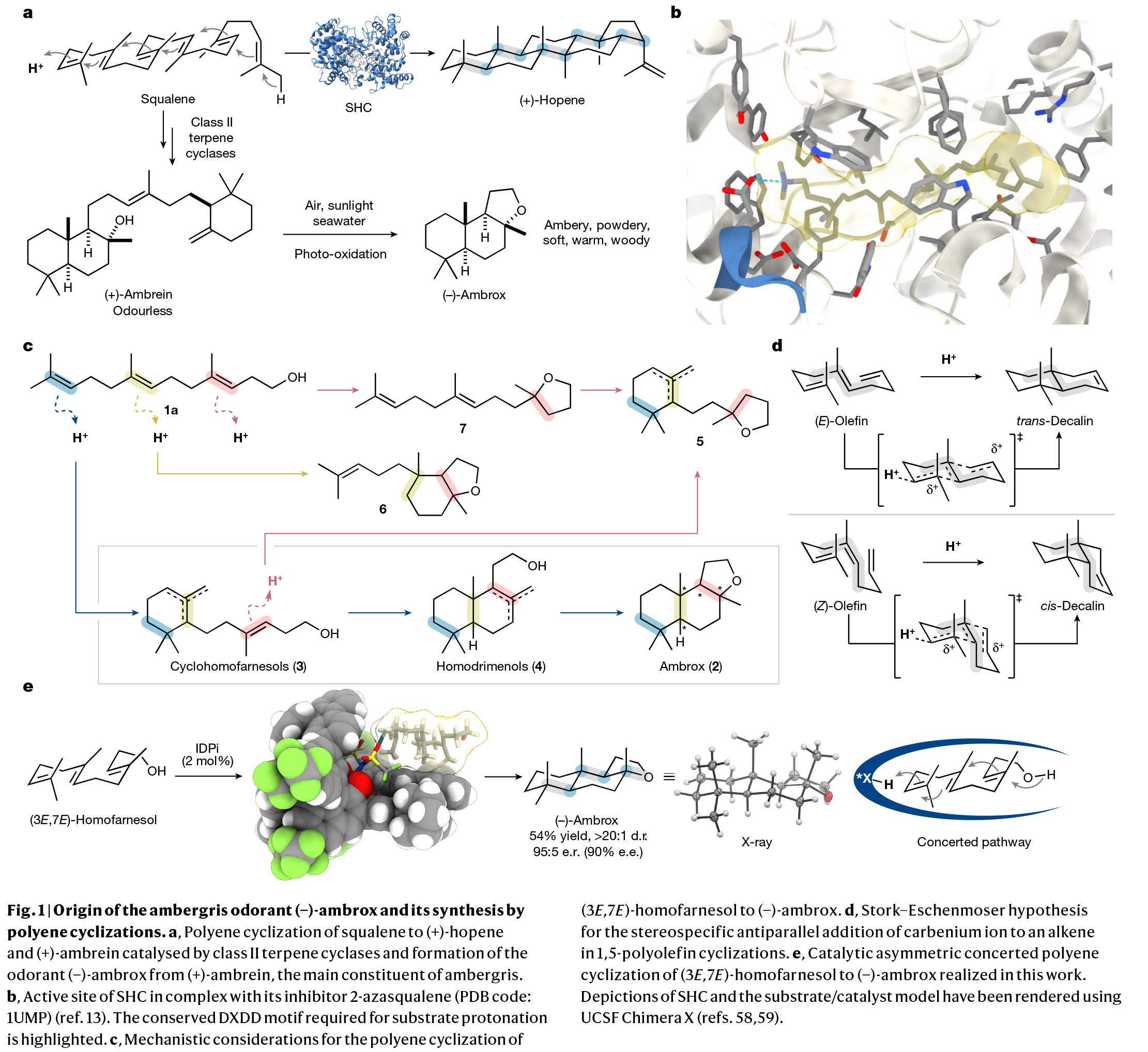
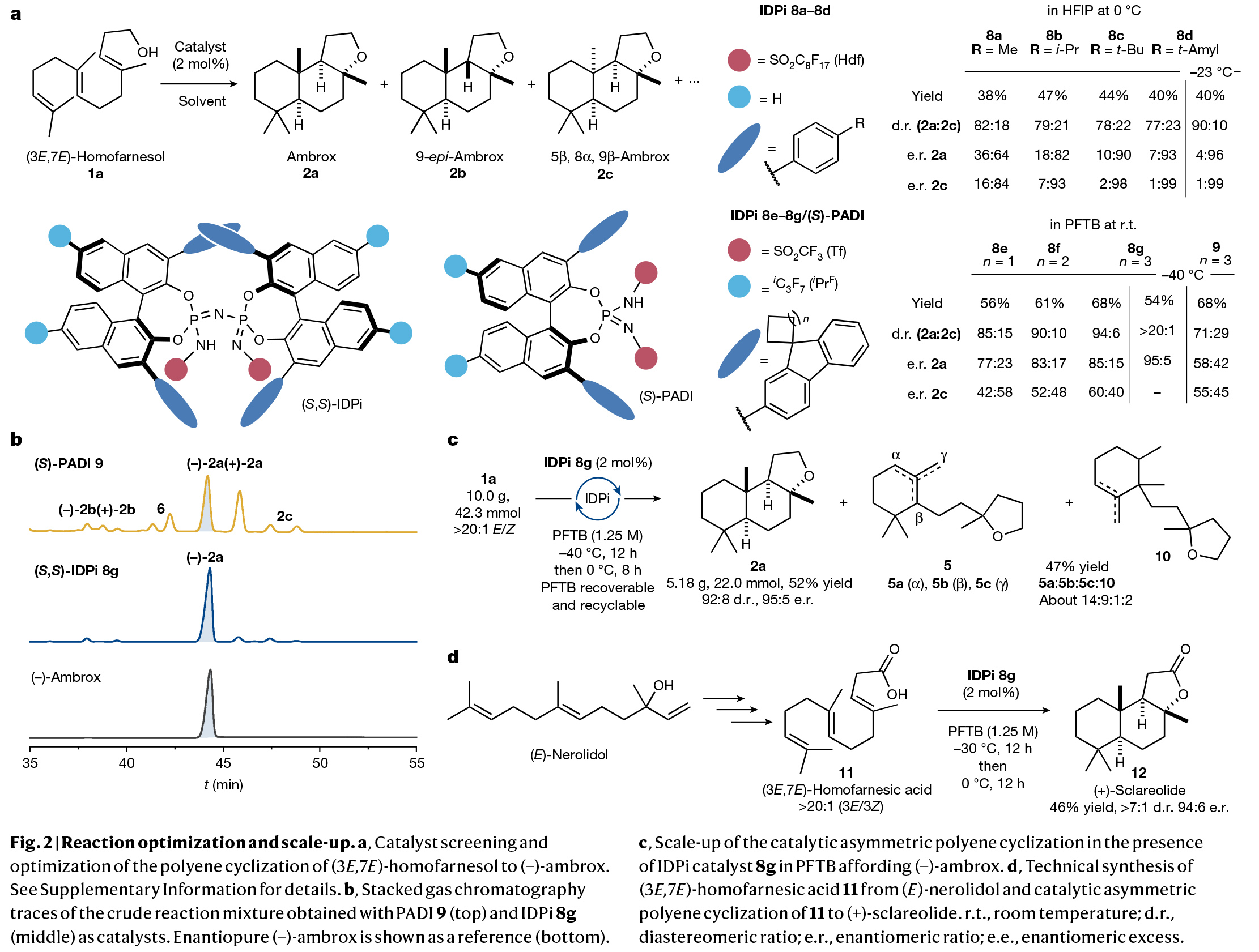
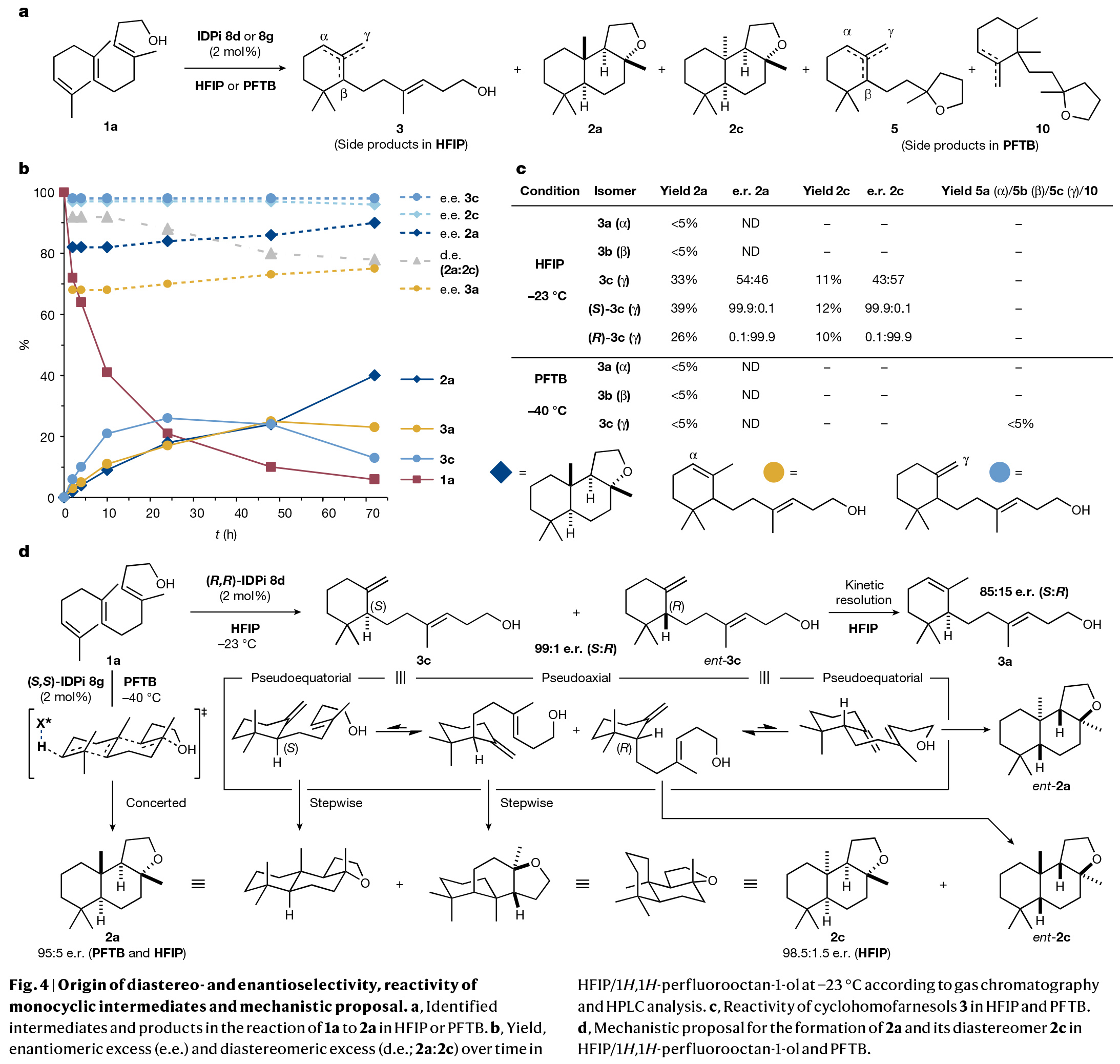
多烯環化是生物學中最復雜且最具挑戰性的轉化之一。其可以在一步反應中中,利用簡單的非環前體實現多根碳碳鍵、環體系和立體中心的構建。而在構建的同時實現產物立體化學的精確控制對化學家來說是一項艱巨的任務。特別是利用(3E,7E)-homofarnesol的多烯環化來合成天然存在且具有重要價值的(?)-ambrox是化學合成中長期存在的挑戰。最近,德國馬克斯-普朗克研究所Benjamin List課題組報道了在氟化醇的存在下,使用具有高Br?nsted酸性的IDPi催化劑,通過催化不對稱多烯環化,以良好的非對映選擇性和對映選擇性實現了(?)-ambrox和倍半萜內酯天然產物(+)-sclareolide的合成(Fig. 1)。化學加——科學家創業合伙人,歡迎下載化學加APP關注。首先,作者以(3E,7E)-homofarnesol 1a為模板底物,對其環化過程進行了條件篩選(Fig. 2a)。實驗結果表明,兩種不同條件下的兩種催化劑模式(IDPi 8d,HFIP;和 IDPi 8g,PFTB)成為以高產率、非對映和對映選擇性提供ambrox 2a的最佳體系。此外,作者通過將IDPi催化劑8g與具有高酸性但結構約束較弱的PADI(N,N’-bistriflylphosphoramidimidate)催化劑9進行比較,后者產生了復雜的產物混合物,這進一步證明了受限活性位點的重要性(Fig. 2b)。在最優反應條件下,作者對多烯環化反應的規模化合成進行了考察。經過催化劑的定量回收和純化,作者以52%的產率得到了5.2 g (-)-ambrox,dr = 92:8, er = 95:5,部分環化產物5和10的產率為47%(Fig. 2c)。這相當于在20小時的反應時間內有296 g l?1的理論體積生產率。目前最優的(?)-ambrox生物催化生產工藝在72小時內可實現300-450 g l?1 (3E,7E)-homofarnesol的完全轉化。將(3E,7E)-homofarnesic酸(很容易從(E)-nerolidol中獲得)在PFTB中的反應條件下,可以以46%的產率,>7:1 dr和94:6 er得到所需的內酯天然產物12(Fig. 2d)。為了深入了解多烯環化的機理,并探討其高化學選擇性、非映體選擇性和對映體選擇性的來源,作者進行了一系列控制實驗。從多烯1a形成三環2a的不同機理是可以想象的。從線性多烯構建三環體系既可以通過協同的級聯環化進行,也可以通過形成單環和雙環中間體的完全逐步進行(Fig. 3a)。受動力學同位素效應(KIE)研究的啟發,在天然豐度下探索Diels-Alder環加成的協同性質,作者設想一個類似的實驗是否也可以得出對多烯環化性質的了解。在協同多烯環化的情況下,由于每根化學鍵的形成都涉及到速率決定步驟,因此在所有雙鍵位置上都可能存在KIEs。在兩個獨立的實驗中(在-40 oC下轉化率分別為96%和91%),在回收的(3E,7E)-homofarnesol中的每個雙鍵上均觀察到了較小但具有統計學意義的13C KIEs,這表明質子化和C-C鍵的形成是同時發生的(Fig. 3b)。接下來,作者進行了氘標記研究,進一步闡明了IDPi催化多烯環化的機理,并探索了初始質子化過程的選擇性。在協同多烯環化的情況下,單一氘化位點是可預期的,而多個標記位置將是逐步過程的特征。通過比較?40 °C下IDPi催化的多烯環化反應所回收的產物2a的2H{1H}和1H NMR,作者發現了一個單一的氘化位點(Fig. 3c)。這表明在低溫(- 40 °C),IDPi 8g存在下所形成的(?)-ambrox大部分是由協同多烯環化產生的。根據2H{1H}NMR得出,從γ-環homofarnesol 3c在-40 °C下通過逐步途徑形成(?)-ambrox的比例小于5%。而對赤道軸位置的高選擇性表明在內烯烴上存在立體定向反平行加成。另一個重要的觀察結果是(3E,7E)-homofarnesol的內部或近端雙鍵的質子化或重原子化沒有產生任何副產物。相比之下,從IDPi催化的多烯環化中分離出的產物2a在多個位點上觀察到了氘的結合。由于在IDPi催化的多烯環化反應中并沒有觀察到雙環副產物6,因此證實了IDPi催化劑對遠端雙鍵質子化的高選擇性。接下來,作者通過將homofarnesol 1的所有可能的非對映體置于反應條件下,進一步研究了IDPi催化的多烯環化的協同性質(Fig. 3d)。對于每一種非對映體,各自的主要分離產物的形成可以用Stork-Eschenmoser假設來解釋,這與協同多烯環化過程相一致。此外,需要將反應溫度提高到-30 oC才能轉化(3E,7Z)和(3Z,7Z)-homofarnesol (1c和1d)。作者認為在較低溫度下,結構擁擠的底物,如1c和1d會無法進入受限的活性位點。最后,為了深入的理解不同非對映選擇性和對映選擇性的來源,作者進行了控制實驗(Fig. 4)。實驗結果表明IDPi的受限活性位點優先選擇醇附近的更容易接近的雙鍵,而不是擁擠的環己烯。在此進行的機理研究的基礎上,作者認為催化劑8g達到所觀察到的高非映體和對映體選擇性的關鍵是協同反應途徑優于逐步過程。Benjamin List課題組報道了可規模化的(3E,7E)-homofarneso不對稱多烯環化,實現了重要的(?)-ambrox的合成,解決了化學合成中長期存在的挑戰,并以前所未有的立體選擇性提供了所需的產物。相信該方法將在相關的多烯環化中得到廣泛應用,并可能加速從現成的非手性起始原料實現天然產物和藥物的不對稱合成。文獻詳情:
The catalytic asymmetric polyene cyclization of homofarnesol to ambrox. Na Luo, Mathias Turberg, Markus Leutzsch, Benjamin Mitschke, Sebastian Brunen, Vijay N. Wakchaure, Nils N?thling, Mathias Schelwies, Ralf Pelzer, Benjamin List*. https://doi.org/10.1038/s41586-024-07757-7.