

(圖片來源:Sci. Adv.)
正文
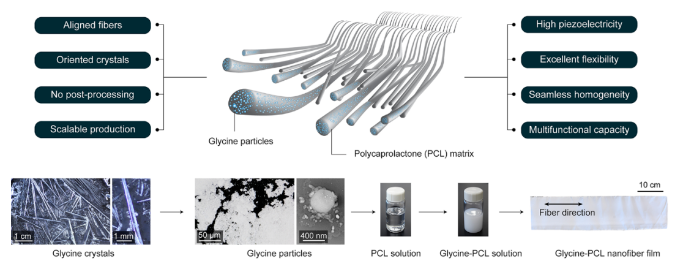
甘氨酸-PCL納米纖維由填充有取向的甘氨酸晶體的PCL基質組成(圖1A)。因此,它們既可以利用甘氨酸晶體的高壓電性,又可以利用PCL基質的輕便、靈活的特性來產生高壓電輸出的大應變。甘氨酸-PCL納米纖維的制備過程如圖1B所示。由于β-甘氨酸是甘氨酸的壓電性最強的相,采用慢蒸發技術生長了β-甘氨酸針狀晶體。然后在均質機中適當地研磨生長的晶體,直到尺寸(約500 nm)適合于靜電紡絲過程。因為甘氨酸晶體不能直接靜電紡絲,所以在這個過程中需要一個聚合物基質。發現PCL具有眾所周知的安全性和低彈性模量,滿足所有要求,以確保穩定和高的壓電響應以及產生強大的超聲的能力。下載化學加APP到你手機,更加方便,更多收獲。
圖1C顯示了PCL和甘氨酸-PCL納米纖維的掃描電子顯微鏡(SEM)圖像,顯示了纖維的表面形態以及單個納米纖維中甘氨酸晶體的存在。極小的甘氨酸顆粒均勻分布在PCL基質的整個納米纖維膜上(圖1D)。圖1E顯示了甘氨酸-PCL納米纖維膜的傅里葉變換紅外(FTIR)光譜。與空白的PCL納米纖維膜相比,甘氨酸帶(氨基和羧基)在甘氨酸-PCL納米纖維樣品中明顯出現在3155、2600和1583 cm?1處。
為了確定晶相,作者對甘氨酸-PCL納米纖維進行了X-射線衍射(圖1F)。結果表明了使用PCL納米纖維來穩定包被β-甘氨酸的好處,它表現出很強的壓電效應,但如果沒有這樣的包被,在環境條件下通常不穩定并且很快轉變為低壓電性的α相。圖1G顯示出嵌入在極軟的PCL基質的納米纖維結構中的晶體具有相當大的改善的靈活性和甚至延伸性。此外,甘氨酸-PCL納米纖維膜可以彎曲、拉伸、折疊和扭曲多次,突出了甘氨酸-PCL納米纖維膜的靈活性和機械穩定性(圖1H)。圖1I顯示了甘氨酸-PCL納米纖維膜插入兩個填充了PBS (pH=7.4)和DMEM的孔中并保持在生理溫度(37 ℃)的兩個序列圖像。整合后的納米纖維膜在PBS中降解均勻,沒有斷裂。而在DMEM中降解不那么均勻,有形成碎片的趨勢。
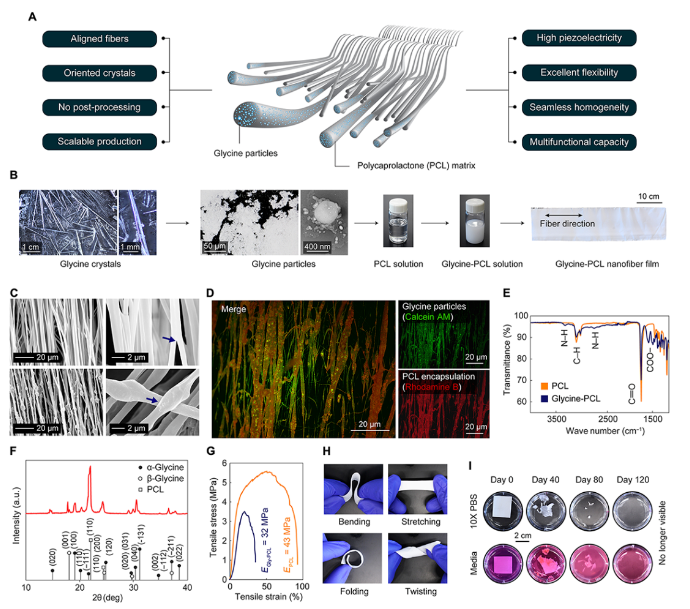
圖1. 甘氨酸-PCL集成納米纖維的制備和表征
圖片來源:Sci. Adv.
該研究中使用三種方法制備了甘氨酸-PCL薄膜:溶劑澆鑄、靜電紡絲和動態靜電紡絲。與其他方法的樣品相比,動態靜電紡絲薄膜具有特殊程度的纖維取向(有利于壓電性)。隨著薄膜中的晶體變得更加定向,WAXS圖案從完整的德拜環變為部分環,證明PCL纖維和甘氨酸晶體的晶體取向(圖2A)。動態靜電紡絲樣品(4000 rpm)顯示出~12 μm的顯著位移,而相同厚度的溶劑澆鑄和靜電紡絲(0 rpm)樣品沒有可測量的位移(圖2B)。這表明取向甘氨酸-PCL納米纖維薄膜能夠產生一種強大的致動器,可以在較高頻率的施加電壓下用于超聲波應用。
通過評估由結晶β-甘氨酸和直接從原料甘氨酸粉(不生長β-甘氨酸晶體)制成的兩個樣品之間的逆壓電性能(圖2C-2D),發現用結晶β-甘氨酸制備的甘氨酸-PCL薄膜的性能優于用原料甘氨酸粉末制備的樣品。這證實了生長β-晶體的必要性,而不是簡單地使用原始粉末進行靜電紡絲。值得注意的是,甘氨酸-PCL 納米纖維的壓電性來自甘氨酸晶體而不是 PCL 基質(圖2E)。如圖2F所示,所有甘氨酸-PCL納米纖維膜都會產生不同的聲壓,而不含甘氨酸的PCL膜只會產生噪聲。在所有實驗中,甘氨酸:PCL重量比為1:1的樣品在相同的施加電壓下提供了最高的輸出和最高的轉換信號。且甘氨酸-PCL納米纖維膜在超聲換能器等驅動應用中的性能優于其他納米纖維膜(圖2G)。
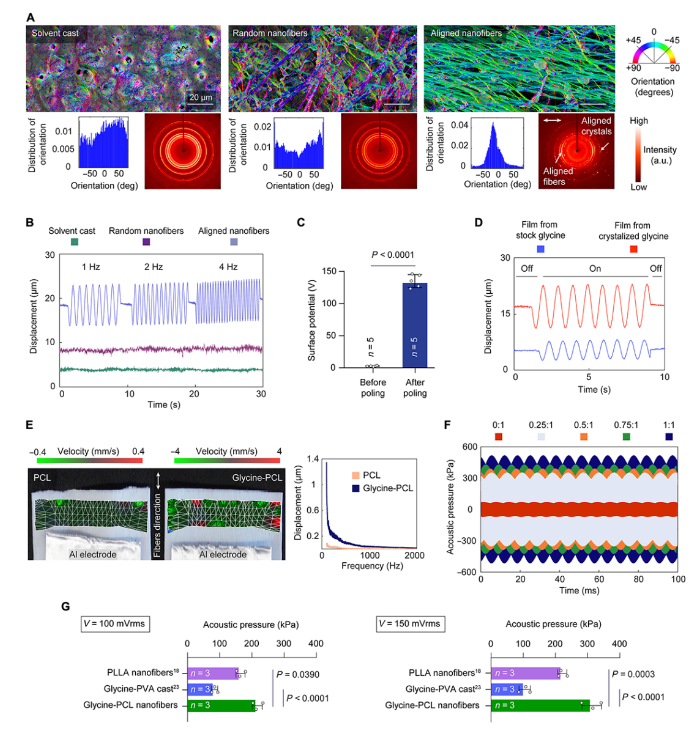
圖2. 壓電機制和壓電性能
圖片來源:Sci. Adv.
如圖3A所示,甘氨酸-PCL納米纖維膜和PCL膜的活/死細胞數與對照組相似,說明甘氨酸-PCL納米纖維膜無細胞毒性。此外,為了進一步證明甘氨酸-PCL納米纖維膜的安全性,對相同的mADSCs進行了流式細胞術檢測。所有組都表現出正常的行為,證明了甘氨酸-PCL納米纖維膜的生物相容性(圖3B-3C)。
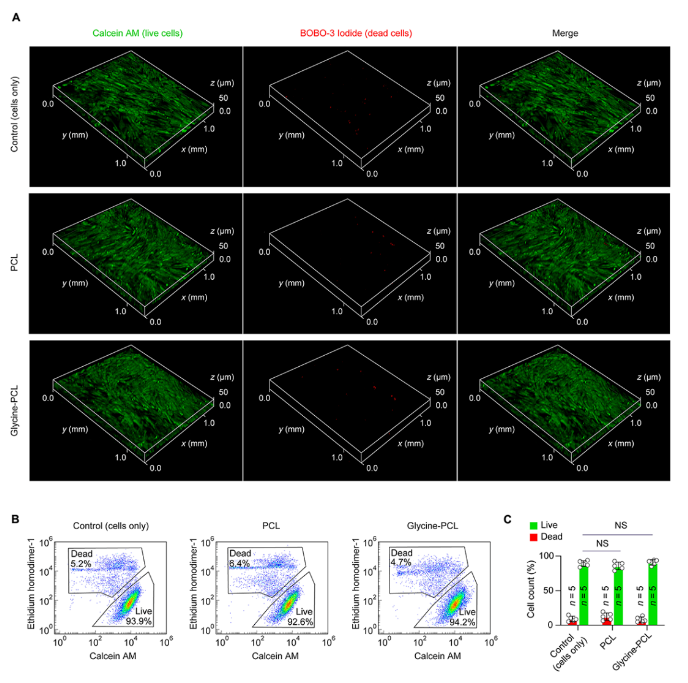
圖3. 甘氨酸-PCL薄膜的體外生物相容性評估
圖片來源:Sci. Adv.
植入的超聲換能器最近已經成為一種有效和安全的方法,以促進將藥物輸送到大腦中的重復血腦屏障(BBB)開放。圖4A介紹了一種可完全生物降解的超聲換能器。所制備的超聲設備由甘氨酸-PCL壓電膜、鉬(Mo)電極和電線制成,并包裹聚乳酸(PLA)層,經過一段可控的時間后,可以在體內安全地降解,以避免傳統超聲換能器經常需要的任何侵入性移除手術(圖4B)。如圖4C所示,將微泡注射到動物的尾靜脈中,使氣泡放大局部超聲脈沖空化,瞬時破壞腦微血管內皮細胞之間的緊密連接,增加BBB的通透性。此外,對大腦進行免疫熒光分析,以檢測葡聚糖的滲漏,葡聚糖滲透到受損的BBB中。對相距2 mm的淺層和深層兩個冠狀腦區域進行成像(圖4D)。微血管(CD31)通過存在均勻的紅色熒光(鈣黃素AM)來區分,其中葡聚糖被明亮的綠色熒光(碘化BOBO-3)檢測到。如圖4E所示,通過甘氨酸-PCL換能器超聲檢測,可以小鼠大腦的各種微血管周圍可以看到明顯數量的葡聚糖。相反,在對照組小鼠的相同冠狀切片上,沒有觀察到類似的信號(圖4E)。小鼠模型中基于甘氨酸-PCL的換能器對 BBB 的顯著破壞表明甘氨酸-PCL 壓電薄膜在這種血腦藥物輸送應用中具有巨大潛力。
最后,作者進行了功能性實驗以確定封裝了90到260 μm厚的PLA的換能器的工作壽命,并證明了在37 °C的PBS中,根據封裝厚度的不同,該器件的壽命為10到25天 (圖4F)。因此,封裝的PLA層允許以定義好的速率完全控制器件退化。所有被測試的器件在其預定的壽命內運行良好,并最終自我降解(圖4G)。
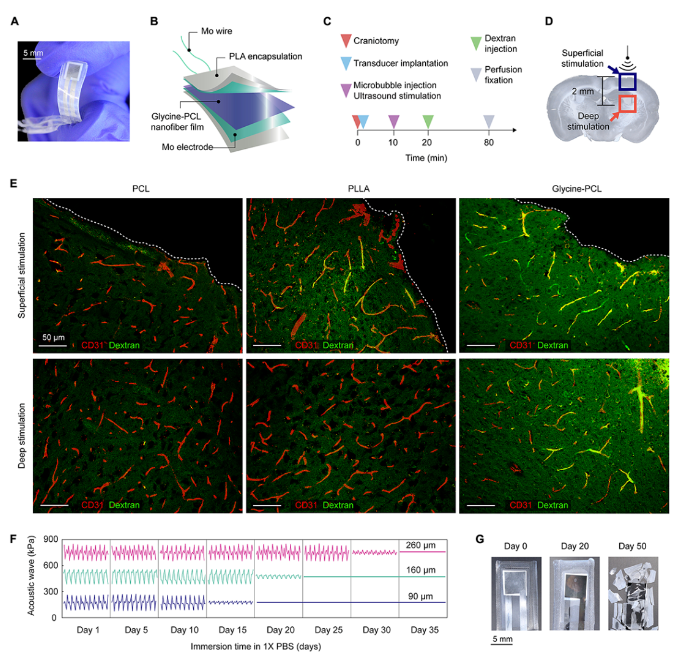
圖4. 用于體內BBB破壞和治療遞送的甘氨酸-PCL超聲換能器
圖片來源:Sci. Adv.
為了進一步證明基于甘氨酸-PCL的超聲換能器增強化療藥物向腦組織輸送的能力,作者評估了攜帶原位GMB腫瘤的裸鼠的抗GBM活性。實驗的感知和時間軸如圖5A和5B所示。在開始時(第0天),進行了開顱手術,并將腫瘤細胞接種到動物的腦中。然后,動物被隨機分成四組。第10天,將可生物降解超聲換能器植入并定位于開顱手術缺損處。超聲后尾靜脈注射PTX-PEG-PLA膠束,劑量為20 mg/kg。在16天內對動物進行6次治療。未接受治療的小鼠,或在沒有超聲治療的情況下接受PTX治療,作為假手術組。每隔2~4 d用IVIS(活體成像系統)監測腫瘤生長情況。在第31天,從每組中隨機抽取兩只動物進行組織學評估,并繼續監測其余動物的存活分析。此外,進行了微型計算機斷層掃描(CT)來跟蹤植入到動物體內的設備(圖5C)。如圖5D所示,從甘氨酸-PCL換能器超聲后接受配方PTX的動物在所有組中表現出最好的抗GBM活性。此外,Kaplan-Meier生存曲線分析(圖5E)表明,甘氨酸-PCL裝置超聲聯合PTX可顯著延長動物的存活時間達72天,中位存活時間為65天,明顯長于假手術組。此外,與所有其他治療組相比,在甘氨酸-PCL換能器超聲作用后接受PTX負載的PEG-PLA膠束治療的小鼠的腫瘤最小(圖5F-5G)。在整個治療期間沒有發現明顯的體重下降和異常行為,表明該治療的安全性很高。這些結果表明,基于甘氨酸-PCL的可生物降解的壓電超聲換能器可以為治療基底膜的新策略提供一個安全而有力的平臺。
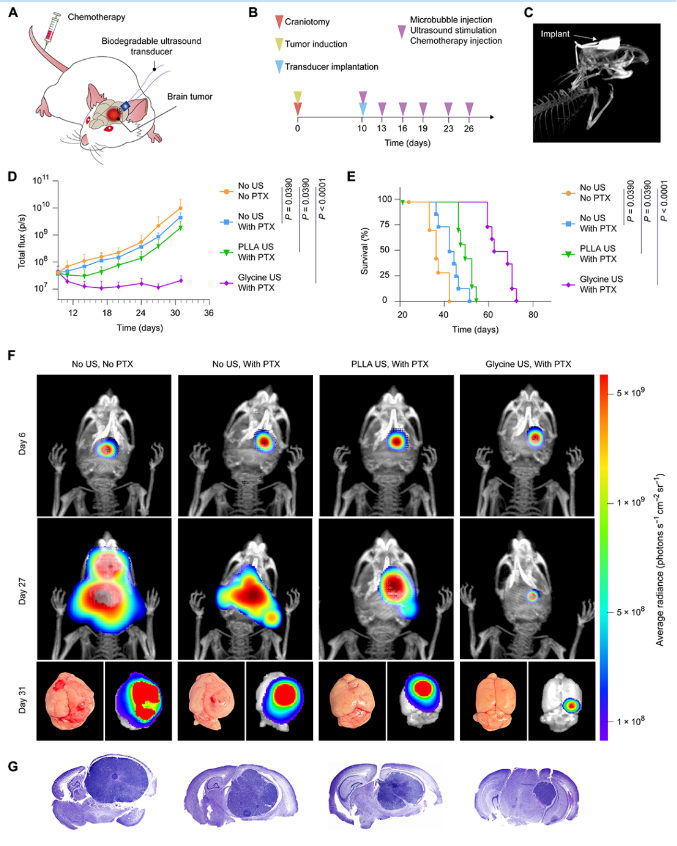
圖5. 用于治療小鼠原位GMB腫瘤的甘氨酸-PCL超聲換能器
圖片來源:Sci. Adv.
總結
美國康涅狄格大學Thanh D. Nguyen & Horea Ilies & Kazem Kazerounian團隊使用靜電紡絲工藝大規模制造具有高度定向甘氨酸晶體的甘氨酸-PCL 納米纖維。特別是,甘氨酸-PCL納米纖維膜具有出色的“有效”壓電系數d33,為19 pC/N。基于甘氨酸-PCL納米纖維的超聲換能器產生顯著水平的超聲,可瞬時打開 BBB 并將藥物模型(葡聚糖)深入腦組織。此外,使用這種基于甘氨酸-PCL的植入式超聲換能器來協助遞送配制的紫杉醇(PTX;一種對繞過BBB具有挑戰性的化療藥物)來治療攜帶原位GBM腫瘤模型的小鼠。且未發現甘氨酸-PCL 超聲換能器治療的顯著副作用。總的來說,這種高壓電、柔性、安全和可生物降解的甘氨酸納米纖維薄膜不僅可以為GBM治療提供有前途的策略,而且可以對許多醫學應用產生顯著影響,從藥物輸送、組織刺激和細胞工程到醫療植入設備,如作為傳感器、執行器和換能器。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn